解题方法
1 . 一水硫酸四氨合铜(Ⅱ)的化学式为 是一种重要的染料及农药中间体。某学习小组以废铜料(含少量铁及难溶性杂质)为主要原料合成该物质,合成路线如下:
是一种重要的染料及农药中间体。某学习小组以废铜料(含少量铁及难溶性杂质)为主要原料合成该物质,合成路线如下:不正确 的是
 是一种重要的染料及农药中间体。某学习小组以废铜料(含少量铁及难溶性杂质)为主要原料合成该物质,合成路线如下:
是一种重要的染料及农药中间体。某学习小组以废铜料(含少量铁及难溶性杂质)为主要原料合成该物质,合成路线如下:
A.操作I中发生的主要反应为: |
| B.操作II中趁热过滤除去的是难溶性杂质和氢氧化铁 |
| C.操作III中洗涤可用乙醇和水的混合液,干燥可采用减压干燥方式 |
| D.设计操作IV的目的是为了提高乙醇的利用率 |
您最近一年使用:0次
解题方法
2 . 氯化亚铜是一种应用较广的催化剂,易水解,微溶于水,不溶于乙醇。以低品位铜矿砂(主要成分CuS)为原料制备氯化亚铜的路线如图:

(1)“酸溶1”步骤中发生反应的化学方程式为___________ 。
(2)用乙醇洗涤的优点为___________ 。
(3)“合成”步骤加入Na2SO3的速率不宜过快,否则会产生___________ 气体(写化学式),除可能与酸溶时硫酸过量有关,还可能的原因是___________ (用离子方程式表示)。
(4)NH3与Cu2+形成配位键的能力___________ (填“强于”或“弱于”)H2O与Cu2+形成配位键的能力。
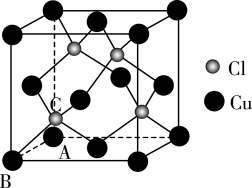
(5)某种铜的氯化物晶体结构如图所示。此晶体中铜原子的配位数是___________ ;设晶胞参数为anm,则该铜的氯化物晶体的密度为___________ g·cm-3(用含a和NA的式子表示,NA为阿伏加德罗常数)
(6)已知: ,
,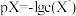 (X-表示Cl-、Br-、I-)。298K时,
(X-表示Cl-、Br-、I-)。298K时, ,
,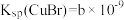 ,
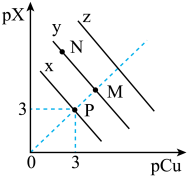
,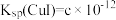 。在CuCl、CuBr、CuI的饱和溶液中阳离子和阴离子浓度关系如图所示。图中x代表
。在CuCl、CuBr、CuI的饱和溶液中阳离子和阴离子浓度关系如图所示。图中x代表___________ 曲线,且Ksp(CuX)=___________ 。

(1)“酸溶1”步骤中发生反应的化学方程式为
(2)用乙醇洗涤的优点为
(3)“合成”步骤加入Na2SO3的速率不宜过快,否则会产生
(4)NH3与Cu2+形成配位键的能力
(5)某种铜的氯化物晶体结构如图所示。此晶体中铜原子的配位数是

(6)已知:
 ,
,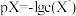 (X-表示Cl-、Br-、I-)。298K时,
(X-表示Cl-、Br-、I-)。298K时, ,
,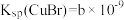 ,
,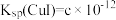 。在CuCl、CuBr、CuI的饱和溶液中阳离子和阴离子浓度关系如图所示。图中x代表
。在CuCl、CuBr、CuI的饱和溶液中阳离子和阴离子浓度关系如图所示。图中x代表
您最近一年使用:0次
名校
解题方法
3 . 将CO或 转化为高附加值化学品是颇具前景的合成路线。
转化为高附加值化学品是颇具前景的合成路线。
(1)相比于煤和石油,天然气作为燃料的主要优点有_______ 。
(2)煤的气化可将煤转化为可燃性气体,写出生成水煤气的化学方程式_______ 。
(3)钴系催化剂催化下CO加氢反应的一种路径如下图所示(*表示微粒吸附在催化剂表面的形态):
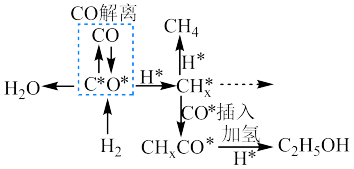
由 和
和 反应生成
反应生成 反应的重要中间体有
反应的重要中间体有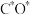 、
、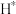 、
、_______ 、 和
和_______ 。
(4) 与二甲醚可发生反应:
与二甲醚可发生反应:
 。反应中二甲醚的平衡转化率与温度和压强的关系见下图:
。反应中二甲醚的平衡转化率与温度和压强的关系见下图:

①
_______ 0(填“大于”“小于”或“等于”)0,a、b、c的大小关系为_______ 。
②TK下,向恒压密闭容器中充入CO和 ,反应前
,反应前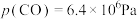 ,
,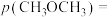
 ;充分反应达到平衡后CO的转化率为25%,则TK下该反应的平衡常数
;充分反应达到平衡后CO的转化率为25%,则TK下该反应的平衡常数
_______ 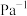 。
。
(5)以 为原料,电解法制取乙烯、乙烷的装置如图,生成乙烷的电极反应式为:
为原料,电解法制取乙烯、乙烷的装置如图,生成乙烷的电极反应式为:_______ ,当左侧有8.96L(标准状况) 反应时,a极区产品中乙烯的体积分数为50%,此时左右两侧溶液质量变化差
反应时,a极区产品中乙烯的体积分数为50%,此时左右两侧溶液质量变化差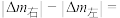
_______ g。
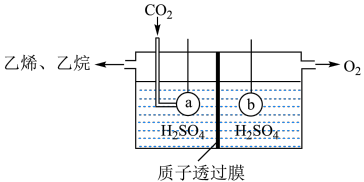
 转化为高附加值化学品是颇具前景的合成路线。
转化为高附加值化学品是颇具前景的合成路线。(1)相比于煤和石油,天然气作为燃料的主要优点有
(2)煤的气化可将煤转化为可燃性气体,写出生成水煤气的化学方程式
(3)钴系催化剂催化下CO加氢反应的一种路径如下图所示(*表示微粒吸附在催化剂表面的形态):

由
 和
和 反应生成
反应生成 反应的重要中间体有
反应的重要中间体有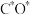 、
、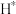 、
、 和
和(4)
 与二甲醚可发生反应:
与二甲醚可发生反应:
 。反应中二甲醚的平衡转化率与温度和压强的关系见下图:
。反应中二甲醚的平衡转化率与温度和压强的关系见下图:
①

②TK下,向恒压密闭容器中充入CO和
 ,反应前
,反应前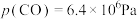 ,
,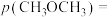
 ;充分反应达到平衡后CO的转化率为25%,则TK下该反应的平衡常数
;充分反应达到平衡后CO的转化率为25%,则TK下该反应的平衡常数
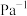 。
。(5)以
 为原料,电解法制取乙烯、乙烷的装置如图,生成乙烷的电极反应式为:
为原料,电解法制取乙烯、乙烷的装置如图,生成乙烷的电极反应式为: 反应时,a极区产品中乙烯的体积分数为50%,此时左右两侧溶液质量变化差
反应时,a极区产品中乙烯的体积分数为50%,此时左右两侧溶液质量变化差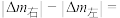

您最近一年使用:0次
4 . CuCl常用作有机合成催化剂,现有如下两种方法制备CuCl。
已知:CuCl晶体呈白色,微溶于水,不溶于稀盐酸和乙醇,露置于潮湿空气中易水解为绿色的 ,见光易分解。
,见光易分解。
方法一:利用热分解 (绿色)制备CuCl,并进行相关探究。
(绿色)制备CuCl,并进行相关探究。
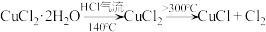

(1)将下列的实验操作按准确的先后顺序排列:a→→→e→→→_____ 。
a.检查装置的气密性后加入药品
b.点燃酒精灯加热至140℃,反应一段时间
c.调整酒精灯温度>300℃,反应一段时间
d.停止通入
e.停止通入HCl,然后通入干燥
f.在“气体入口”处通入干燥HCl
g.熄灭酒精灯
(2)关于上述实验说法正确的是___________(填字母)
方法二:以CuCl(含少量 )粗品为原料制取CuCl,设计的合成路线如下:
)粗品为原料制取CuCl,设计的合成路线如下:

查阅资料可知:
①在较高的盐酸浓度下, 能溶解于甲基异丁基甲酮;
能溶解于甲基异丁基甲酮;
②CuCl在溶液中存在: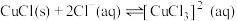 。
。
(3)下列叙述正确的是___________(填字母)。

(4)向混合液中加入去氧水的主要目的是___________ 。
(5)现称取m g产品,用硫酸酸化的硫酸铁溶解,并稀释成250mL。每次用移液管移取25.00mL溶液于锥形瓶中,用c 溶液滴定,平均消耗V mL。
溶液滴定,平均消耗V mL。
①用移液管吸取25.00mL溶液后,将移液管垂直放入稍倾斜的锥形瓶中,___________ ,数秒后,取出移液管。
②有同学认为该实验方案明显不合理,会导致产品中CuCl的纯度严重偏高,理由是___________ 。
已知:CuCl晶体呈白色,微溶于水,不溶于稀盐酸和乙醇,露置于潮湿空气中易水解为绿色的
 ,见光易分解。
,见光易分解。方法一:利用热分解
 (绿色)制备CuCl,并进行相关探究。
(绿色)制备CuCl,并进行相关探究。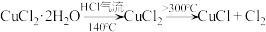

(1)将下列的实验操作按准确的先后顺序排列:a→→→e→→→
a.检查装置的气密性后加入药品
b.点燃酒精灯加热至140℃,反应一段时间
c.调整酒精灯温度>300℃,反应一段时间
d.停止通入

e.停止通入HCl,然后通入干燥

f.在“气体入口”处通入干燥HCl
g.熄灭酒精灯
(2)关于上述实验说法正确的是___________(填字母)
A.若加热时间不足或温度偏低,最终可能混有 |
| B.可通过固体颜色变化,判断反应终点 |
| C.干燥管中最好放无水硫酸铜固体 |
D.通入干燥HCl的作用是防止CuCl被氧化,可用干燥 代替 代替 |
方法二:以CuCl(含少量
 )粗品为原料制取CuCl,设计的合成路线如下:
)粗品为原料制取CuCl,设计的合成路线如下:
查阅资料可知:
①在较高的盐酸浓度下,
 能溶解于甲基异丁基甲酮;
能溶解于甲基异丁基甲酮;②CuCl在溶液中存在:
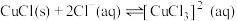 。
。(3)下列叙述正确的是___________(填字母)。

A. 原料中含有的 原料中含有的 经氧化、萃取几乎都在有机相中被除去 经氧化、萃取几乎都在有机相中被除去 |
| B.加入萃取剂后,混合物转移至分液漏斗中,塞上玻璃塞,如图用力振摇 |
C.通入 的目的是将 的目的是将 还原直接生成CuCl沉淀 还原直接生成CuCl沉淀 |
| D.上述合成路线中,一系列操作包括:抽滤、洗涤、干燥,且干燥时应注意密封、避光 |
(5)现称取m g产品,用硫酸酸化的硫酸铁溶解,并稀释成250mL。每次用移液管移取25.00mL溶液于锥形瓶中,用c
 溶液滴定,平均消耗V mL。
溶液滴定,平均消耗V mL。①用移液管吸取25.00mL溶液后,将移液管垂直放入稍倾斜的锥形瓶中,
②有同学认为该实验方案明显不合理,会导致产品中CuCl的纯度严重偏高,理由是
您最近一年使用:0次
5 . 化学在“三废”治理方面发挥着重要的作用。回答下列问题:
Ⅰ.制革厂含硫废水中主要含有 ,需要对含硫废水进行处理与利用。
,需要对含硫废水进行处理与利用。
(1) 的电子式为
的电子式为___________ ;
(2)废水混合处理不但可以同时处理不同类型的废水,同时可以获得某些化工原料。某地区使用含有硫离子的废水治理含有铜离子的废水,写出该反应的离子方程式___________ 。
(3)部分地区采用空气催化氧化法脱硫。该方法以空气中的氧作为氧化剂,将废水中的 转化为
转化为 ,反应中还原剂与氧化剂的物质的量之比为
,反应中还原剂与氧化剂的物质的量之比为___________ 。
Ⅱ.工业上用烟气制酸的废料(主要含S、Se、 、CuO、ZnO、
、CuO、ZnO、 等)为原料提取硒,流程如图:
等)为原料提取硒,流程如图:
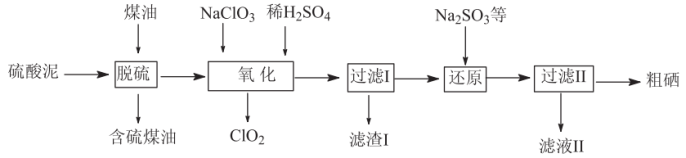
(4)硒与硫是同主族的相邻元素,其在周期表中的位置是___________ 。
(5)“脱硫”过程中,温度控制在95℃,原因是___________ 。
(6)“氧化”过程中,Se转化成弱酸 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
Ⅲ.粗硒经过下列流程可获得亚硒酸钠(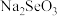 )。
)。
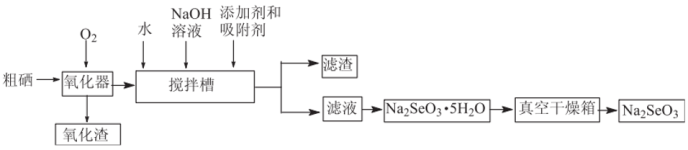
(7)已知在上述合成路线中粗硒在转化为二氧化硒时损失4%,搅拌槽中二氧化硒的利用率为95%,其他损耗忽略不计,试计算利用1t含硒79%的粗硒最终可生产___________ t(精确到0.01t)含亚硒酸钠95%的产品。
Ⅰ.制革厂含硫废水中主要含有
 ,需要对含硫废水进行处理与利用。
,需要对含硫废水进行处理与利用。(1)
 的电子式为
的电子式为(2)废水混合处理不但可以同时处理不同类型的废水,同时可以获得某些化工原料。某地区使用含有硫离子的废水治理含有铜离子的废水,写出该反应的离子方程式
(3)部分地区采用空气催化氧化法脱硫。该方法以空气中的氧作为氧化剂,将废水中的
 转化为
转化为 ,反应中还原剂与氧化剂的物质的量之比为
,反应中还原剂与氧化剂的物质的量之比为Ⅱ.工业上用烟气制酸的废料(主要含S、Se、
 、CuO、ZnO、
、CuO、ZnO、 等)为原料提取硒,流程如图:
等)为原料提取硒,流程如图:
(4)硒与硫是同主族的相邻元素,其在周期表中的位置是
(5)“脱硫”过程中,温度控制在95℃,原因是
(6)“氧化”过程中,Se转化成弱酸
 ,该反应的离子方程式为
,该反应的离子方程式为Ⅲ.粗硒经过下列流程可获得亚硒酸钠(
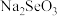 )。
)。
(7)已知在上述合成路线中粗硒在转化为二氧化硒时损失4%,搅拌槽中二氧化硒的利用率为95%,其他损耗忽略不计,试计算利用1t含硒79%的粗硒最终可生产
您最近一年使用:0次
名校
6 . 如图是氯的价类二维图:
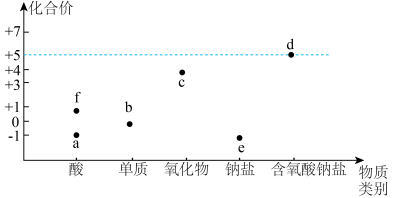
其中c是一种新型净水剂,其合成路线如图:
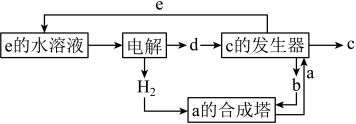
(1)c为___________ (填化学式)。
(2)“a时合成塔”中发生反应的化学方程式为___________ 。
(3)“c的发生器”中发生反应的离子方程式为___________ (写出正确的离子方程式并用单线桥 法分析电子转移的情况)。
(4)实验测得等物质的量的f、 、
、 具有相同的漂白能力,原因是
具有相同的漂白能力,原因是___________ 。
(5)在氧化还原反应中,可将其拆成氧化半反应和还原半反应,比如: 的氧化半反应可以表示为:
的氧化半反应可以表示为: ,电解时生成d的氧化半反应式为
,电解时生成d的氧化半反应式为___________ 。
(6)为测定新型净水剂溶液中c的浓度(加入某种物质使c在溶液中稳定存在),量取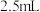 该溶液于锥形瓶中,加蒸馏水稀释到
该溶液于锥形瓶中,加蒸馏水稀释到 ,再加入适量的稀硫酸和碘化钾溶液,此时溶液出现棕色(发生反应:
,再加入适量的稀硫酸和碘化钾溶液,此时溶液出现棕色(发生反应: )。然后用
)。然后用 硫代硫酸钠溶液还原产生的
硫代硫酸钠溶液还原产生的 (发生反应:
(发生反应: ),完全反应时消耗的硫代硫酸钠的体积
),完全反应时消耗的硫代硫酸钠的体积 ,计算此新型净水剂中c的物质的量浓度为
,计算此新型净水剂中c的物质的量浓度为___________ 。

其中c是一种新型净水剂,其合成路线如图:

(1)c为
(2)“a时合成塔”中发生反应的化学方程式为
(3)“c的发生器”中发生反应的离子方程式为
(4)实验测得等物质的量的f、
 、
、 具有相同的漂白能力,原因是
具有相同的漂白能力,原因是(5)在氧化还原反应中,可将其拆成氧化半反应和还原半反应,比如:
 的氧化半反应可以表示为:
的氧化半反应可以表示为: ,电解时生成d的氧化半反应式为
,电解时生成d的氧化半反应式为(6)为测定新型净水剂溶液中c的浓度(加入某种物质使c在溶液中稳定存在),量取
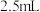 该溶液于锥形瓶中,加蒸馏水稀释到
该溶液于锥形瓶中,加蒸馏水稀释到 ,再加入适量的稀硫酸和碘化钾溶液,此时溶液出现棕色(发生反应:
,再加入适量的稀硫酸和碘化钾溶液,此时溶液出现棕色(发生反应: )。然后用
)。然后用 硫代硫酸钠溶液还原产生的
硫代硫酸钠溶液还原产生的 (发生反应:
(发生反应: ),完全反应时消耗的硫代硫酸钠的体积
),完全反应时消耗的硫代硫酸钠的体积 ,计算此新型净水剂中c的物质的量浓度为
,计算此新型净水剂中c的物质的量浓度为
您最近一年使用:0次
2024-02-20更新
|
99次组卷
|
2卷引用:吉林省长春市东北师大附中2023-2024学年高一上学期期末考试化学试题
7 . 低碳经济已成为人们一种新的生活理念,二氧化碳的捕捉和利用是能源领域的一个重要研究方向。回答下列问题:
(1)工业上用 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知:
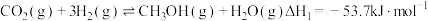
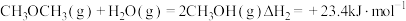
则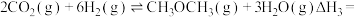
_______ kJ∙mol-1。
(2)二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。科学家提出由 制取
制取 的太阳能工艺如图:
的太阳能工艺如图: ,则
,则 的化学式为
的化学式为_______ ,“热分解系统”中每转移 电子,需消耗
电子,需消耗
_______  。
。
(3)催化时还可以使用一种无机固体电解质作催化剂,其由正离子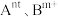 和负离子
和负离子 组成,该物质
组成,该物质 以上形成无序结构(高温相),
以上形成无序结构(高温相), 以下变为有序结构(低温相),二者晶体晶胞结构如图所示:
以下变为有序结构(低温相),二者晶体晶胞结构如图所示:_______ 。
ii.“高温相”具有良好的离子导电性,其主要原因是_______ 。
(4)铜基催化剂 (
( 为
为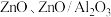 等)是
等)是 加氢制甲醇常用的催化剂,部分合成路线如图所示。
加氢制甲醇常用的催化剂,部分合成路线如图所示。 上发生反应的总化学方程式
上发生反应的总化学方程式_______ 。
(5)利用电解法在碱性或酸性条件下将 还原为
还原为 和
和 的原理如下图所示:
的原理如下图所示: 和法拉第效率(
和法拉第效率(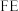 )的定义(X代表
)的定义(X代表 或
或 )如下:
)如下:
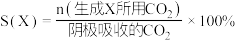

①实验测得,碱性条件生成 总的选择性小于酸性条件,原因是
总的选择性小于酸性条件,原因是_______ 。
②实验测得,酸性条件生成 总的法拉第效率小于碱性条件,原因是
总的法拉第效率小于碱性条件,原因是_______ 。
(1)工业上用
 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知: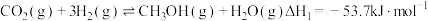
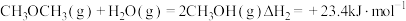
则
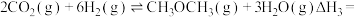
(2)二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。科学家提出由
 制取
制取 的太阳能工艺如图:
的太阳能工艺如图: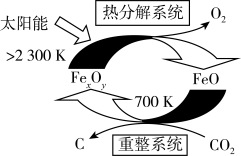
 ,则
,则 的化学式为
的化学式为 电子,需消耗
电子,需消耗
 。
。(3)催化时还可以使用一种无机固体电解质作催化剂,其由正离子
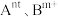 和负离子
和负离子 组成,该物质
组成,该物质 以上形成无序结构(高温相),
以上形成无序结构(高温相), 以下变为有序结构(低温相),二者晶体晶胞结构如图所示:
以下变为有序结构(低温相),二者晶体晶胞结构如图所示: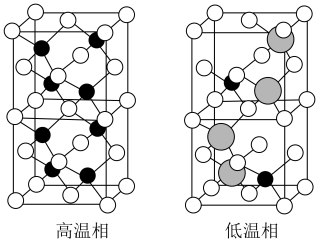
说明:图中,○球为负离子;高温相中的●深色球为正离子或空位;低温相中的 球为
球为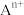 离子,●球为
离子,●球为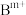 离子。
离子。
ii.“高温相”具有良好的离子导电性,其主要原因是
(4)铜基催化剂
 (
( 为
为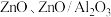 等)是
等)是 加氢制甲醇常用的催化剂,部分合成路线如图所示。
加氢制甲醇常用的催化剂,部分合成路线如图所示。 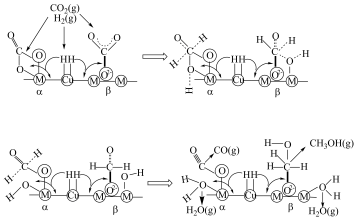
 上发生反应的总化学方程式
上发生反应的总化学方程式(5)利用电解法在碱性或酸性条件下将
 还原为
还原为 和
和 的原理如下图所示:
的原理如下图所示: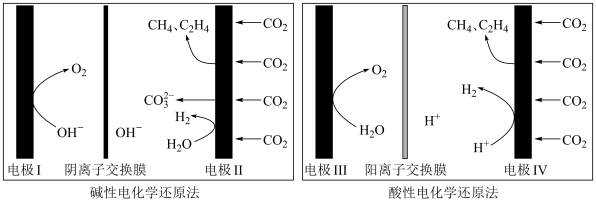
 和法拉第效率(
和法拉第效率( )的定义(X代表
)的定义(X代表 或
或 )如下:
)如下: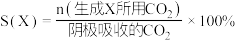

①实验测得,碱性条件生成
 总的选择性小于酸性条件,原因是
总的选择性小于酸性条件,原因是②实验测得,酸性条件生成
 总的法拉第效率小于碱性条件,原因是
总的法拉第效率小于碱性条件,原因是
您最近一年使用:0次
名校
8 . 硼氢化钠(NaBH4)和氨硼烷(BNH6)是优良的储氢材料,合成路线如图所示,下列叙述错误的是


| A.硼氢化钠中阴离子的VSEPR模型为正四面体形 |
| B.反应①中氧化剂与还原剂物质的量之比为1∶2 |
| C.SiO2是反应①的催化剂 |
| D.将氨硼烷移出体系有利于提高反应②转化率 |
您最近一年使用:0次
名校
9 . 纳米氧化亚铜(Cu2O,颗粒直径1~100nm)具有特殊的光学、光电和催化性能,采用化学沉淀法制备晶型结构完整、粒度分布均匀的纳米Cu2O(在潮湿空气中会慢慢氧化生成CuO)的合成路线如图所示。下列说法正确的是
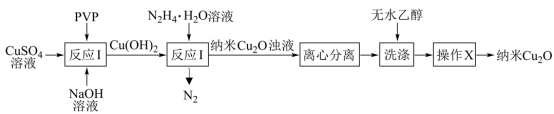

| A.反应Ⅰ为化合反应 |
| B.操作X为过滤 |
| C.反应Ⅱ中,每生成22.4L(标准状况)N2,转移4mol电子 |
| D.“洗涤”时,无水乙醇可用蒸馏水代替 |
您最近一年使用:0次
2021-10-09更新
|
412次组卷
|
3卷引用:重庆市西南大学附属中学2022届高三上学期第二次月考化学试题
解题方法
10 . 尿素还原法合成溴化锂,设备简单、产品质量好、无有毒气体排放、生产成本低。下图是制备无水溴化锂的工艺路线:
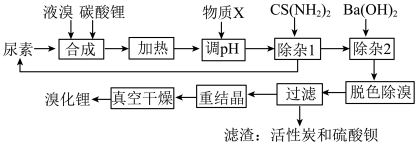
回答下列问题:
(1)Br位于周期表第________ 周期________ 族。
(2)常用焰色试验鉴别碳酸锂,火焰呈现________ 色。
(3)在溶解槽中,边搅拌边分次少量地将细粉末状的碳酸锂溶解于冷的溴水中至饱和为止,选用“冷”的溴水溶解碳酸锂的主要原因________ 。
(4)合成溴化锂的主要化学方程式________ 。
(5)合成时加入液溴会使pH降低,实际生产时需维持pH为4-5,为调节pH为4-5,从生产实际出发物质X最佳为________ 。
(6)加热体系的温度超过80℃会发生副反应:
3Br2+3H2O=5HBr+HBrO3
3HBrO=2HBr+HBrO3
Li2CO3+2HBrO3=2LiBrO3+H2O+CO2↑
还原溴酸锂需要选用硫脲,“除杂1”所发生的化学方程式是________ 。
(7)重结晶的操作为________ 。

温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
碳酸锂溶解度(g) | 1.51 | 1.43 | 1.33 | 1.26 | 1.17 | 1.08 | 1.01 | 0.85 | 0.72 |
(1)Br位于周期表第
(2)常用焰色试验鉴别碳酸锂,火焰呈现
(3)在溶解槽中,边搅拌边分次少量地将细粉末状的碳酸锂溶解于冷的溴水中至饱和为止,选用“冷”的溴水溶解碳酸锂的主要原因
(4)合成溴化锂的主要化学方程式
(5)合成时加入液溴会使pH降低,实际生产时需维持pH为4-5,为调节pH为4-5,从生产实际出发物质X最佳为
(6)加热体系的温度超过80℃会发生副反应:
3Br2+3H2O=5HBr+HBrO3
3HBrO=2HBr+HBrO3
Li2CO3+2HBrO3=2LiBrO3+H2O+CO2↑
还原溴酸锂需要选用硫脲,“除杂1”所发生的化学方程式是
(7)重结晶的操作为
您最近一年使用:0次
2024-04-02更新
|
330次组卷
|
2卷引用:2024届湖北省十一校高三下学期第二次联考化学试卷



