1 . 汽车剧烈碰撞时,安全气囊中发生反应: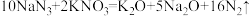 。若氧化产物比还原产物多
。若氧化产物比还原产物多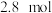 ,则下列判断正确的是
,则下列判断正确的是
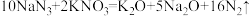 。若氧化产物比还原产物多
。若氧化产物比还原产物多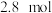 ,则下列判断正确的是
,则下列判断正确的是A.生成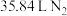 (标准状况) (标准状况) | B.有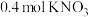 被氧化 被氧化 |
C.转移电子的物质的量为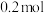 | D.被氧化的N原子的物质的量为 |
您最近一年使用:0次
2021-11-19更新
|
703次组卷
|
2卷引用:河北省沧州市第一中学2021-2022学年高一上学期第二次月考(期中)化学试题
名校
2 . 汽车安全气囊是在发生撞车时,能自动膨胀保护乘员的装置,碰撞时发生的反应为:10NaN3+2KNO3=K2O+5Na2O+16N2↑,已知氧化剂的氧化性大于氧化产物,还原剂的还原性大于还原产物,下列有关该反应的说法正确的是
| A.该反应中,每生成16个N2转移30个电子 |
| B.氧化性:KNO3>N2 |
| C.该反应中KNO3被氧化 |
| D.该反应中N2既是氧化剂又是还原剂 |
您最近一年使用:0次
3 . 二氧化氯具有杀菌消毒作用,是一种广谱型消毒剂。工业上常用 氧化
氧化 制得,方程式为:
制得,方程式为: ,下列相关说法正确的是
,下列相关说法正确的是
 氧化
氧化 制得,方程式为:
制得,方程式为: ,下列相关说法正确的是
,下列相关说法正确的是A.反应中 被氧化 被氧化 | B.消耗5个 时,转移5个电子 时,转移5个电子 |
C. 是还原产物 是还原产物 | D.还原剂与氧化剂的计量系数之比为1∶2 |
您最近一年使用:0次
名校
解题方法
4 . 水热法制备直径为1~100nm的颗粒Y(化合物),反应原理为3Fe2++2S2O +O2+aOH—=Y+S4O
+O2+aOH—=Y+S4O +2H2O,下列说法中错误的是
+2H2O,下列说法中错误的是
 +O2+aOH—=Y+S4O
+O2+aOH—=Y+S4O +2H2O,下列说法中错误的是
+2H2O,下列说法中错误的是| A.a=4 |
| B.将Y均匀分散到水中形成的分散系具有丁达尔效应 |
C.还原剂是Fe2+、S2O |
| D.反应过程中转移电子数为3 |
您最近一年使用:0次
2021-10-22更新
|
185次组卷
|
2卷引用:【石家庄新东方】2021-2022石家庄28中高一化学10月月考
名校
解题方法
5 . 亚氯酸钠( )是一种高效氧化剂和漂白剂。种制备亚氯酸钠粗产品的工艺流程如下:
)是一种高效氧化剂和漂白剂。种制备亚氯酸钠粗产品的工艺流程如下:
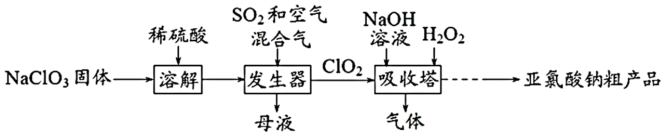
已知:纯 易分解爆炸;
易分解爆炸; 在碱性溶液中稳定存在,在酸性溶液中分解为
在碱性溶液中稳定存在,在酸性溶液中分解为 和
和 。
。
下列说法正确的是
 )是一种高效氧化剂和漂白剂。种制备亚氯酸钠粗产品的工艺流程如下:
)是一种高效氧化剂和漂白剂。种制备亚氯酸钠粗产品的工艺流程如下:
已知:纯
 易分解爆炸;
易分解爆炸; 在碱性溶液中稳定存在,在酸性溶液中分解为
在碱性溶液中稳定存在,在酸性溶液中分解为 和
和 。
。下列说法正确的是
A.发生器中鼓入空气的作用是将 氧化 氧化 |
B.从母液中回收的主要物质是 和 和 |
C.吸收塔内反应的离子方程式为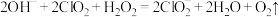 |
D.理论上,每生产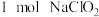 至少需要通入 至少需要通入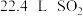 (标准状况) (标准状况) |
您最近一年使用:0次
2021-10-13更新
|
1234次组卷
|
2卷引用:山东省潍坊市安丘市等三县2022届高三10月过程性测试化学试题
6 . 从砷化镓废料(主要成分为 、
、 、
、 和
和 )中回收镓和砷的工艺流程如图所示。
)中回收镓和砷的工艺流程如图所示。
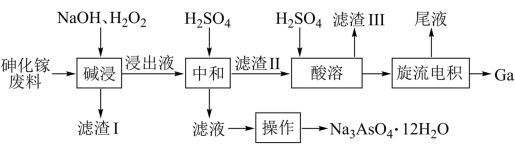
下列说法错误的是
 、
、 、
、 和
和 )中回收镓和砷的工艺流程如图所示。
)中回收镓和砷的工艺流程如图所示。
下列说法错误的是
A.“碱浸”时,温度保持在70℃的目的是提高“碱浸”速率,同时防止 过度分解 过度分解 |
B.“碱浸”时, 被 被 氧化,每反应 氧化,每反应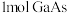 ,转移电子的数目为 ,转移电子的数目为 |
C.“旋流电积”所得“尾液”溶质主要是 ,可进行循环利用,提高经济效益 ,可进行循环利用,提高经济效益 |
D.该工艺得到的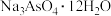 纯度较低,可以通过重结晶的方法进行提纯 纯度较低,可以通过重结晶的方法进行提纯 |
您最近一年使用:0次
2021-09-09更新
|
1505次组卷
|
13卷引用:全国2022届高三上学期第一次学业质量联合检测化学试题
全国2022届高三上学期第一次学业质量联合检测化学试题山东省潍坊市第一中学2022届高三10月月考化学试题安徽省合肥工业大学附属中学2021-2022学年高三上学期第一次阶段考试化学试题陕西省西安市长安区第一中学2022届高三第一次模拟考试化学试题(已下线)专题06 金属及其化合物-2022年高考化学二轮复习重点专题常考点突破练(已下线)提升卷02-【新高考新题型】2022年高考化学选择题标准化练习20卷(山东专用)安徽省宿松中学2021-2022学年高三上学期第一次联考化学试题福建省莆田第一中学2021-2022学年高三上学期10月月考化学试题黑龙江省大庆铁人中学2021-2022学年高三上学期第二次月考化学试题(已下线)押新高考卷03题 元素化合物的性质-备战2022年高考化学临考题号押题(新高考通版)湖南省株洲市攸县第一中学2022-2023学年高三上学期第一次月考化学试题湖南省吉首市泸溪一中2022届高三第三次联合检测化学试题福建省莆田第二十五中学2022-2023学年高三上学期期中考试化学试题
10-11高二上·甘肃武威·阶段练习
名校
解题方法
7 . 在FeCl3、CuCl2、FeCl2的混合溶液中,Fe3+、Cu2+、Fe2+的物质的量之比为3:2:1,现加入适量铁粉,使溶液中三种离子物质的量浓度之比变为1:2:4,则参加反应的铁粉和原溶液中Fe3+的物质的量之比为
| A.2:1 | B.1:2 | C.1:3 | D.1:4 |
您最近一年使用:0次
2021-09-09更新
|
1700次组卷
|
28卷引用:2010年甘肃省武威五中高二11月月考化学试卷
(已下线)2010年甘肃省武威五中高二11月月考化学试卷2015届河北省邯郸市高三上学期1月教学质量检测化学试卷2014-2015江西省新余市高一上学期期末考试化学试卷2014-2015学年辽宁师大附中高二下学期期末考试化学试卷2015-2016学年陕西省长安区一中高一上期末化学试卷(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第3讲 铁及其化合物【押题专练】【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高一上学期12月月考化学试题安徽省阜阳市第三中学2018-2019学年高一上学期小期末考试(期末模拟)化学试题河北省大名县第一中学2020届高三9月月考化学试题河北省武安市第一中学2020届高三9月月考化学试题甘肃省兰州市第一中学2020届高三9月月考化学试题宁夏石嘴山市第三中学2019-2020学年高一上学期第二次(12月)月考化学试题安徽省安庆一中2018-2019学年高一上学期期末考试化学试题安徽省太和第一中学2019-2020学年高一上学期期末考试化学试题人教版高中化学必修1第三章《金属及其化合物》测试卷2专题1.3 氧化还原反应(综合提升卷)——巅峰冲刺2020年高考化学二轮专项提升(已下线)3.1.2 铁的氢氧化物 铁盐和亚铁盐练习(1)——《高中新教材同步备课》(人教版 必修第一册)(已下线)第03章 铁 金属材料(B卷能力提高篇)——2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)人教版(2019)高一必修第一册第三章 铁 金属材料 素养拓展区人教版(2019)高一必修第一册 第三章素养检测江西省鹰潭市第一中学2021届高三上学期期中考试化学试题重庆市三峡名校联盟2020-2021学年高一上学期12月联考化学试题四川省仁寿第一中学校南校区2020-2021学年高一下学期开学考试化学试题(已下线)8.1 铁及其化合物-2020-2021学年秋季班高二上学期化学教材知识点精讲练(沪科版)(已下线)3.1.2 不同价态铁元素之间的转化-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)黑龙江省七台河市勃利县高级中学2021-2022学年高三上学期期中考试化学试题广东省普宁市华侨中学2021—2022学年高一上学期第三次月考化学试题陕西省延安子长市中学2021-2022学年高三上学期期中考试化学试题
13-14高三·宁夏银川·阶段练习
名校
解题方法
8 . 足量铜与一定量的浓硝酸反应,得到硝酸铜溶液和二氧化氮、一氧化氮的混合气体2.24L(标准状况),这些气体与一定体积(标准状况)氧气混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入4mol·L-1氢氧化钠溶液至铜离子恰好完全沉淀,则消耗氢氧化钠溶液的体积是50mL,下列说法正确的是
| A.混合气体中含二氧化氮1.12L |
| B.消耗氧气的体积为1.68L |
| C.此反应过程中转移的电子为0.3mol |
| D.参加反应的硝酸是0.4mol |
您最近一年使用:0次
2021-08-25更新
|
798次组卷
|
30卷引用:2015届宁夏银川一中高三第四次月考化学试卷
(已下线)2015届宁夏银川一中高三第四次月考化学试卷2014-2015吉林省松原市扶余县一中高一上学期期末化学试卷2015届山东省滕州市三中上学期高三第四次月考理综化学试卷2016届河南省扶沟县高级中学高三上学期开学考试化学试卷2016届河南省三门峡市陕州中学高三上学期第一次精英对抗赛化学试卷2016届重庆市万州第二高级中学高三上学期期中测试理综化学试卷2015-2016学年河北省冀州中学高一下开学考试化学试卷2016届河南省信阳市鸡公山风景区学校高三下2月月考化学试卷2015-2016学年安徽省六安一中高一下周末作业二化学试卷2015-2016学年安徽师大附中高一下学期期中考查化学试卷2015-2016学年山东省淄博六中高一下学科竞赛化学试卷2017届广西桂林市第十八中学高三上第二次月考化学试卷2018届高三一轮复习化学:考点21-铜及其化合物性质探究(已下线)《考前20天终极攻略》-5月26日 元素及其化合物福建省三明市第一中学2018-2019学年高二上学期开学考化学试题云南省新平县一中2018-2019学年高一上学期12月月考化学试题贵州省黔南布依族苗族自治州龙里中学2019-2020学年高一上学期期末考试化学试题辽宁省大连市一〇三中学2019-2020学年高一下学期期中考试化学试题河南省漯河市临颍县南街高级中学2020届高三阶段性测试化学试题安徽省芜湖市2021届高三第二次月考化学试题江西省高安中学2020-2021学年高一上学期期末考试化学试题四川省邻水实验学校2020-2021学年高一下学期第一次月考化学试题福建省福州第三中学2020-2021学年高一下学期期中考化学试题(已下线)专题02 氮及其化合物【专项训练】-2020-2021学年高一化学下学期期末专项复习(人教版2019必修第二册)(已下线)专题13 氮及其化合物 (热点讲义)-2022年高三毕业班化学常考点归纳与变式演练 浙江省诸暨市第二高级中学2020-2021学年高二下学期期中考试化学试题内蒙古自治区包钢第一中学2021-2022学年高三上学期10月月考化学试题重庆市第七中学校2021-2022学年高一下学期3月月考化学试题云南省普洱市镇沅彝族哈尼族拉祜族自治县第一中学2021-2022学年高一下学期4月份考试化学试题湖南省怀化市沅陵县第一中学2021-2022学年高一下学期第一次月考化学试题
名校
9 . 利用 氧化尿素制备
氧化尿素制备 (水合肼)的实验流程如图所示:
(水合肼)的实验流程如图所示: 有强还原性,能与
有强还原性,能与 剧烈反应生成
剧烈反应生成 。
。
下列说法不正确的是
 氧化尿素制备
氧化尿素制备 (水合肼)的实验流程如图所示:
(水合肼)的实验流程如图所示: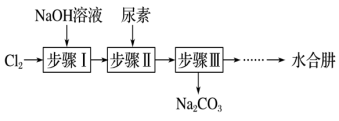
 有强还原性,能与
有强还原性,能与 剧烈反应生成
剧烈反应生成 。
。下列说法不正确的是
| A.步骤Ⅰ中为避免温度过高,可采用冰水浴 |
B.步骤Ⅰ制备 溶液时,测得产物中 溶液时,测得产物中 与 与 的物质的量之比为5∶1,则参与反应的氧化剂与还原剂的物质的量之比为5∶3 的物质的量之比为5∶1,则参与反应的氧化剂与还原剂的物质的量之比为5∶3 |
C.步骤Ⅱ中可将尿素水溶液逐滴滴入 碱性溶液中 碱性溶液中 |
D.生成水合肼反应的离子方程式为ClO﹣+CO(NH2)2+2OH﹣=Cl-+N2H4•H2O+CO |
您最近一年使用:0次
2021-07-24更新
|
1575次组卷
|
10卷引用:辽宁省铁岭市六校2020-2021学年高二下学期期末联考化学试题
辽宁省铁岭市六校2020-2021学年高二下学期期末联考化学试题山西省运城市2021-2022学年高三上学期期中考试化学试题(已下线)第二章 单元检测-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)2021年北京高考化学试题变式题1-10 河南大学附属中学2022-2023学年高一下学期第一次月考化学试题江苏省南菁高级中学2023-2024学年高一上学期9月阶段性检测化学(创优班)试题江苏省南京市第九中学2023-2024学年高一上学期10月阶段学情调研化学试题江苏省苏州市吴县中学2023-2024学年高一上学期12月月考化学试题四川省成都市树德中学2023-2024学年高一下学期3月月考化学试题安徽省马鞍山市第二中学2023-2024学年高一下学期期中测试(实验班)化学试卷
解题方法
10 .  是火箭的固体燃料,发生的反应为
是火箭的固体燃料,发生的反应为 ,下列说法不正确的是
,下列说法不正确的是
 是火箭的固体燃料,发生的反应为
是火箭的固体燃料,发生的反应为 ,下列说法不正确的是
,下列说法不正确的是A. 完全分解产生标准状况下气体体积为 完全分解产生标准状况下气体体积为 |
B. 溶于水,溶液中含氮微粒的物质的量共 溶于水,溶液中含氮微粒的物质的量共 |
C.产生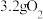 时被氧元素还原而生成的氯气有 时被氧元素还原而生成的氯气有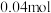 |
| D.反应中氧化产物与还原产物的分子总数之比为3:1 |
您最近一年使用:0次



