名校
1 . 在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如图:
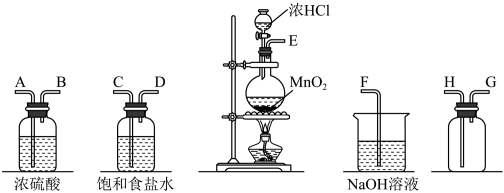
(1)连接上述仪器的正确顺序是(填各接口处的字母): E接_______ ,_______ 接_______ ,B接_______ ,_______ 接F。
(2)上述制备氯气的化学方程式为:_______ 。该反应中浓HCl体现出来的性质:_______ 。
(3)在上述装置中饱和食盐水的作用是_______ , 浓硫酸的作用是_______ 。用离子方程式表示F中NaOH的作用_______ 。
(4)实验中为了检验Cl2有没有收集满,常用湿润的淀粉-KI试纸靠近瓶口,如果Cl2收集满了,可观察到的现象是_______
(5)为了验证氯气的氧化性,将氯气通入Na2SO3溶液中,检验出反应后溶液中含有SO 和Cl-,写出Cl2与Na2SO3反应的离子方程式:
和Cl-,写出Cl2与Na2SO3反应的离子方程式:_______ 。

(1)连接上述仪器的正确顺序是(填各接口处的字母): E接
(2)上述制备氯气的化学方程式为:
(3)在上述装置中饱和食盐水的作用是
(4)实验中为了检验Cl2有没有收集满,常用湿润的淀粉-KI试纸靠近瓶口,如果Cl2收集满了,可观察到的现象是
(5)为了验证氯气的氧化性,将氯气通入Na2SO3溶液中,检验出反应后溶液中含有SO
 和Cl-,写出Cl2与Na2SO3反应的离子方程式:
和Cl-,写出Cl2与Na2SO3反应的离子方程式:
您最近一年使用:0次
名校
2 .  是一种有还原性的气体,可以将
是一种有还原性的气体,可以将 还原为Fe,自身被氧化为
还原为Fe,自身被氧化为 。某学习小组欲制备氨气以还原氧化铁并探究反应产物的成分。
。某学习小组欲制备氨气以还原氧化铁并探究反应产物的成分。
已知:①实验室可用 固体与碱石灰[(NaOH、CaO、
固体与碱石灰[(NaOH、CaO、 的混合物]共热制备氨气。
的混合物]共热制备氨气。
②无水 ——白色粉末,
——白色粉末, 晶体——蓝色晶体
晶体——蓝色晶体
(1)下列各装置中可用于实验室制备氨气的是___________。
(2) 还原
还原 的实验装置如下图:
的实验装置如下图:
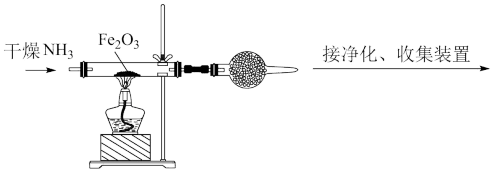
①氨气与氧化铁反应的化学方程式为:___________ 。
②装置右侧干燥管中装有无水硫酸铜,其作用是___________ 。
(3)反应一段时间后试管中固体变为黑色,小组同学为探究黑色固体的成分,进行了如下实验:取反应后黑色固体适量加入足稀盐酸,固体完全溶解,并放出大量气泡。取所得溶液分置于两支试管中,向一支试管中滴入2-3滴KSCN溶液,溶液不变色;向另一支试管中滴加2-3滴酸性 溶液,紫色褪去。
溶液,紫色褪去。
①该小组同学由此确定反应后的黑色固体中不含 ,该结论是否正确?
,该结论是否正确? ___________ (填“是”或“否”);说明你的理由,理由是___________ 。
②假设该反应所得黑色固体的成分只有纯净的铁粉或铁粉与氧化铁的混合物两种可能,请提出一种方案确证之_____________ 。
 是一种有还原性的气体,可以将
是一种有还原性的气体,可以将 还原为Fe,自身被氧化为
还原为Fe,自身被氧化为 。某学习小组欲制备氨气以还原氧化铁并探究反应产物的成分。
。某学习小组欲制备氨气以还原氧化铁并探究反应产物的成分。已知:①实验室可用
 固体与碱石灰[(NaOH、CaO、
固体与碱石灰[(NaOH、CaO、 的混合物]共热制备氨气。
的混合物]共热制备氨气。②无水
 ——白色粉末,
——白色粉末, 晶体——蓝色晶体
晶体——蓝色晶体(1)下列各装置中可用于实验室制备氨气的是___________。
A.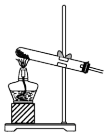 | B. | C.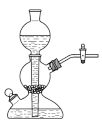 | D.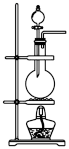 |
 还原
还原 的实验装置如下图:
的实验装置如下图:
①氨气与氧化铁反应的化学方程式为:
②装置右侧干燥管中装有无水硫酸铜,其作用是
(3)反应一段时间后试管中固体变为黑色,小组同学为探究黑色固体的成分,进行了如下实验:取反应后黑色固体适量加入足稀盐酸,固体完全溶解,并放出大量气泡。取所得溶液分置于两支试管中,向一支试管中滴入2-3滴KSCN溶液,溶液不变色;向另一支试管中滴加2-3滴酸性
 溶液,紫色褪去。
溶液,紫色褪去。①该小组同学由此确定反应后的黑色固体中不含
 ,该结论是否正确?
,该结论是否正确? ②假设该反应所得黑色固体的成分只有纯净的铁粉或铁粉与氧化铁的混合物两种可能,请提出一种方案确证之
您最近一年使用:0次
3 . 以冶铝的废弃物铝灰为原料制取超细a-氧化铝,既降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为Al2O3(含少量杂质SiO2、FeO、Fe2O3),其制备实验流程图如下:

(1)铝灰中氧化铝与硫酸反应的化学方程式为_______ 。
(2)加30%的H2O2作用为将Fe2+氧化为Fe3+,其发生的离子反应方程式为__________ 。该反应需控制温度低于40℃,其目的是_____________ 。
(3)煅烧硫酸铝铵晶体,发生的主要反应为:4[NH4Al(SO4)2·12H2O]=2Al2O3+2NH3↑+5SO3↑+3SO2↑+N2↑+53H2O,将产生的气体通过如图所示的装置。

①足量饱和NaHSO3溶液吸收的物质除大部分H2O外还有________ (填化学式)。集气瓶中收集到的气体是_______ 。
②KMnO4溶液褪色(MnO4-还原为Mn2+),发生的离子方程式为_____________ 。

(1)铝灰中氧化铝与硫酸反应的化学方程式为
(2)加30%的H2O2作用为将Fe2+氧化为Fe3+,其发生的离子反应方程式为
(3)煅烧硫酸铝铵晶体,发生的主要反应为:4[NH4Al(SO4)2·12H2O]=2Al2O3+2NH3↑+5SO3↑+3SO2↑+N2↑+53H2O,将产生的气体通过如图所示的装置。

①足量饱和NaHSO3溶液吸收的物质除大部分H2O外还有
②KMnO4溶液褪色(MnO4-还原为Mn2+),发生的离子方程式为
您最近一年使用:0次
名校
4 . 据报道,磷酸二氢钾(KH2PO4)大晶体已应用于我国研制的巨型激光器“神光二号”中。利用氟磷灰石(化学式为Ca5P3FO12)制备磷酸二氢钾的工艺流程如下图所示(部分流程步骤已省略):
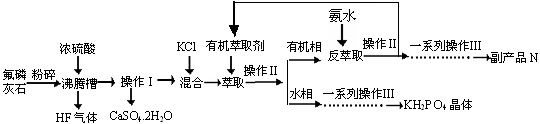
已知萃取的主要反应原理:KCl+H3PO4 KH2PO4+HCl;其中,反应产生的HCl易溶于有机萃取剂。
KH2PO4+HCl;其中,反应产生的HCl易溶于有机萃取剂。
请回答下列问题:
(1)流程中将氟磷灰石粉碎的目的是__________________________________ 。
(2)不能使用二氧化硅陶瓷材质的沸腾槽的主要原因是____________ (用化学方程式表示)。
(3)副产品N的化学式是____________ ;在得到KH2PO4晶体的一系列操作Ⅲ,其主要包括____________ 、过滤、洗涤、干燥等。
(4)若用1000kg质量分数为50.4%的氟磷灰石(化学式为Ca5P3FO12,摩尔质量为504g/mol)来制取磷酸二氢钾晶体,其产率为80%,则理论上可生产KH2PO4(摩尔质量为136g/mol)的质量为_______ kg。
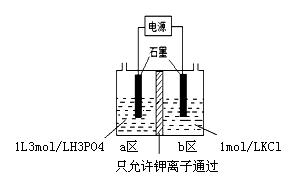
(5)电解法制备KH2PO4的装置如图所示.该电解装置中,a 区属于_______ 区(填“阳极”或“阴极”),阴极区的电极反应式是________________ 。
(6)工业上还可以用氟磷灰石与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,同时逸出SiF4和CO,该反应的化学方程式为________________________________________ 。

已知萃取的主要反应原理:KCl+H3PO4
 KH2PO4+HCl;其中,反应产生的HCl易溶于有机萃取剂。
KH2PO4+HCl;其中,反应产生的HCl易溶于有机萃取剂。请回答下列问题:
(1)流程中将氟磷灰石粉碎的目的是
(2)不能使用二氧化硅陶瓷材质的沸腾槽的主要原因是
(3)副产品N的化学式是
(4)若用1000kg质量分数为50.4%的氟磷灰石(化学式为Ca5P3FO12,摩尔质量为504g/mol)来制取磷酸二氢钾晶体,其产率为80%,则理论上可生产KH2PO4(摩尔质量为136g/mol)的质量为
(5)电解法制备KH2PO4的装置如图所示.该电解装置中,a 区属于

(6)工业上还可以用氟磷灰石与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,同时逸出SiF4和CO,该反应的化学方程式为
您最近一年使用:0次
2018-05-13更新
|
1519次组卷
|
6卷引用:【校级联考】广东省中山一中、仲元中学等七校2019届高三上学期第二次联考(11月)理科综合化学试题



