1 . Ⅷ族元素铁及其化合物性质多样,大多发生氧化还原反应.
(1)高铁酸钠( )是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾强,其本身在反应中被还原为
)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾强,其本身在反应中被还原为 .请配平如下制取高铁酸钠的化学方程式.
.请配平如下制取高铁酸钠的化学方程式._______
______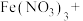 ______NaOH+______
______NaOH+______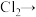 _____
_____ _____
_____ _____NaCl+_____
_____NaCl+_____
(2)在如图所示的装置中,用NaOH溶液、铁粉、稀 等试剂制备氢氧化亚铁.
等试剂制备氢氧化亚铁.
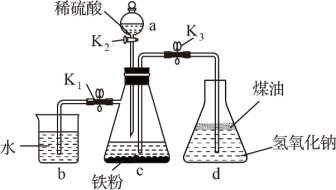
①仪器a的名称是______ .
②关闭 ,打开
,打开 和
和 ,向仪器c中加入适量稀硫酸,关闭
,向仪器c中加入适量稀硫酸,关闭 ,写出装置c中发生反应的离子方程式
,写出装置c中发生反应的离子方程式____________ .同时c中有气体产生,该气体的作用是______ .
③当仪器b中产生均匀气泡后的操作是______ .写出仪器c、d中可能出现的实验现象______ .
(3)已知 .向2支试管中各加入5 mL
.向2支试管中各加入5 mL 
 溶液,若直接通入
溶液,若直接通入 至饱和,1小时后,溶液逐渐变为浅绿色;若先滴加2滴浓盐酸,再通入
至饱和,1小时后,溶液逐渐变为浅绿色;若先滴加2滴浓盐酸,再通入 至饱和,几分钟后,溶液由黄色变为浅绿色.由此可知:促使该氧化还原反应快速发生,可采取的措施是
至饱和,几分钟后,溶液由黄色变为浅绿色.由此可知:促使该氧化还原反应快速发生,可采取的措施是______ .
(1)高铁酸钠(
 )是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾强,其本身在反应中被还原为
)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾强,其本身在反应中被还原为 .请配平如下制取高铁酸钠的化学方程式.
.请配平如下制取高铁酸钠的化学方程式.______
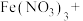 ______NaOH+______
______NaOH+______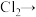 _____
_____ _____
_____ _____NaCl+_____
_____NaCl+_____
(2)在如图所示的装置中,用NaOH溶液、铁粉、稀
 等试剂制备氢氧化亚铁.
等试剂制备氢氧化亚铁.
①仪器a的名称是
②关闭
 ,打开
,打开 和
和 ,向仪器c中加入适量稀硫酸,关闭
,向仪器c中加入适量稀硫酸,关闭 ,写出装置c中发生反应的离子方程式
,写出装置c中发生反应的离子方程式③当仪器b中产生均匀气泡后的操作是
(3)已知
 .向2支试管中各加入5 mL
.向2支试管中各加入5 mL 
 溶液,若直接通入
溶液,若直接通入 至饱和,1小时后,溶液逐渐变为浅绿色;若先滴加2滴浓盐酸,再通入
至饱和,1小时后,溶液逐渐变为浅绿色;若先滴加2滴浓盐酸,再通入 至饱和,几分钟后,溶液由黄色变为浅绿色.由此可知:促使该氧化还原反应快速发生,可采取的措施是
至饱和,几分钟后,溶液由黄色变为浅绿色.由此可知:促使该氧化还原反应快速发生,可采取的措施是
您最近一年使用:0次
名校
解题方法
2 . 一氧化二氯(Cl2O)是一种工业上常用的氯化剂和氧化剂,还可用作灭菌和漂白。常压下,Cl2O的熔点为-120.6°C,沸点为3.5°C,遇水会发生反应。某化学实验小组用纯碱和氯气利用下图中装置制备Cl2O(夹持装置、装置C中的冷却装置或加热装置均略去)。

回答下列问题:
(1)分液漏斗使用前必须进行的操作为_______ ,欲使分液漏斗内的浓盐酸顺利滴下,可将分液漏斗上部的玻璃塞打开或_______ 。
(2)装置的正确连接顺序是_______ (按气流方向,用小写字母表示)。
(3)装置C中发生Cl2O的制备反应中的固体产物为NaHCO3和NaCl,写出该反应的化学方程式_______ 。反应一段时间后,装置B中观察到的实验现象为_______ 。
(4)研究表明,装置B中Cl2O的收率与装置C的温度和纯碱的含水量的关系如下表所示:
本实验中适宜选用的温度范围和纯碱的含水量分别为_______ 、_______ 。
(5)装置F中盛放碱石灰的仪器名称为_______ ,碱石灰的作用为_______ 。
(6)若将少量Cl2O气体通入用稀硫酸酸化的KI-淀粉溶液中,溶液会变蓝色,溶液变蓝色的原因为_______ (用离子方程式表示)。

回答下列问题:
(1)分液漏斗使用前必须进行的操作为
(2)装置的正确连接顺序是
(3)装置C中发生Cl2O的制备反应中的固体产物为NaHCO3和NaCl,写出该反应的化学方程式
(4)研究表明,装置B中Cl2O的收率与装置C的温度和纯碱的含水量的关系如下表所示:
| 温度/°C | 纯碱中含水量/% | Cl2O的收率/% |
| 0~10 | 5.44 | 67.85 |
| 0~10 | 7.88 | 89.26 |
| 10~20 | 8.00 | 64.24 |
| 30~40 | 10.25 | 52.63 |
| 30~40 | 12.50 | 30.38 |
(5)装置F中盛放碱石灰的仪器名称为
(6)若将少量Cl2O气体通入用稀硫酸酸化的KI-淀粉溶液中,溶液会变蓝色,溶液变蓝色的原因为
您最近一年使用:0次
2022-06-27更新
|
292次组卷
|
2卷引用:新疆莎车县第一中学2022-2023学年高三上学期11月月考化学试题
名校
解题方法
3 . 铁是人类较早使用的金属之一。运用铁及其化合物的知识,完成下列问题。
(1)向沸水中逐滴滴加lmol/LFeCl3溶液﹐至液体呈透明的红褐色,该分散系中粒子直径的范围是_______ nm。
(2)在实验室中,FeCl3可以用铁粉与_______ 反应制备,保存FeCl2溶液会加入少量铁屑,其原理是_______ (用化学方程式表示)。
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:_______ 。某校同学为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:
①甲同学取少量待测溶液﹐滴入_______ (写出试剂名称),溶液呈红色,证明溶液中含有Fe3+。
②乙同学取少量待测溶液﹐滴加酸性高锰酸钾溶液,振荡后紫红色褪去,因此他得出结论,溶液中存在Fe2+。丙同学认为乙同学的实验方法不严谨,理由是_______ 。(用离子方程式和必要的文字进行解释)已知:氧化性KMnO4>Cl2
③通过查阅资料,同学们得知,Fe2+能与K3[Fe(CN)6)]溶液反应生成Fe3[Fe(CN)6)]2蓝色沉淀。乙同学另取少量待测溶液﹐滴加K3[Fe(CN)6)]溶液,有蓝色沉淀生成,证明溶液中存在Fe2+。该反应的离子方程式为_______ 。
(4)欲从FeCl3腐蚀铜后所得溶液中回收铜,并重新获得FeCl3溶液,设计实验方案如下:
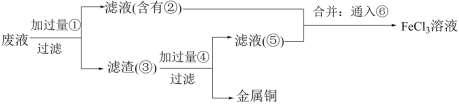
已知⑥为黄绿色的气体单质,请写出通入⑥的离子方程式:_______ 。用H2O2代替⑥也能实现实验目的。请写出加入H2O2的离子方程式:_______ 。
(1)向沸水中逐滴滴加lmol/LFeCl3溶液﹐至液体呈透明的红褐色,该分散系中粒子直径的范围是
(2)在实验室中,FeCl3可以用铁粉与
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:
①甲同学取少量待测溶液﹐滴入
②乙同学取少量待测溶液﹐滴加酸性高锰酸钾溶液,振荡后紫红色褪去,因此他得出结论,溶液中存在Fe2+。丙同学认为乙同学的实验方法不严谨,理由是
③通过查阅资料,同学们得知,Fe2+能与K3[Fe(CN)6)]溶液反应生成Fe3[Fe(CN)6)]2蓝色沉淀。乙同学另取少量待测溶液﹐滴加K3[Fe(CN)6)]溶液,有蓝色沉淀生成,证明溶液中存在Fe2+。该反应的离子方程式为
(4)欲从FeCl3腐蚀铜后所得溶液中回收铜,并重新获得FeCl3溶液,设计实验方案如下:
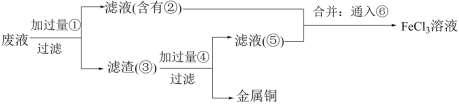
已知⑥为黄绿色的气体单质,请写出通入⑥的离子方程式:
您最近一年使用:0次
2022-04-05更新
|
406次组卷
|
2卷引用:新疆维吾尔自治区乌鲁木齐市第一中学2021--2022学年高一上学期期末考试化学试题
名校
4 . 根据已经学过的化学知识,回答下列问题。
I.金属及其化合物在生产生活中有着广泛的应用。
(1)胃舒平(主要成分为氢氧化铝)可用于治疗胃酸过多,氢氧化铝体现___________ 性;___________ (填“能”或“不能”)用氢氧化钠溶液代替。
(2)将Cu与稀硫酸混合,二者不能反应,滴入 后,溶液很快变成蓝色,该反应的化学方程式为
后,溶液很快变成蓝色,该反应的化学方程式为___________ 。
(3) 是一种酸式盐,写出
是一种酸式盐,写出 在水中的电离方程式:
在水中的电离方程式:___________ 。
(4)Na2CO3和NaHCO3是厨房中常见的两种盐,可用化学性质的差异进行鉴别。回答下列问题:
①与酸反应的差异。甲组进行了如下4组实验。

其中实验________ 和________ (填实验序号)可以鉴别 和
和 ,实验现象分别是
,实验现象分别是________ 。
②热稳定性差异。乙组设计如下装置进行实验(加热及夹持装置省略)。
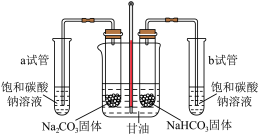
将分别装有 和
和 的试管同时放入甘油浴加热(甘油沸点为290℃)。该实验用饱和碳酸钠溶液检验反应的产物,b试管中的实验现象分别为:
的试管同时放入甘油浴加热(甘油沸点为290℃)。该实验用饱和碳酸钠溶液检验反应的产物,b试管中的实验现象分别为:___________ ,试管b中发生反应的化学方程式为___________ 。
Ⅱ.物质的量是学习化学的基础。
(5)14.4gCO和 的混合气体在标准状况下所占的体积为8.96L,其中CO的质量为
的混合气体在标准状况下所占的体积为8.96L,其中CO的质量为______ 。
(6)19g某二价金属的氯化物 中含有0.4molCl,金属A的相对原子质量是
中含有0.4molCl,金属A的相对原子质量是___________ 。
(7)根据反应 ,可知当有2.5molFeS2参加反应时,被氧化的硫元素的物质的量为
,可知当有2.5molFeS2参加反应时,被氧化的硫元素的物质的量为___________ mol。
I.金属及其化合物在生产生活中有着广泛的应用。
(1)胃舒平(主要成分为氢氧化铝)可用于治疗胃酸过多,氢氧化铝体现
(2)将Cu与稀硫酸混合,二者不能反应,滴入
 后,溶液很快变成蓝色,该反应的化学方程式为
后,溶液很快变成蓝色,该反应的化学方程式为(3)
 是一种酸式盐,写出
是一种酸式盐,写出 在水中的电离方程式:
在水中的电离方程式:(4)Na2CO3和NaHCO3是厨房中常见的两种盐,可用化学性质的差异进行鉴别。回答下列问题:
①与酸反应的差异。甲组进行了如下4组实验。

其中实验
 和
和 ,实验现象分别是
,实验现象分别是②热稳定性差异。乙组设计如下装置进行实验(加热及夹持装置省略)。

将分别装有
 和
和 的试管同时放入甘油浴加热(甘油沸点为290℃)。该实验用饱和碳酸钠溶液检验反应的产物,b试管中的实验现象分别为:
的试管同时放入甘油浴加热(甘油沸点为290℃)。该实验用饱和碳酸钠溶液检验反应的产物,b试管中的实验现象分别为:Ⅱ.物质的量是学习化学的基础。
(5)14.4gCO和
 的混合气体在标准状况下所占的体积为8.96L,其中CO的质量为
的混合气体在标准状况下所占的体积为8.96L,其中CO的质量为(6)19g某二价金属的氯化物
 中含有0.4molCl,金属A的相对原子质量是
中含有0.4molCl,金属A的相对原子质量是(7)根据反应
 ,可知当有2.5molFeS2参加反应时,被氧化的硫元素的物质的量为
,可知当有2.5molFeS2参加反应时,被氧化的硫元素的物质的量为
您最近一年使用:0次
5 . 某小组同学探究不同条件下氯气与二价锰化合物的反应。
资料:ⅰ、Mn2+在一定条件下被Cl2或ClO-氧化成MnO2(棕黑色)、MnO (绿色)、MnO
(绿色)、MnO (紫色)。
(紫色)。
ⅱ、浓碱条件下,MnO 可被OH-还原为MnO
可被OH-还原为MnO 。
。
ⅲ、Cl2的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
实验装置如图(夹持装置略):
(1)B中试剂是_____ 。
(2)通入Cl2前,实验Ⅱ、Ⅲ中沉淀由白色变为棕黑色的化学方程式为_____ 。
(3)对比实验Ⅰ、Ⅱ通入Cl2后的实验现象,对于二价锰化合物还原性的认识是_____ 。
(4)根据资料ⅱ,实验Ⅲ中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入Cl2导致溶液的碱性减弱。
原因二:可能是氧化剂过量,氧化剂将MnO 氧化为MnO
氧化为MnO 。
。
①用化学方程式表示可能导致溶液碱性减弱的原因:_____ ,但通过实验测定溶液的碱性变化很小。
②取实验Ⅲ中放置后的1mL悬浊液,加入4mL40%NaOH溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为_____ ,溶液绿色缓慢加深,原因是MnO2被_____ (填化学式)氧化,可证明实验Ⅲ的悬浊液中氧化剂过量。
③取实验Ⅱ中放置后的1mL悬浊液,加入4mL水,溶液紫色缓慢加深,发生反应的离子方程式是_____ 。
④从反应速率的角度,分析实验Ⅲ未得到绿色溶液的可能原因:_____ 。
资料:ⅰ、Mn2+在一定条件下被Cl2或ClO-氧化成MnO2(棕黑色)、MnO
 (绿色)、MnO
(绿色)、MnO (紫色)。
(紫色)。ⅱ、浓碱条件下,MnO
 可被OH-还原为MnO
可被OH-还原为MnO 。
。ⅲ、Cl2的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
实验装置如图(夹持装置略):
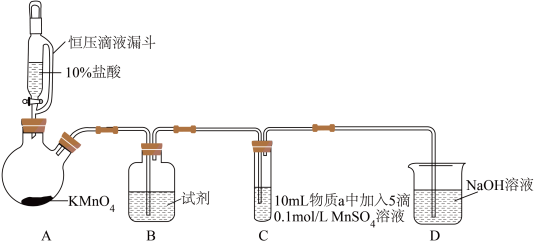
| 实验 | 物质a | C中实验现象 | |
| 通入Cl2前 | 通入Cl2后 | ||
| Ⅰ | 水 | 得到无色溶液 | 产生棕黑色沉淀,且放置后不发生变化 |
| Ⅱ | 5%NaOH溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
| Ⅲ | 40%NaOH溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
(2)通入Cl2前,实验Ⅱ、Ⅲ中沉淀由白色变为棕黑色的化学方程式为
(3)对比实验Ⅰ、Ⅱ通入Cl2后的实验现象,对于二价锰化合物还原性的认识是
(4)根据资料ⅱ,实验Ⅲ中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入Cl2导致溶液的碱性减弱。
原因二:可能是氧化剂过量,氧化剂将MnO
 氧化为MnO
氧化为MnO 。
。①用化学方程式表示可能导致溶液碱性减弱的原因:
②取实验Ⅲ中放置后的1mL悬浊液,加入4mL40%NaOH溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为
③取实验Ⅱ中放置后的1mL悬浊液,加入4mL水,溶液紫色缓慢加深,发生反应的离子方程式是
④从反应速率的角度,分析实验Ⅲ未得到绿色溶液的可能原因:
您最近一年使用:0次
2023-11-29更新
|
719次组卷
|
29卷引用:新疆乌鲁木齐市第101中学2022-2023学年高一上学期12月月考化学试题
新疆乌鲁木齐市第101中学2022-2023学年高一上学期12月月考化学试题(已下线)2022年北京市高考真题化学试题(部分试题)(已下线)考点53 化学实验方案设计与评价-备战2023年高考化学一轮复习考点帮(全国通用)四川省成都市树德中学2022-2023学年高三上学期入学考试理综化学试题2022年北京市高考真题化学试题(已下线)第28讲 定性、定量实验(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)2022年北京高考真题变式题1-14(已下线)易错点09 氯元素及其化合物-备战2023年高考化学考试易错题(已下线)专题三 离子反应-实战高考·二轮复习核心突破突破超重点 高效突破综合实验 实验4 创新探究实验角度1控制变量法探究(已下线)2022年北京高考真题化学试题变式题(实验探究题)(已下线)题型46 实验原理探究型综合实验(已下线)专题19 实验综合题(已下线)专题19 实验综合题(已下线)第18练 化学实验综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)考点09 氯及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第11讲 氯气和卤族元素(已下线)专题15 化学实验综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题14 化学实验综合题-2023年高考化学真题题源解密(全国通用)(已下线)考点14 氯及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点4 化学实验方案设计与探究 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)北京一零一中学2023-2024学年高三上学期11月统练五化学试题(已下线)微专题 物质性质综合实验探究北京市日坛中学2023-2024学年高三上学期10月检测化学试题北京师范大学第二附属中学2023-2024学年高三上学期期中考试化学试题江苏省苏州市工业园区星海实验高级中学2023-2024学年高一上学期12月调研化学试题山东省日照神州天立高级中学高复部2023-2024学年高三上学期12月份阶段性测试化学试题
名校
6 . 废旧锌锰电池中的黑锰粉含有 、
、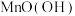 、
、 和少量
和少量 、
、 及炭黑等,为了保护环境、充分利用锰资源,通过如图流程制备
及炭黑等,为了保护环境、充分利用锰资源,通过如图流程制备 。
。
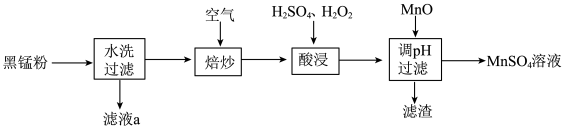
回答下列问题:
(1)“滤液a”的主要成分为 ,另外还含有少量
,另外还含有少量 等。
等。
①用离子方程式表示“滤液a“呈酸性的原因:______ 。
②根据如图所示的溶解度曲线,将“滤液a”______ 、洗涤、干燥,得 固体。
固体。

(2)“熔炒”的目的是除炭、氧化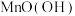 等。空气中
等。空气中 氧化
氧化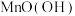 的化学方程式为
的化学方程式为______ 。
(3)探究“酸浸”中 溶解的适宜操作。
溶解的适宜操作。
实验Ⅰ.向 中加入
中加入 溶液,产生大量气泡;再加入稀
溶液,产生大量气泡;再加入稀 ,固体未明显溶解。
,固体未明显溶解。
实验Ⅱ.向 中加入稀
中加入稀 ,固体未溶解;再加入
,固体未溶解;再加入 溶液,产生大量气泡,固体完全溶解。
溶液,产生大量气泡,固体完全溶解。
实验Ⅰ中 的作用是
的作用是____ ,实验Ⅱ中 的作用是
的作用是______ 。
(4)证明 溶液中
溶液中 沉淀完全:取少量溶液,滴加
沉淀完全:取少量溶液,滴加______ (填试剂),观察到______ (填现象)。
 、
、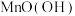 、
、 和少量
和少量 、
、 及炭黑等,为了保护环境、充分利用锰资源,通过如图流程制备
及炭黑等,为了保护环境、充分利用锰资源,通过如图流程制备 。
。
回答下列问题:
(1)“滤液a”的主要成分为
 ,另外还含有少量
,另外还含有少量 等。
等。①用离子方程式表示“滤液a“呈酸性的原因:
②根据如图所示的溶解度曲线,将“滤液a”
 固体。
固体。
(2)“熔炒”的目的是除炭、氧化
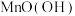 等。空气中
等。空气中 氧化
氧化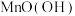 的化学方程式为
的化学方程式为(3)探究“酸浸”中
 溶解的适宜操作。
溶解的适宜操作。实验Ⅰ.向
 中加入
中加入 溶液,产生大量气泡;再加入稀
溶液,产生大量气泡;再加入稀 ,固体未明显溶解。
,固体未明显溶解。实验Ⅱ.向
 中加入稀
中加入稀 ,固体未溶解;再加入
,固体未溶解;再加入 溶液,产生大量气泡,固体完全溶解。
溶液,产生大量气泡,固体完全溶解。实验Ⅰ中
 的作用是
的作用是 的作用是
的作用是(4)证明
 溶液中
溶液中 沉淀完全:取少量溶液,滴加
沉淀完全:取少量溶液,滴加
您最近一年使用:0次
名校
解题方法
7 . 实验小组同学欲探究 的性质并测定空气中
的性质并测定空气中 的体积分数。他们设计了如图所示的实验装置,请你参与探究并回答问题。
的体积分数。他们设计了如图所示的实验装置,请你参与探究并回答问题。_______ 。
(2)装置E的作用是_______ 。(用离子方程式表示)
(3)装置D用于验证 的
的_______ 性,发生的化学方程式为_______ 。
(4)装置C中的现象是_______ ;若将C中的溴水改为酸性高锰酸钾溶液,现象为_______ ,发生的离子方程式为_______ 。
(5)如果用硫酸溶液和 固体反应制取
固体反应制取 装置如图所示。其中a导管的作用是
装置如图所示。其中a导管的作用是_______ 。 含量(假设空气中无其他还原性气体)。
含量(假设空气中无其他还原性气体)。

实验中若通过空气的体积为 (标准状况下),最终所得固体质量为0.466g,通过计算确定该空气中二氧化硫的含量是
(标准状况下),最终所得固体质量为0.466g,通过计算确定该空气中二氧化硫的含量是_______ 。(结果精确到0.001%)
 的性质并测定空气中
的性质并测定空气中 的体积分数。他们设计了如图所示的实验装置,请你参与探究并回答问题。
的体积分数。他们设计了如图所示的实验装置,请你参与探究并回答问题。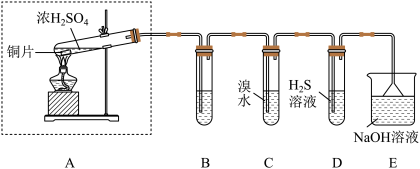
(2)装置E的作用是
(3)装置D用于验证
 的
的(4)装置C中的现象是
(5)如果用硫酸溶液和
 固体反应制取
固体反应制取 装置如图所示。其中a导管的作用是
装置如图所示。其中a导管的作用是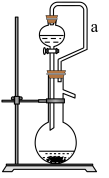
 含量(假设空气中无其他还原性气体)。
含量(假设空气中无其他还原性气体)。
实验中若通过空气的体积为
 (标准状况下),最终所得固体质量为0.466g,通过计算确定该空气中二氧化硫的含量是
(标准状况下),最终所得固体质量为0.466g,通过计算确定该空气中二氧化硫的含量是
您最近一年使用:0次
名校
解题方法
8 . 高铁酸钠( )是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为
)是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为
 。回答下列问题:
。回答下列问题:
(1)上述反应中的
_______ ,
_______ 。
(2)写出方程式,并用单线桥表示出电子转移方向_______ 。
(3)亚硝酸钠( )是一种工业盐,某化学兴趣小组设计实验探究
)是一种工业盐,某化学兴趣小组设计实验探究 的性质。请完善表格中的实验现象和结论(已知
的性质。请完善表格中的实验现象和结论(已知 遇淀粉变蓝)。
遇淀粉变蓝)。
通过上述实验可知, 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为_______ 。
 )是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为
)是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为
 。回答下列问题:
。回答下列问题:(1)上述反应中的


(2)写出方程式,并用单线桥表示出电子转移方向
(3)亚硝酸钠(
 )是一种工业盐,某化学兴趣小组设计实验探究
)是一种工业盐,某化学兴趣小组设计实验探究 的性质。请完善表格中的实验现象和结论(已知
的性质。请完善表格中的实验现象和结论(已知 遇淀粉变蓝)。
遇淀粉变蓝)。| 实验 | 实验操作及现象或结果 | 结论 |
| ① | 取5  溶液于试管中,加入少量 溶液于试管中,加入少量 溶液,充分反应后,再滴加淀粉溶液,溶液变蓝 溶液,充分反应后,再滴加淀粉溶液,溶液变蓝 |  具有 具有 |
| ② | 取2  溶液(先酸化好)于试管中,滴加足量的 溶液(先酸化好)于试管中,滴加足量的 溶液,可观察到的实验现象为 溶液,可观察到的实验现象为 |  具有还原性 具有还原性 |
| ③ |  固体与70%硫酸反应生成了 固体与70%硫酸反应生成了 和 和 两种气体 两种气体 |  具有 具有 |
 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为
您最近一年使用:0次
9 . 按照要求回答以下问题:
I.学兴趣小组按照如下流程进行“由镁铝合金制备硫酸铝晶体”的实验。
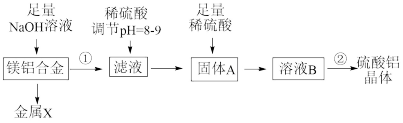
(1)请写出合金和足量的氢氧化钠溶液反应的离子方程式:_____ 。
II.A是一种红棕色金属氧化物,B、D是金属单质,J是一种难溶于水的白色化合物,受热后容易发生分解。
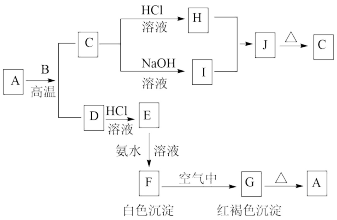
按要求写方程式:
(2)过程E→F→G的实验现象为_____ 。
(3)向E溶液中滴加过氧化氢溶液的离子方程式_____ 。
III.有一透明溶液,预确定是否含有下列离子:H+、Ca2+、K+、Cl-、SO 、HCO
、HCO 、MnO
、MnO 实验如下:
实验如下:
①用玻璃棒蘸取少量该溶液,点在pH试纸中部,试纸变为红色;
②取少量该溶液,加入过量BaCl2溶液,有白色沉淀生成;
③取②中反应后的上层清液,加入AgNO3溶液,有白色沉淀生成,且不溶于稀硝酸;
④取少量原溶液,加入FeSO4溶液,溶液变成棕黄色
回答下列问题:
(4)溶液中一定不存在的离子是_____ 。
(5)写出实验步骤④的离子方程式_____ 。
I.学兴趣小组按照如下流程进行“由镁铝合金制备硫酸铝晶体”的实验。

(1)请写出合金和足量的氢氧化钠溶液反应的离子方程式:
II.A是一种红棕色金属氧化物,B、D是金属单质,J是一种难溶于水的白色化合物,受热后容易发生分解。

按要求写方程式:
(2)过程E→F→G的实验现象为
(3)向E溶液中滴加过氧化氢溶液的离子方程式
III.有一透明溶液,预确定是否含有下列离子:H+、Ca2+、K+、Cl-、SO
 、HCO
、HCO 、MnO
、MnO 实验如下:
实验如下:①用玻璃棒蘸取少量该溶液,点在pH试纸中部,试纸变为红色;
②取少量该溶液,加入过量BaCl2溶液,有白色沉淀生成;
③取②中反应后的上层清液,加入AgNO3溶液,有白色沉淀生成,且不溶于稀硝酸;
④取少量原溶液,加入FeSO4溶液,溶液变成棕黄色
回答下列问题:
(4)溶液中一定不存在的离子是
(5)写出实验步骤④的离子方程式
您最近一年使用:0次
名校
解题方法
10 . 工业上以黄铁矿(主要成分为FeS2)为原料来制备硫酸,过程如下:
i.4FeS2+11O2 _______+8SO2
_______+8SO2
ii.2SO2+O2 2SO3
2SO3
iii.SO3+H2O=H2SO4
(1)补全过程i的方程式_______ 。
(2)硫酸工厂的烟气中含有SO2,工业上用NaOH溶液作吸收剂脱除烟气中的SO2。

①过程Ⅰ的化学方程式是_______ 。
②过程Ⅱ参加反应的物质A有_______ 。
③NaOH吸收SO2过程中常伴有少量SO42-,证明吸收液中含SO42-的方法是:取少量上层清液,_______ (填操作和现象)。
(3)测定烟气中SO2的含量。将V1 L烟气缓慢通过1L水(假设SO2完全被吸收,且溶液体积变化忽略不计),取20.00mL溶液,滴加2~3滴淀粉溶液,用c mol•L-1的碘水滴定,消耗碘水V2 mL。该烟气中SO2的含量为_______ mg•L-1。(已知:滴定反应为SO2+I2+2H2O=H2SO4+2HI)
i.4FeS2+11O2
 _______+8SO2
_______+8SO2ii.2SO2+O2
 2SO3
2SO3iii.SO3+H2O=H2SO4
(1)补全过程i的方程式
(2)硫酸工厂的烟气中含有SO2,工业上用NaOH溶液作吸收剂脱除烟气中的SO2。

①过程Ⅰ的化学方程式是
②过程Ⅱ参加反应的物质A有
③NaOH吸收SO2过程中常伴有少量SO42-,证明吸收液中含SO42-的方法是:取少量上层清液,
(3)测定烟气中SO2的含量。将V1 L烟气缓慢通过1L水(假设SO2完全被吸收,且溶液体积变化忽略不计),取20.00mL溶液,滴加2~3滴淀粉溶液,用c mol•L-1的碘水滴定,消耗碘水V2 mL。该烟气中SO2的含量为
您最近一年使用:0次
2022-07-07更新
|
184次组卷
|
3卷引用:新疆维吾尔自治区喀什地区喀什市第六中学2022-2023学年高二上学期10月期中考试化学试题



