解题方法
1 . 以菱锰矿(主要成分为MnCO3,还含有铁、镍的碳酸盐以及SiO2杂质)为原料生产次锰酸钠(Na3MnO4)的工艺流程如图:
(1)次锰酸钠中Mn的化合价为___________ ;滤渣1的主要成分为MnO2和___________ (填化学式)。
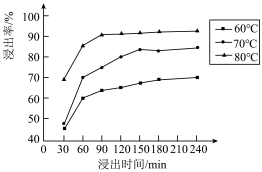
(2)锰的浸出率结果如图所示。由图可知,所采用的最佳实验条件为___________ 。___________ 。
(4)“除镍”步骤发生的反应为:MnS(s)+Ni2+(aq)=NiS(s)+Mn2+(aq)。反应的平衡常数K=___________ 。
(5)“母液1”中主要溶质的用途___________ 。
(6)煅烧产物MnO2在“共熔”过程中,反应得到Na2MnO4及一种单质气体,则该反应的化学方程式为___________ 。
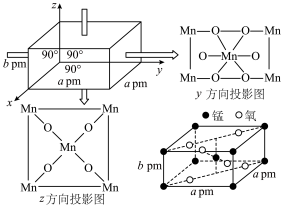
(7)某MnxO,四方晶胞结构及其投影如图所示,该晶胞由O2-和Mn3+构成。___________ ,Mn与Mn之间最近(顶点和体心)距离为___________ pm。(用含a、b的代数式表示)

| 物质 | MnS | NiS |
| Ksp | 2.0×10-13 | 1.0×10-21 |
(1)次锰酸钠中Mn的化合价为
(2)锰的浸出率结果如图所示。由图可知,所采用的最佳实验条件为
(4)“除镍”步骤发生的反应为:MnS(s)+Ni2+(aq)=NiS(s)+Mn2+(aq)。反应的平衡常数K=
(5)“母液1”中主要溶质的用途
(6)煅烧产物MnO2在“共熔”过程中,反应得到Na2MnO4及一种单质气体,则该反应的化学方程式为
(7)某MnxO,四方晶胞结构及其投影如图所示,该晶胞由O2-和Mn3+构成。
您最近半年使用:0次
解题方法
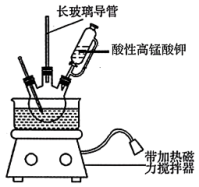
2 . 3,4-亚甲二氧基苯甲酸是一种用途广泛的有机合成中间体,微溶于水。实验室可用KMnO4氧化3,4-亚甲二氧基苯甲醛(油状液体)制备,实验装置如下图(夹持仪器已省略),其反应方程式为:
步骤1:向三颈烧瓶中加入3,4-亚甲二氧基苯甲醛11.2mL(约15.0g)和一定量水,缓慢开启搅拌器并加热。于70~80℃滴加稍过量的酸性KMnO4溶液,反应结束后,加入KOH溶液至碱性。
步骤2:趁热过滤,洗涤滤渣。合并滤液和洗涤液,向其中加入硫酸至水层不再产生沉淀。
步骤3:抽滤,洗涤,干燥,得3,4-亚甲二氧基苯甲酸固体12.2g。
回答下列问题:
(1)盛酸性KMnO4溶液的仪器的名称是___________ ;实验装置中长玻璃导管可用___________ 代替(填仪器名称)。
(2)反应结束后,加入KOH溶液前需向溶液中加入H2C2O4溶液在酸性条件下处理,发生反应的离子方程式为___________ 。
(3)步骤1中加入KOH溶液至碱性的目的是___________ 。
(4)步骤2中趁热过滤除去的物质是___________ (填化学式)。
(5)步骤3中检验产品是否洗净的操作为___________ 。
(6)写出步骤2中加入H2SO4发生的化学方程式___________ 。
(7)本实验3,4-亚甲二氧基苯甲酸的产率约为___________ %(保留两位小数)
3 +2KMnO4→2
+2KMnO4→2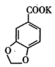 +
+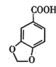 +2MnO2↓+H2O
+2MnO2↓+H2O
步骤1:向三颈烧瓶中加入3,4-亚甲二氧基苯甲醛11.2mL(约15.0g)和一定量水,缓慢开启搅拌器并加热。于70~80℃滴加稍过量的酸性KMnO4溶液,反应结束后,加入KOH溶液至碱性。
步骤2:趁热过滤,洗涤滤渣。合并滤液和洗涤液,向其中加入硫酸至水层不再产生沉淀。
步骤3:抽滤,洗涤,干燥,得3,4-亚甲二氧基苯甲酸固体12.2g。
回答下列问题:
(1)盛酸性KMnO4溶液的仪器的名称是
(2)反应结束后,加入KOH溶液前需向溶液中加入H2C2O4溶液在酸性条件下处理,发生反应的离子方程式为
(3)步骤1中加入KOH溶液至碱性的目的是
(4)步骤2中趁热过滤除去的物质是
(5)步骤3中检验产品是否洗净的操作为
(6)写出步骤2中加入H2SO4发生的化学方程式
(7)本实验3,4-亚甲二氧基苯甲酸的产率约为
您最近半年使用:0次
3 . 利用含钴废料(主要成分为Co、Ni、Mn、Pb以及 、
、 等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示:
等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示:
(1)基态Co原子的价电子原子轨道表达式为_______ 。铂钴合金具有较高的永磁性能,其晶胞如图所示,若A点Pt原子的坐标参数为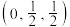 ,则B点Pt原子的坐标参数为
,则B点Pt原子的坐标参数为______ 。_______ 。“酸浸”时 发生反应的总离子方程式为
发生反应的总离子方程式为_______ 。
(3)酸浸后滤渣的主要成分为______ 。
(4)“沉锰”时, 转化为
转化为 ,则“沉锰”时发生反应的离子方程式为:
,则“沉锰”时发生反应的离子方程式为:_______ 。
(5)可以通过电解 溶液获得单质Co和较浓的盐酸,其工作原理如图所示:
溶液获得单质Co和较浓的盐酸,其工作原理如图所示:______ (填“膜a”或者“膜b”)。阴极的电极方程式为:_______ 。
 、
、 等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示:
等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示: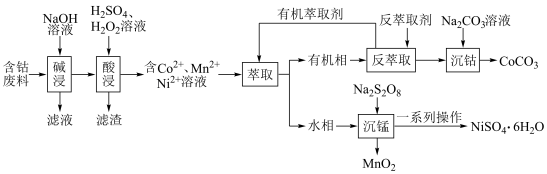
(1)基态Co原子的价电子原子轨道表达式为
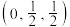 ,则B点Pt原子的坐标参数为
,则B点Pt原子的坐标参数为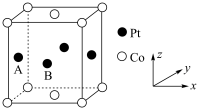
 发生反应的总离子方程式为
发生反应的总离子方程式为(3)酸浸后滤渣的主要成分为
(4)“沉锰”时,
 转化为
转化为 ,则“沉锰”时发生反应的离子方程式为:
,则“沉锰”时发生反应的离子方程式为:(5)可以通过电解
 溶液获得单质Co和较浓的盐酸,其工作原理如图所示:
溶液获得单质Co和较浓的盐酸,其工作原理如图所示: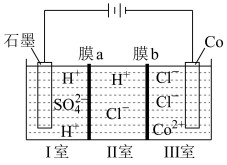
您最近半年使用:0次
4 . 金属钨是重要的战略资源,由黑钨矿(主要成分为 、
、 ,含有少量Si、As的化合物)制取金属钨的流程如图所示:
,含有少量Si、As的化合物)制取金属钨的流程如图所示:
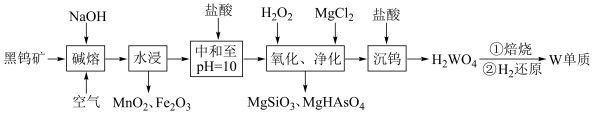
已知:常温下钨酸( )难溶于水,酸性很弱,其钠盐易溶于水。
)难溶于水,酸性很弱,其钠盐易溶于水。
回答下列问题:
(1)已知元素周期表中74号元素钨与铬同族,钨在元素周期表中的位置是第六周期第________ 族。 中铁元素的化合价为
中铁元素的化合价为________ 。
(2)“碱熔”步骤中为提高反应速率,可以将黑钨矿预先________ ,“碱熔”过程 发生反应的化学方程式为
发生反应的化学方程式为________ 。
(3)上述流程中加盐酸中和至pH=10时,溶液中的杂质阴离子有 、
、 、
、 等,则“氧化、净化”过程中,先加入
等,则“氧化、净化”过程中,先加入 发生反应的离子方程式为
发生反应的离子方程式为________ 。
(4)沉钨过程中,判断 是否沉淀完全的方法是
是否沉淀完全的方法是________ 。
(5)钨酸钙( )和氢氧化钙都是微溶电解质。某温度下
)和氢氧化钙都是微溶电解质。某温度下 和
和 的饱和溶液中,
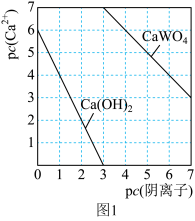
的饱和溶液中,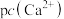 与pc(阴离子)的关系如图1所示,已知:pc(离子)=-lgc(离子)。该温度下将
与pc(阴离子)的关系如图1所示,已知:pc(离子)=-lgc(离子)。该温度下将 溶液加入石灰乳中得到大量钨酸钙,该反应的平衡常数K=
溶液加入石灰乳中得到大量钨酸钙,该反应的平衡常数K=________ 。
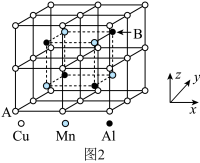
(6)合金具有比金属单质更优越的性能,Cu-Mn-Al合金为磁性形状记忆合金材料之一,其晶胞结构如图2所示。该合金的化学式为________ 。若A原子的坐标参数为(0,0,0),则B原子的坐标参数为________ 。
 、
、 ,含有少量Si、As的化合物)制取金属钨的流程如图所示:
,含有少量Si、As的化合物)制取金属钨的流程如图所示:
已知:常温下钨酸(
 )难溶于水,酸性很弱,其钠盐易溶于水。
)难溶于水,酸性很弱,其钠盐易溶于水。回答下列问题:
(1)已知元素周期表中74号元素钨与铬同族,钨在元素周期表中的位置是第六周期第
 中铁元素的化合价为
中铁元素的化合价为(2)“碱熔”步骤中为提高反应速率,可以将黑钨矿预先
 发生反应的化学方程式为
发生反应的化学方程式为(3)上述流程中加盐酸中和至pH=10时,溶液中的杂质阴离子有
 、
、 、
、 等,则“氧化、净化”过程中,先加入
等,则“氧化、净化”过程中,先加入 发生反应的离子方程式为
发生反应的离子方程式为(4)沉钨过程中,判断
 是否沉淀完全的方法是
是否沉淀完全的方法是(5)钨酸钙(
 )和氢氧化钙都是微溶电解质。某温度下
)和氢氧化钙都是微溶电解质。某温度下 和
和 的饱和溶液中,
的饱和溶液中, 与pc(阴离子)的关系如图1所示,已知:pc(离子)=-lgc(离子)。该温度下将
与pc(阴离子)的关系如图1所示,已知:pc(离子)=-lgc(离子)。该温度下将 溶液加入石灰乳中得到大量钨酸钙,该反应的平衡常数K=
溶液加入石灰乳中得到大量钨酸钙,该反应的平衡常数K=
(6)合金具有比金属单质更优越的性能,Cu-Mn-Al合金为磁性形状记忆合金材料之一,其晶胞结构如图2所示。该合金的化学式为

您最近半年使用:0次
5 . 连二硫酸锰(MnS2O6,其中Mn为+2价)是一种常用的果蔬保鲜剂,易溶于水,室温下其水溶液在pH为2.8~3.5时最稳定。回答下列问题:
Ⅰ.制备连二硫酸锰(MnS2O6)
某化学小组利用MnO2悬浊液吸收SO2气体制取连二硫酸锰的装置(部分夹持、加热仪器已省略)如图所示。
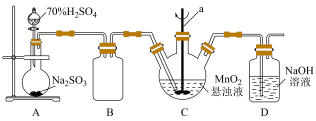
(1)仪器a的名称为________ ,装置B的作用是________ 。
(2)装置C中的反应温度需要控制在0℃左右,控制温度的方法是_______ 。实验时需要向C中通入稍过量的SO2,目的是________ 。
(3)装置C中反应生成等物质的量的MnS2O6和MnSO4,则反应的化学方程式为_______ ,判断反应完成的现象是_______ ,待反应结束后经除杂、减压蒸发浓缩、结晶可得产品MnS2O6•nH2O。
Ⅱ.测定产品中Mn的质量分数
称取ag产品充分加热使其分解为MnSO4,然后加水溶解,用cmol•L-1的KMnO4溶液进行滴定(Mn元素均转化为MnO2)。
(4)滴定时,发生反应的离子方程式为_______ ;若滴定消耗KMnO4溶液的体积为VmL,则产品中Mn的质量分数为_______ 。
(5)下列操作会使得测定结果偏大的是_______ 。
Ⅰ.制备连二硫酸锰(MnS2O6)
某化学小组利用MnO2悬浊液吸收SO2气体制取连二硫酸锰的装置(部分夹持、加热仪器已省略)如图所示。

(1)仪器a的名称为
(2)装置C中的反应温度需要控制在0℃左右,控制温度的方法是
(3)装置C中反应生成等物质的量的MnS2O6和MnSO4,则反应的化学方程式为
Ⅱ.测定产品中Mn的质量分数
称取ag产品充分加热使其分解为MnSO4,然后加水溶解,用cmol•L-1的KMnO4溶液进行滴定(Mn元素均转化为MnO2)。
(4)滴定时,发生反应的离子方程式为
(5)下列操作会使得测定结果偏大的是
| A.滴定前锥形瓶用蒸馏水洗后未用待测MnSO4溶液润洗 |
| B.滴定前平视读数,滴定结束俯视读数 |
| C.滴定前滴定管中尖嘴处有气泡,滴定后气泡消失 |
| D.对连二硫酸锰产品进行加热操作时加热不充分 |
您最近半年使用:0次
6 . 按要求写出下列反应的离子方程式:
(1)碳酸氢钠溶液与稀盐酸混合:______________ 。
(2)少量二氧化碳通入澄清石灰水中:______________ 。
(3)氧化钠与稀盐酸反应:______________ 。
(4)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液呈中性:______________ 。
(5)配平下列离子方程式:
①Fe3++SO2+H2O=Fe2++ +H+
+H+____________________ ;
② +
+ +H+=CO2↑+Mn2++H2O
+H+=CO2↑+Mn2++H2O____________________ 。
(1)碳酸氢钠溶液与稀盐酸混合:
(2)少量二氧化碳通入澄清石灰水中:
(3)氧化钠与稀盐酸反应:
(4)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液呈中性:
(5)配平下列离子方程式:
①Fe3++SO2+H2O=Fe2++
 +H+
+H+②
 +
+ +H+=CO2↑+Mn2++H2O
+H+=CO2↑+Mn2++H2O
您最近半年使用:0次
7 . Ⅷ族元素铁及其化合物性质多样,大多发生氧化还原反应.
(1)高铁酸钠( )是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾强,其本身在反应中被还原为
)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾强,其本身在反应中被还原为 .请配平如下制取高铁酸钠的化学方程式.
.请配平如下制取高铁酸钠的化学方程式._______
______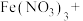 ______NaOH+______
______NaOH+______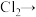 _____
_____ _____
_____ _____NaCl+_____
_____NaCl+_____
(2)在如图所示的装置中,用NaOH溶液、铁粉、稀 等试剂制备氢氧化亚铁.
等试剂制备氢氧化亚铁.
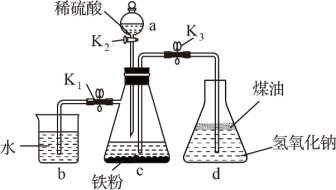
①仪器a的名称是______ .
②关闭 ,打开
,打开 和
和 ,向仪器c中加入适量稀硫酸,关闭
,向仪器c中加入适量稀硫酸,关闭 ,写出装置c中发生反应的离子方程式
,写出装置c中发生反应的离子方程式____________ .同时c中有气体产生,该气体的作用是______ .
③当仪器b中产生均匀气泡后的操作是______ .写出仪器c、d中可能出现的实验现象______ .
(3)已知 .向2支试管中各加入5 mL
.向2支试管中各加入5 mL 
 溶液,若直接通入
溶液,若直接通入 至饱和,1小时后,溶液逐渐变为浅绿色;若先滴加2滴浓盐酸,再通入
至饱和,1小时后,溶液逐渐变为浅绿色;若先滴加2滴浓盐酸,再通入 至饱和,几分钟后,溶液由黄色变为浅绿色.由此可知:促使该氧化还原反应快速发生,可采取的措施是
至饱和,几分钟后,溶液由黄色变为浅绿色.由此可知:促使该氧化还原反应快速发生,可采取的措施是______ .
(1)高铁酸钠(
 )是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾强,其本身在反应中被还原为
)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾强,其本身在反应中被还原为 .请配平如下制取高铁酸钠的化学方程式.
.请配平如下制取高铁酸钠的化学方程式.______
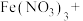 ______NaOH+______
______NaOH+______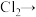 _____
_____ _____
_____ _____NaCl+_____
_____NaCl+_____
(2)在如图所示的装置中,用NaOH溶液、铁粉、稀
 等试剂制备氢氧化亚铁.
等试剂制备氢氧化亚铁.
①仪器a的名称是
②关闭
 ,打开
,打开 和
和 ,向仪器c中加入适量稀硫酸,关闭
,向仪器c中加入适量稀硫酸,关闭 ,写出装置c中发生反应的离子方程式
,写出装置c中发生反应的离子方程式③当仪器b中产生均匀气泡后的操作是
(3)已知
 .向2支试管中各加入5 mL
.向2支试管中各加入5 mL 
 溶液,若直接通入
溶液,若直接通入 至饱和,1小时后,溶液逐渐变为浅绿色;若先滴加2滴浓盐酸,再通入
至饱和,1小时后,溶液逐渐变为浅绿色;若先滴加2滴浓盐酸,再通入 至饱和,几分钟后,溶液由黄色变为浅绿色.由此可知:促使该氧化还原反应快速发生,可采取的措施是
至饱和,几分钟后,溶液由黄色变为浅绿色.由此可知:促使该氧化还原反应快速发生,可采取的措施是
您最近半年使用:0次
名校
解题方法
8 . I.某化学自主实验小组利用如图所示装置探究 能否被
能否被 还原
还原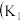 、
、 为止水夹,夹持固定装置略去)。
为止水夹,夹持固定装置略去)。________ 。 装置发生的化学反应方程式为
装置发生的化学反应方程式为_________ 。
(2)甲、乙分别是___________  填标号
填标号 。
。
a.硫酸、浓硫酸 b.碱石灰、无水氯化钙 c.碱石灰、碱石灰 d.五氧化二磷、五氧化二磷
(3)若 能够被
能够被 还原,写出发生反应的化学方程式:
还原,写出发生反应的化学方程式:___________ 。
(4)此实验装置存在一个明显的缺陷是___________ 。
II.硫酸可用于生产化肥、农药、炸药、染料和盐类等。工业生产硫酸的流程图如下: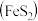 为原料来制备SO2,将黄铁矿粉碎的原因是:
为原料来制备SO2,将黄铁矿粉碎的原因是:___________ 。
(6)写出催化反应室中SO2被氧化为SO3的化学方程式___________ 。
(7)硫酸工业的尾气中含有少量SO2,若直接排放会污染空气,并导致硫酸型酸雨,可用___________ 吸收。
 能否被
能否被 还原
还原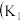 、
、 为止水夹,夹持固定装置略去)。
为止水夹,夹持固定装置略去)。
 装置发生的化学反应方程式为
装置发生的化学反应方程式为(2)甲、乙分别是
 填标号
填标号 。
。a.硫酸、浓硫酸 b.碱石灰、无水氯化钙 c.碱石灰、碱石灰 d.五氧化二磷、五氧化二磷
(3)若
 能够被
能够被 还原,写出发生反应的化学方程式:
还原,写出发生反应的化学方程式:(4)此实验装置存在一个明显的缺陷是
II.硫酸可用于生产化肥、农药、炸药、染料和盐类等。工业生产硫酸的流程图如下:
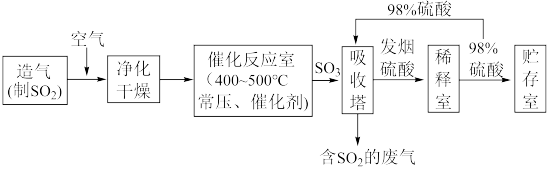
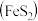 为原料来制备SO2,将黄铁矿粉碎的原因是:
为原料来制备SO2,将黄铁矿粉碎的原因是:(6)写出催化反应室中SO2被氧化为SO3的化学方程式
(7)硫酸工业的尾气中含有少量SO2,若直接排放会污染空气,并导致硫酸型酸雨,可用
您最近半年使用:0次
2024-02-24更新
|
636次组卷
|
2卷引用:新疆克孜勒苏柯尔克孜自治州第二中学2022-2023学年高一下学期期末考试化学试题
9 . 氧化还原反应在工农业生产、日常生活中具有广泛用途,贯穿古今。
(1)工业盐的主要成分是 ,以前有许多起因误食
,以前有许多起因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力,这说明
结合的能力,这说明 具有
具有_______ (填“氧化”或“还原”,下同)。工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有________ 性。
(2) 常用于焊接,在焊接铜器时可用
常用于焊接,在焊接铜器时可用 除去铜器表面的氧化铜,便于焊接,其反应如下:
除去铜器表面的氧化铜,便于焊接,其反应如下: 。
。
①配平上述氧化还原反应方程式___________ 。
②该反应中,氧化剂是___________ (填化学式),被氧化的元素是___________ (填元素名称)。
(3)二氧化氯是一种高效消毒剂。工业上制备 的反应为:
的反应为: 。
。
①该反应中的还原产物是___________ (写化学式),反应中每生成1mol 分子,被氧化的HCl的物质的量为
分子,被氧化的HCl的物质的量为___________ ,转移电子的数目为___________ 。
②用“单线桥”标出反应中电子转移的方向与数目___________ 。
③ 在杀菌消毒的过程中会生成副产物亚氯酸盐(
在杀菌消毒的过程中会生成副产物亚氯酸盐( ),要将其转化为
),要将其转化为 除去,下列试剂能实现其转化过程的是
除去,下列试剂能实现其转化过程的是___________ (填字母)。
a. b.
b. c.
c. d.
d.
(4)双氯水是公认的绿色氧化剂。已知氯化性强弱顺序为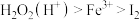 ,向
,向 溶液中加入足量硫酸酸化的双氧水,发生反应的离子方程式为
溶液中加入足量硫酸酸化的双氧水,发生反应的离子方程式为___________ 。
(1)工业盐的主要成分是
 ,以前有许多起因误食
,以前有许多起因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力,这说明
结合的能力,这说明 具有
具有(2)
 常用于焊接,在焊接铜器时可用
常用于焊接,在焊接铜器时可用 除去铜器表面的氧化铜,便于焊接,其反应如下:
除去铜器表面的氧化铜,便于焊接,其反应如下: 。
。①配平上述氧化还原反应方程式
②该反应中,氧化剂是
(3)二氧化氯是一种高效消毒剂。工业上制备
 的反应为:
的反应为: 。
。①该反应中的还原产物是
 分子,被氧化的HCl的物质的量为
分子,被氧化的HCl的物质的量为②用“单线桥”标出反应中电子转移的方向与数目
③
 在杀菌消毒的过程中会生成副产物亚氯酸盐(
在杀菌消毒的过程中会生成副产物亚氯酸盐( ),要将其转化为
),要将其转化为 除去,下列试剂能实现其转化过程的是
除去,下列试剂能实现其转化过程的是a.
 b.
b. c.
c. d.
d.
(4)双氯水是公认的绿色氧化剂。已知氯化性强弱顺序为
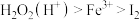 ,向
,向 溶液中加入足量硫酸酸化的双氧水,发生反应的离子方程式为
溶液中加入足量硫酸酸化的双氧水,发生反应的离子方程式为
您最近半年使用:0次
名校
10 . 工业上用生物法处理H2S的原理如下:
反应1:H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
反应2:4Fe2SO4+2H2SO4+O2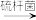 2Fe(SO4)3+2H2O
2Fe(SO4)3+2H2O
以硫杆菌作催化剂时,反应温度及溶液pH对Fe2+氧化速率的影响分别如图1、图2所示,下列说法不正确的是

反应1:H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
反应2:4Fe2SO4+2H2SO4+O2
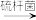 2Fe(SO4)3+2H2O
2Fe(SO4)3+2H2O以硫杆菌作催化剂时,反应温度及溶液pH对Fe2+氧化速率的影响分别如图1、图2所示,下列说法不正确的是

| A.上述总反应方程式为:2H2S+O2=2S↓+2H2O,Fe2(SO4)3是该反应的催化剂 |
| B.当反应温度过高时,Fe2+氧化速率下降的原因可能是硫杆菌失去活性 |
| C.由图-1、图-2可得出结论:使用硫杆菌作催化剂的最佳条件为30℃、pH=2.0 |
| D.当反应1中转移0.1mol电子时,反应1中消耗的H2S在标准状况下的体积为2.24L |
您最近半年使用:0次
2024-02-14更新
|
135次组卷
|
2卷引用:新疆乌鲁木齐市第十一中学2023-2024学年高一上学期1月期末化学试题



