解题方法
1 . 过氧乙酸( )是无色透明液体,常用于速效漂白和消毒,氧化性比
)是无色透明液体,常用于速效漂白和消毒,氧化性比 强,与酸性
强,与酸性 相近。某课外实验小组同学用
相近。某课外实验小组同学用 溶液与乙酸酐制备高浓度过氧乙酸并对其含量测定,实验过程如下。
溶液与乙酸酐制备高浓度过氧乙酸并对其含量测定,实验过程如下。
 。
。Ⅰ.过氧化氢的浓缩:
 溶液浓缩至75%(
溶液浓缩至75%( 沸点150.2℃):浓缩装置如下图所示(连接用橡胶管和支持仪器以及抽气泵已省略):
沸点150.2℃):浓缩装置如下图所示(连接用橡胶管和支持仪器以及抽气泵已省略):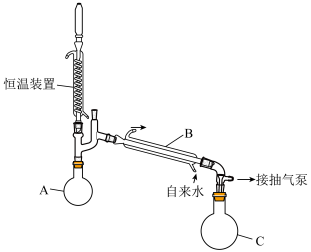
 溶液主要在
溶液主要在(2)该实验过程操作的正确顺序是
_______→_______→_______→_______→③→④
①水浴加热;②连接装置;③抽真空后向冷凝管中通水;
④自滴液漏斗往烧瓶中缓慢滴加
 溶液;
溶液;⑤在滴液漏斗中装入
 溶液;
溶液;⑥检查装置气密性。
Ⅱ.过氧乙酸的制备:如下图所示,搅拌器不断搅拌下,向三颈烧瓶中加入45mL乙酸酐,逐步滴加
 溶液25mL(过量),再加1mL浓硫酸,搅拌4小时,室温静置15小时即得47%的过氧乙酸溶液。
溶液25mL(过量),再加1mL浓硫酸,搅拌4小时,室温静置15小时即得47%的过氧乙酸溶液。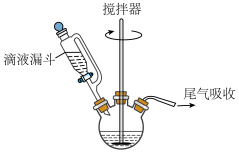
(4)实验中,利用搅拌器充分搅拌的作用是
(5)乙酸酐与
 反应的尾气可以用
反应的尾气可以用Ⅲ.过氧乙酸(含杂质)的含量测定:取适量样品按下图所示步骤依次进行实验,测定过氧乙酸的含量。

 溶液恰好除尽
溶液恰好除尽 的实验现象是
的实验现象是②第3步中过氧乙酸可被
 还原为乙酸,其离子方程式为
还原为乙酸,其离子方程式为③若实验中所取样品体积为
 ,第3步中加入
,第3步中加入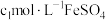 溶液
溶液 ,第4步滴定中消耗
,第4步滴定中消耗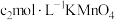 溶液
溶液 ,则过氧乙酸含量为
,则过氧乙酸含量为 。
。
您最近半年使用:0次
2 . 钢渣是钢铁行业的固体废弃物,含有2CaO·SiO2、Fe2O3、FeO、Al2O3和V2O3等物质。一种以钢渣粉为原料固定CO2并制备V2O3的工艺流程如图所示。
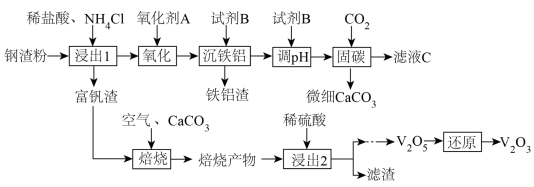
已知钢渣中Ca元素质量分数为30%。V2O3在稀盐酸和NH4Cl混合溶液中不易被浸出。该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH如下表所示:
回答下列问题:
(1)浸出1过程生成的SiO2“包裹”在钢渣表面形成固体膜,阻碍反应物向钢渣扩散。提高浸出率的措施有_______ (除粉碎外,举1例)。该浸出过程不使用稀硫酸代替稀盐酸的原因是_______ 。
(2)为避免引入杂质离子,氧化剂A应为_______ (举1例)。
(3)滤液C的溶质可循环利用,试剂B应为_______ 。
(4)若钢渣粉中含有钒酸钙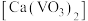 ,加入Na2CO3溶液能够使钒酸钙溶解,是因为存在平衡:
,加入Na2CO3溶液能够使钒酸钙溶解,是因为存在平衡: 。已知
。已知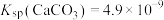 ,
,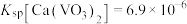 ,则该平衡常数
,则该平衡常数
_______ (结果保留2位有效数字)。
(5)富钒渣焙烧可生成钒钙盐,不同钒钙盐的溶解率随pH变化如图所示。已知浸出2的pH约为2.5,则应控制焙烧条件使该钒钙盐为_______ 。该培烧反应的化学方程式是_______ 。

(6)若Ca的浸出率为90%,理论上1吨钢渣在“固碳”中可固定_______ kgCO2。

已知钢渣中Ca元素质量分数为30%。V2O3在稀盐酸和NH4Cl混合溶液中不易被浸出。该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH如下表所示:
| 金属离子 | Fe3+ | Fe2+ | Al3+ | Ca2+ |
| 开始沉淀的pH | 1.9 | 7.2 | 3.5 | 12.4 |
| 沉淀完全的pH | 2.9 | 8.2 | 5.1 | 13.8 |
(1)浸出1过程生成的SiO2“包裹”在钢渣表面形成固体膜,阻碍反应物向钢渣扩散。提高浸出率的措施有
(2)为避免引入杂质离子,氧化剂A应为
(3)滤液C的溶质可循环利用,试剂B应为
(4)若钢渣粉中含有钒酸钙
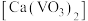 ,加入Na2CO3溶液能够使钒酸钙溶解,是因为存在平衡:
,加入Na2CO3溶液能够使钒酸钙溶解,是因为存在平衡: 。已知
。已知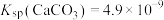 ,
,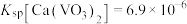 ,则该平衡常数
,则该平衡常数
(5)富钒渣焙烧可生成钒钙盐,不同钒钙盐的溶解率随pH变化如图所示。已知浸出2的pH约为2.5,则应控制焙烧条件使该钒钙盐为

(6)若Ca的浸出率为90%,理论上1吨钢渣在“固碳”中可固定
您最近半年使用:0次
名校
解题方法
3 . 水中溶解的氧气高温下对锅炉有很强的腐蚀性,可以用联氨(N2H4)处理锅炉水中的溶解氧。其中一种反应机理如图所示。下列说法错误的是

| A.联氨(N2H4)易溶于水,所得溶液中存在四种氢键 |
| B.稳定性:H2O2<N2H4,是因为H2O2分子中孤电子对较多 |
C.①中发生的反应为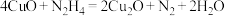 |
D.该过程中产生的氮气和消耗的氧气之比为: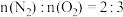 |
您最近半年使用:0次
2024-04-05更新
|
155次组卷
|
2卷引用:宁夏银川市贺兰县第一中学2023-2024学年高二下学期第一阶段考试化学试卷
解题方法
4 . 某湿法炼锌的萃余液中含有 、
、 、
、 、
、 、
、 、
、 及30~60
及30~60
 等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图:
等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图:
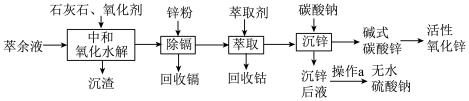
已知:
回答下列问题:
(1)“中和氧化水解”时,先加入适量的石灰石调节溶液的pH为1.0;加入一定量的 ;再加入石灰石调节溶液的pH为4.0。
;再加入石灰石调节溶液的pH为4.0。
①“氧化”时, 转化为
转化为 除去,反应的离子方程式为
除去,反应的离子方程式为________ ,为提高反应速率可采取的措施_______ (举1例)。
②“沉渣”的主要成分除 、
、 外还有
外还有______ 。
③“氧化”时,若加入过量的 ,钴元素将会进入“沉渣”中,则氧化水解后的溶液中含钴微粒浓度为
,钴元素将会进入“沉渣”中,则氧化水解后的溶液中含钴微粒浓度为______  。
。
(2)“除镉”时,主要反应的离子方程式为________ 。
(3)“沉锌”时,在近中性条件下加入 可得碱式碳酸锌[
可得碱式碳酸锌[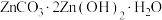 ]固体,同时产生大量的气体。
]固体,同时产生大量的气体。
①产生大量气体的原因是________ 。
②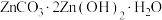 需洗涤,检验是否洗净的试剂是
需洗涤,检验是否洗净的试剂是________ 。
(4)不同质量分数的 溶液在不同温度下析出
溶液在不同温度下析出 晶体的物种如图所示。欲从含20%
晶体的物种如图所示。欲从含20%  及微量杂质的“沉锌后液”中直接析出无水
及微量杂质的“沉锌后液”中直接析出无水 ,“操作a”步骤为
,“操作a”步骤为________ 。

 、
、 、
、 、
、 、
、 、
、 及30~60
及30~60
 等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图:
等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图:
已知:
| 沉淀物 |  |  |  |  | 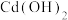 |
 | 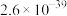 |  | 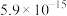 |  | 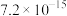 |
(1)“中和氧化水解”时,先加入适量的石灰石调节溶液的pH为1.0;加入一定量的
 ;再加入石灰石调节溶液的pH为4.0。
;再加入石灰石调节溶液的pH为4.0。①“氧化”时,
 转化为
转化为 除去,反应的离子方程式为
除去,反应的离子方程式为②“沉渣”的主要成分除
 、
、 外还有
外还有③“氧化”时,若加入过量的
 ,钴元素将会进入“沉渣”中,则氧化水解后的溶液中含钴微粒浓度为
,钴元素将会进入“沉渣”中,则氧化水解后的溶液中含钴微粒浓度为 。
。(2)“除镉”时,主要反应的离子方程式为
(3)“沉锌”时,在近中性条件下加入
 可得碱式碳酸锌[
可得碱式碳酸锌[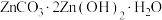 ]固体,同时产生大量的气体。
]固体,同时产生大量的气体。①产生大量气体的原因是
②
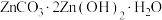 需洗涤,检验是否洗净的试剂是
需洗涤,检验是否洗净的试剂是(4)不同质量分数的
 溶液在不同温度下析出
溶液在不同温度下析出 晶体的物种如图所示。欲从含20%
晶体的物种如图所示。欲从含20%  及微量杂质的“沉锌后液”中直接析出无水
及微量杂质的“沉锌后液”中直接析出无水 ,“操作a”步骤为
,“操作a”步骤为
您最近半年使用:0次
名校
解题方法
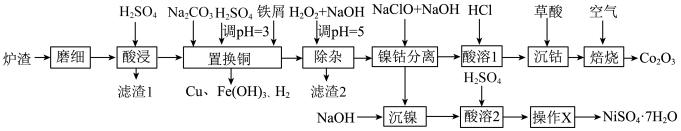
5 . 酸浸法回收废炉渣中(主要为铜、钴、镍、铁等金属元素的氧化物)的铜、钴、镍的流程如下:
已知:25℃时,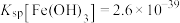 ,
, 。
。
(1)“磨细”过程的目的是_______ 。
(2)酸浸液中大量铁元素以 存在,加入
存在,加入 可减少铁屑的消耗从而降低成本,
可减少铁屑的消耗从而降低成本, 与
与 反应过程中会产生气泡,其离子方程式为
反应过程中会产生气泡,其离子方程式为_______ 。
(3)“滤渣2”主要成分为_______ (填化学式)。
(4)“镍钴分离”过程 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(5)“酸溶1”过程用 替换
替换 ,从绿色化学角度分析其可行性
,从绿色化学角度分析其可行性_______ 。
(6)“焙烧”过程发生反应的化学方程式为_______ 。
(7)已知当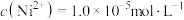 时,认为其沉淀完全。“沉镍”过程的目的是为了将“
时,认为其沉淀完全。“沉镍”过程的目的是为了将“ ”,此时应调节溶液的pH为
”,此时应调节溶液的pH为_______ 。
(8)“操作X”为_______ 。

已知:25℃时,
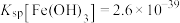 ,
, 。
。(1)“磨细”过程的目的是
(2)酸浸液中大量铁元素以
 存在,加入
存在,加入 可减少铁屑的消耗从而降低成本,
可减少铁屑的消耗从而降低成本, 与
与 反应过程中会产生气泡,其离子方程式为
反应过程中会产生气泡,其离子方程式为(3)“滤渣2”主要成分为
(4)“镍钴分离”过程
 发生反应的离子方程式为
发生反应的离子方程式为(5)“酸溶1”过程用
 替换
替换 ,从绿色化学角度分析其可行性
,从绿色化学角度分析其可行性(6)“焙烧”过程发生反应的化学方程式为
(7)已知当
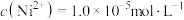 时,认为其沉淀完全。“沉镍”过程的目的是为了将“
时,认为其沉淀完全。“沉镍”过程的目的是为了将“ ”,此时应调节溶液的pH为
”,此时应调节溶液的pH为(8)“操作X”为
您最近半年使用:0次
2024-03-17更新
|
410次组卷
|
2卷引用:宁夏石嘴山市第三中学2024届高三第一次模拟考试理综-化学试题
名校
6 . 2023年10月26日11时14分,神舟十七号载人飞船在酒泉卫星发射中心点火发射。飞船返回地球时,为了减弱返回舱着陆的速度,反推发动机的燃料是高氯酸铵 和铝粉混合物。请回答与高氮酸铵和铝粉相关元素的问题:
和铝粉混合物。请回答与高氮酸铵和铝粉相关元素的问题:
(1)二氧化氯 和过氧化氢均有强氧化性。
和过氧化氢均有强氧化性。
①Cl和O分别形成简单氢化物的稳定性比较_______ >_______
②在酸性条件下,由 和双氧水反应制备
和双氧水反应制备 ,其反应的离子方程式为
,其反应的离子方程式为_______ ;该反应中还原剂与氧化剂的物质的量之比为_______ 。
(2)高氯酸铵中铵根离子的电子式为_______ ;高氯酸铵和铝粉中的元素所形成的简单离子中,核外电子数相同、半径由小到大的顺序是_______ (用离子符号表示)。
(3)氮元素的非金属性较强,N2分子的性质比较稳定,其原因是_______ 。
(4)高氯酸铵和铝粉反应除了生成 和N2外,还有另外两种不含氮元素的物质生成,请写出其化学方程式
和N2外,还有另外两种不含氮元素的物质生成,请写出其化学方程式_______ 。
 和铝粉混合物。请回答与高氮酸铵和铝粉相关元素的问题:
和铝粉混合物。请回答与高氮酸铵和铝粉相关元素的问题:(1)二氧化氯
 和过氧化氢均有强氧化性。
和过氧化氢均有强氧化性。①Cl和O分别形成简单氢化物的稳定性比较
②在酸性条件下,由
 和双氧水反应制备
和双氧水反应制备 ,其反应的离子方程式为
,其反应的离子方程式为(2)高氯酸铵中铵根离子的电子式为
(3)氮元素的非金属性较强,N2分子的性质比较稳定,其原因是
(4)高氯酸铵和铝粉反应除了生成
 和N2外,还有另外两种不含氮元素的物质生成,请写出其化学方程式
和N2外,还有另外两种不含氮元素的物质生成,请写出其化学方程式
您最近半年使用:0次
名校
7 . 硫代硫酸钠( )俗称大苏打,广泛用于定影、媒染等领域,临床上用于氰化物解毒。实验室中以
)俗称大苏打,广泛用于定影、媒染等领域,临床上用于氰化物解毒。实验室中以 和
和 为主要原料制备
为主要原料制备 。回答下列问题:
。回答下列问题:
(1) 能解毒氰化物的原理为
能解毒氰化物的原理为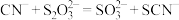 ,为检验该反应产生了
,为检验该反应产生了 ,最佳方法是取少量反应液,先向其中加入足量的盐酸,再加入
,最佳方法是取少量反应液,先向其中加入足量的盐酸,再加入___________ (填化学式),观察到的现象是___________ 。
(2)工业级硫化钠中混有杂质(重金属硫化物、煤粉等),需进行纯化。纯化实验装置如图1,保持水浴沸腾,回流一段时间后,过滤,将滤液冷却至室温后析出高纯硫化钠。
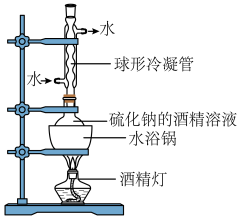
图1
将工业硫化钠溶于酒精并加热时,采取水浴加热优点是___________ 。
(3)利用图2装置制备 。
。
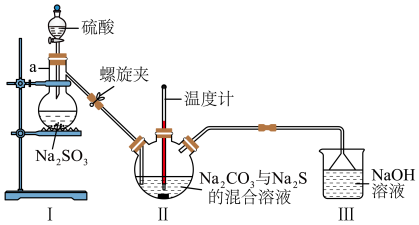
图2
①仪器a的名称为___________ 。
②实验开始时,打开螺旋夹并适当调节螺旋夹,一方面可以防止倒吸,另一方面可以___________ 。
③装置Ⅱ处发生反应的总化学方程式为___________ ,停止通入 前要控制Ⅱ装置中溶液pH约为7而不能小于7的理由是
前要控制Ⅱ装置中溶液pH约为7而不能小于7的理由是___________ 。
④装置 Ⅲ 的作用是___________ 。
(4)实验结束后,经过一系列操作得到粗产品,测定粗产品中 (
( )的质量分数。精确称取0.5g硫代硫酸钠样品,用少量水溶解后滴入1~2滴淀粉溶液,再注入缓冲溶液。用
)的质量分数。精确称取0.5g硫代硫酸钠样品,用少量水溶解后滴入1~2滴淀粉溶液,再注入缓冲溶液。用 的
的 标准溶液滴定,待指示剂颜色变化稳定后停止滴定,测得消耗
标准溶液滴定,待指示剂颜色变化稳定后停止滴定,测得消耗 标准溶液的体积为VmL。(已知
标准溶液的体积为VmL。(已知 )
)
①滴定达到终点时的现象是___________ 。
②产品中 的质量分数为
的质量分数为___________ %。
 )俗称大苏打,广泛用于定影、媒染等领域,临床上用于氰化物解毒。实验室中以
)俗称大苏打,广泛用于定影、媒染等领域,临床上用于氰化物解毒。实验室中以 和
和 为主要原料制备
为主要原料制备 。回答下列问题:
。回答下列问题:(1)
 能解毒氰化物的原理为
能解毒氰化物的原理为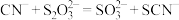 ,为检验该反应产生了
,为检验该反应产生了 ,最佳方法是取少量反应液,先向其中加入足量的盐酸,再加入
,最佳方法是取少量反应液,先向其中加入足量的盐酸,再加入(2)工业级硫化钠中混有杂质(重金属硫化物、煤粉等),需进行纯化。纯化实验装置如图1,保持水浴沸腾,回流一段时间后,过滤,将滤液冷却至室温后析出高纯硫化钠。

图1
将工业硫化钠溶于酒精并加热时,采取水浴加热优点是
(3)利用图2装置制备
 。
。
图2
①仪器a的名称为
②实验开始时,打开螺旋夹并适当调节螺旋夹,一方面可以防止倒吸,另一方面可以
③装置Ⅱ处发生反应的总化学方程式为
 前要控制Ⅱ装置中溶液pH约为7而不能小于7的理由是
前要控制Ⅱ装置中溶液pH约为7而不能小于7的理由是④装置 Ⅲ 的作用是
(4)实验结束后,经过一系列操作得到粗产品,测定粗产品中
 (
( )的质量分数。精确称取0.5g硫代硫酸钠样品,用少量水溶解后滴入1~2滴淀粉溶液,再注入缓冲溶液。用
)的质量分数。精确称取0.5g硫代硫酸钠样品,用少量水溶解后滴入1~2滴淀粉溶液,再注入缓冲溶液。用 的
的 标准溶液滴定,待指示剂颜色变化稳定后停止滴定,测得消耗
标准溶液滴定,待指示剂颜色变化稳定后停止滴定,测得消耗 标准溶液的体积为VmL。(已知
标准溶液的体积为VmL。(已知 )
)①滴定达到终点时的现象是
②产品中
 的质量分数为
的质量分数为
您最近半年使用:0次
2024-02-13更新
|
93次组卷
|
2卷引用:宁夏银川市育才中学2023-2024学年高三上学期1月期末理科综合化学试题
名校
8 . 钯(Pd)是一种贵金属,性质类似铂(Pt)。活性炭载钯催化剂广泛应用于石油化工、制药等工业,但使用过程中因生成难溶于酸的PdO而失活。一种从废钯催化剂(杂质主要含有机物、活性炭、及少量Fe、Cu、Al等元素)中回收海绵钯的工艺流程如图:

已知:
Ⅰ.阴、阳离子交换树脂的基本工作原理分别为 、
、 (
( 表示树脂的有机成分)。
表示树脂的有机成分)。
Ⅱ.“沉钯”时得到氯钯酸铵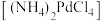 固体,不溶于冷水,可溶于稀盐酸。
固体,不溶于冷水,可溶于稀盐酸。
(1)温度、固液比对浸取率的影响如图,则“浸取”的最佳条件为___________ 。
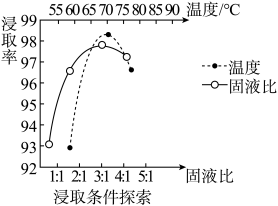
(2)“浸取”时,加入试剂A的目的为___________ 。
(3)“浸取”时,加入 有利于Pd的溶解,生成的四氯合钯(Ⅱ)酸(
有利于Pd的溶解,生成的四氯合钯(Ⅱ)酸( )为二元强酸。加入浓盐酸和
)为二元强酸。加入浓盐酸和 后主要反应的离子方程式:
后主要反应的离子方程式:___________ 。
(4)“离子交换除杂”应使用___________ (填“阳离子”或“阴离子”)树脂,“洗脱”时应使用的洗脱液为___________ (填标号)。
A.硫酸 B.盐酸 C.无水乙醇
(5)“还原”过程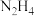 转化为
转化为 ,在反应器出口处器壁内侧有白色晶体生成,该过程还产生的副产物为
,在反应器出口处器壁内侧有白色晶体生成,该过程还产生的副产物为___________ ,且该产物可循环利用至___________ 环节(填环节名称)。

已知:
Ⅰ.阴、阳离子交换树脂的基本工作原理分别为
 、
、 (
( 表示树脂的有机成分)。
表示树脂的有机成分)。Ⅱ.“沉钯”时得到氯钯酸铵
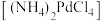 固体,不溶于冷水,可溶于稀盐酸。
固体,不溶于冷水,可溶于稀盐酸。(1)温度、固液比对浸取率的影响如图,则“浸取”的最佳条件为

(2)“浸取”时,加入试剂A的目的为
(3)“浸取”时,加入
 有利于Pd的溶解,生成的四氯合钯(Ⅱ)酸(
有利于Pd的溶解,生成的四氯合钯(Ⅱ)酸( )为二元强酸。加入浓盐酸和
)为二元强酸。加入浓盐酸和 后主要反应的离子方程式:
后主要反应的离子方程式:(4)“离子交换除杂”应使用
A.硫酸 B.盐酸 C.无水乙醇
(5)“还原”过程
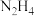 转化为
转化为 ,在反应器出口处器壁内侧有白色晶体生成,该过程还产生的副产物为
,在反应器出口处器壁内侧有白色晶体生成,该过程还产生的副产物为
您最近半年使用:0次
名校
解题方法
9 . 某种电镀污泥主要含有碲化亚铜(Cu2Te)、三氧化二铬(Cr2O3)以及少量的金(Au),可以用于制取Na2Cr2O7溶液、金属铜和粗碲等,以实现有害废料的资源化利用,工艺流程如下:

已知:煅烧时,Cu2Te发生的反应为Cu2Te+2O2 2CuO+TeO2。
2CuO+TeO2。
(1)为提高酸浸速率,可采用的措施是__________ 。
(2)煅烧时,Cr2O3发生反应的化学方程式为______ 。
(3)浸出液中除了含有TeOSO4(在电解过程中不反应)外,还可能含有________ (写化学式)。
(4)在实际的含铬废水处理中,还可采用直接沉淀的方法,处理成本较低。已知含铬酸性废水中存在着CrO 和Cr2O
和Cr2O 相互转化的平衡,请用离子方程式表示它们之间的转化反应
相互转化的平衡,请用离子方程式表示它们之间的转化反应________ 。
(5)测定某固体产品中Na2Cr2O7含量的方法如下:称取产品试样2.50g配成250mL溶液,用移液管取出25.00mL于锥形瓶中,加入足量稀硫酸酸化后,再加入几滴指示剂,用0.1000mol·L-1硫酸亚铁铵(NH4)2Fe(SO4)2标准液进行滴定,重复进行二次实验。
①氧化还原滴定过程中的离子方程式为_______ 。
②滴定到达终点的现象是________ 。
③若三次实验消耗(NH4)2Fe(SO4)2标准液的平均体积为25.00mL,则所得产品中Na2Cr2O7的纯度为_______ %。[已知M(Na2Cr2O7)=262g·mol-1,计算结果保留三位有效数字]

已知:煅烧时,Cu2Te发生的反应为Cu2Te+2O2
 2CuO+TeO2。
2CuO+TeO2。(1)为提高酸浸速率,可采用的措施是
(2)煅烧时,Cr2O3发生反应的化学方程式为
(3)浸出液中除了含有TeOSO4(在电解过程中不反应)外,还可能含有
(4)在实际的含铬废水处理中,还可采用直接沉淀的方法,处理成本较低。已知含铬酸性废水中存在着CrO
 和Cr2O
和Cr2O 相互转化的平衡,请用离子方程式表示它们之间的转化反应
相互转化的平衡,请用离子方程式表示它们之间的转化反应(5)测定某固体产品中Na2Cr2O7含量的方法如下:称取产品试样2.50g配成250mL溶液,用移液管取出25.00mL于锥形瓶中,加入足量稀硫酸酸化后,再加入几滴指示剂,用0.1000mol·L-1硫酸亚铁铵(NH4)2Fe(SO4)2标准液进行滴定,重复进行二次实验。
①氧化还原滴定过程中的离子方程式为
②滴定到达终点的现象是
③若三次实验消耗(NH4)2Fe(SO4)2标准液的平均体积为25.00mL,则所得产品中Na2Cr2O7的纯度为
您最近半年使用:0次
名校
解题方法
10 . 废弃电池是一种有害垃圾,合理处理则能变废为宝。下图是废弃锌锰电池的处理流程图:
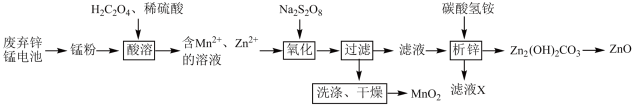
已知:锰粉的主要成分是Mn元素的+2、+3、+4价氧化物和ZnO。
回答下列问题:
(1)“废弃锌锰电池→锰粉”的操作是拆分、煅烧,煅烧类似于实验室中的焙烧,实验室焙烧使用的仪器名称是___________ 。
(2)“酸溶”采用锰粉比锰块的浸取速率快,为提高“酸溶”的浸取速率,还可以采取的措施有___________ (任写两条),
(3)“酸溶” 过程中H2C2O4与Mn元素+4价氧化物反应的离子方程式___________ ,“氧化”操作的氧化产物是___________ (填化学式)。
(4)“洗涤、干燥”时,检验MnO2洗涤干净的实验方法及现象是___________ 。
(5)滤液X可以用于制取化肥,其中除Na+外,主要含___________ 、 (填离子符号)。
(填离子符号)。
(6)由Zn2(OH)2CO3制备ZnO的条件是加热,写出该反应的化学方程式:___________ 。

已知:锰粉的主要成分是Mn元素的+2、+3、+4价氧化物和ZnO。
回答下列问题:
(1)“废弃锌锰电池→锰粉”的操作是拆分、煅烧,煅烧类似于实验室中的焙烧,实验室焙烧使用的仪器名称是
(2)“酸溶”采用锰粉比锰块的浸取速率快,为提高“酸溶”的浸取速率,还可以采取的措施有
(3)“酸溶” 过程中H2C2O4与Mn元素+4价氧化物反应的离子方程式
(4)“洗涤、干燥”时,检验MnO2洗涤干净的实验方法及现象是
(5)滤液X可以用于制取化肥,其中除Na+外,主要含
 (填离子符号)。
(填离子符号)。(6)由Zn2(OH)2CO3制备ZnO的条件是加热,写出该反应的化学方程式:
您最近半年使用:0次



