名校
1 . 三氧化二铬 是一种绿色固体,常作颜料。以它为原料实现如下转化:
是一种绿色固体,常作颜料。以它为原料实现如下转化:
②沉淀E溶于浓的强碱。
③在二价锰盐中,除少数 、
、 难溶与水外,其余大部分易溶于水。
难溶与水外,其余大部分易溶于水。
(1)写出溶液B中的所有阳离子__________ 。写出步骤Ⅱ中生成气体C的离子方程式__________ 。沉淀E的化学式为__________ 。
(2)下列说法正确的是__________。
(3)在碱性条件下, 具有强还原剂,可被
具有强还原剂,可被 氧化为最高价,写出两者恰好反应的离子方程式
氧化为最高价,写出两者恰好反应的离子方程式__________ 。根据该反应原理,设计实验检验上述反应后溶液中生成的阴离子__________ 。
 是一种绿色固体,常作颜料。以它为原料实现如下转化:
是一种绿色固体,常作颜料。以它为原料实现如下转化: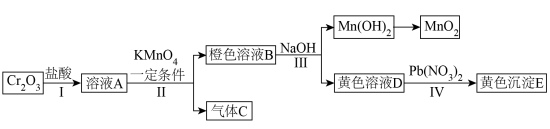
②沉淀E溶于浓的强碱。
③在二价锰盐中,除少数
 、
、 难溶与水外,其余大部分易溶于水。
难溶与水外,其余大部分易溶于水。(1)写出溶液B中的所有阳离子
(2)下列说法正确的是__________。
| A.气体C在工业上可通过电解法制备 |
| B.在溶液B中加入乙醇,溶液变为绿色,再变为蓝色 |
| C.将步骤Ⅰ中的盐酸换成硫酸,仅影响步骤Ⅱ的反应 |
| D.在步骤Ⅲ中,溶液B加入纯碱溶液,也能分离出锰元素 |
(3)在碱性条件下,
 具有强还原剂,可被
具有强还原剂,可被 氧化为最高价,写出两者恰好反应的离子方程式
氧化为最高价,写出两者恰好反应的离子方程式
您最近半年使用:0次
名校
2 . 电镀废水中常含有阴离子A,排放前可加 溶液处理,使之转化为沉淀B。取一定质量沉淀B按如图流程进行实验:
溶液处理,使之转化为沉淀B。取一定质量沉淀B按如图流程进行实验:
(1)组成B的三种元素为______ ,黑色固体E的化学式为______ 。
(2)气体F的结构式______ ,阴离子A的电子式______
(3)沉淀B隔绝空气加热分解的化学方程式是______
(4)固体C在沸腾的稀盐酸中会生成一种弱酸和一种白色沉淀,该白色沉淀是共价化合物(测其分子量为99.5),则反应的化学方程式是______ 。
 溶液处理,使之转化为沉淀B。取一定质量沉淀B按如图流程进行实验:
溶液处理,使之转化为沉淀B。取一定质量沉淀B按如图流程进行实验: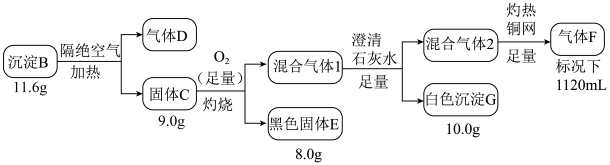
(1)组成B的三种元素为
(2)气体F的结构式
(3)沉淀B隔绝空气加热分解的化学方程式是
(4)固体C在沸腾的稀盐酸中会生成一种弱酸和一种白色沉淀,该白色沉淀是共价化合物(测其分子量为99.5),则反应的化学方程式是
您最近半年使用:0次
名校
解题方法
3 . 高铁酸钾( )是一种新型绿色消毒剂,
)是一种新型绿色消毒剂, 为紫色固体,微溶于KOH溶液,在酸性或中性溶液中快速产生
为紫色固体,微溶于KOH溶液,在酸性或中性溶液中快速产生 ,在碱性溶液中较稳定。实验室中制备
,在碱性溶液中较稳定。实验室中制备 的装置如图所示,下列说法不正确的是
的装置如图所示,下列说法不正确的是
 )是一种新型绿色消毒剂,
)是一种新型绿色消毒剂, 为紫色固体,微溶于KOH溶液,在酸性或中性溶液中快速产生
为紫色固体,微溶于KOH溶液,在酸性或中性溶液中快速产生 ,在碱性溶液中较稳定。实验室中制备
,在碱性溶液中较稳定。实验室中制备 的装置如图所示,下列说法不正确的是
的装置如图所示,下列说法不正确的是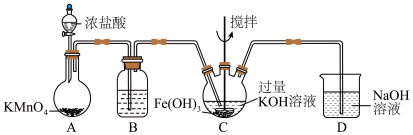
| A.该制备实验需在通风橱中进行 |
| B.装置B的作用是吸收HCl气体 |
C.C中制备 反应方程式为: 反应方程式为: |
D.取C中紫色溶液加入稀硫酸后,经检验溶液中含有 ,说明 ,说明 被 被 还原 还原 |
您最近半年使用:0次
4 . 下列化学反应与方程式相符的是
A.氢氧化钠溶液中加入过量草酸: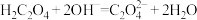 |
B.碱性条件下,氢氧化铁与次氯酸钠溶液反应制备高铁酸钠 : :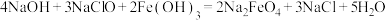 |
C.工业制取高纯硅: |
D.尿素与甲醛反应生成某线型脲醛树脂: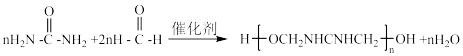 |
您最近半年使用:0次
解题方法
5 . 一种制备 的工艺路线如图所示,反应②所得溶液
的工艺路线如图所示,反应②所得溶液 在3~4之间,反应③需及时补充
在3~4之间,反应③需及时补充 以保持反应在
以保持反应在 条件下进行。
条件下进行。 的电离平衡常数
的电离平衡常数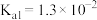 ,
,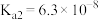 。请回答:
。请回答:
(1)溶液①中阴离子浓度大小(用“>”表示):___________ 。
(2)下列说法正确的是___________。
(3)写出反应③的化学方程式:___________ 。
(4)“低温真空蒸发”可防止 被氧化。请设计实验证明
被氧化。请设计实验证明 是否被氧化
是否被氧化___________ 。若 部分被氧化,为不降低
部分被氧化,为不降低 的产率,补充
的产率,补充 的量应适当
的量应适当___________ (填“增加”“减少”或“不变”)。
 的工艺路线如图所示,反应②所得溶液
的工艺路线如图所示,反应②所得溶液 在3~4之间,反应③需及时补充
在3~4之间,反应③需及时补充 以保持反应在
以保持反应在 条件下进行。
条件下进行。
 的电离平衡常数
的电离平衡常数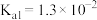 ,
,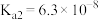 。请回答:
。请回答:(1)溶液①中阴离子浓度大小(用“>”表示):
(2)下列说法正确的是___________。
| A.反应①、②和③均为氧化还原反应 |
| B.气体①和②是造成酸雨的主要成分 |
| C.往反应①后的溶液中加水可得到硫酸铜溶液 |
| D.溶液Y可循环用于反应②进行吸收气体① |
(3)写出反应③的化学方程式:
(4)“低温真空蒸发”可防止
 被氧化。请设计实验证明
被氧化。请设计实验证明 是否被氧化
是否被氧化 部分被氧化,为不降低
部分被氧化,为不降低 的产率,补充
的产率,补充 的量应适当
的量应适当
您最近半年使用:0次
2024-04-21更新
|
116次组卷
|
2卷引用:浙江省金华市十校2023-2024学年高三下学期4月模拟考试化学试题
6 . 某固态化合物Y的组成为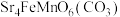 ,以Y为原料可实现如下转化:
,以Y为原料可实现如下转化: 均不能形成配合物。请回答:
均不能形成配合物。请回答:
(1)写出溶液C中的所有阳离子____________ 。
(2)步骤V中的反应为 ,请说明
,请说明 能够较完全转化为
能够较完全转化为 的两个原因是:①生成
的两个原因是:①生成 降低了体系的能量;②
降低了体系的能量;②____________ 。
(3)下列说法正确的是____________。
(4)固体Y可与 溶液反应,写出该反应的离子方程式
溶液反应,写出该反应的离子方程式____________ 。
(5)设计实验方案检验气体中除 以外的两种主要成分
以外的两种主要成分____________ 。
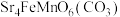 ,以Y为原料可实现如下转化:
,以Y为原料可实现如下转化: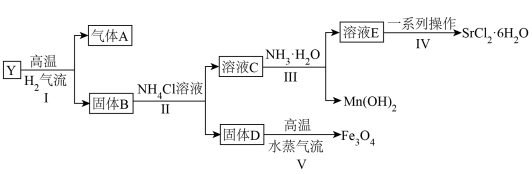
 均不能形成配合物。请回答:
均不能形成配合物。请回答:(1)写出溶液C中的所有阳离子
(2)步骤V中的反应为
 ,请说明
,请说明 能够较完全转化为
能够较完全转化为 的两个原因是:①生成
的两个原因是:①生成 降低了体系的能量;②
降低了体系的能量;②(3)下列说法正确的是____________。
A.固体B中含有 单质 单质 |
B.步骤Ⅱ反应促进了 水解平衡正向移动 水解平衡正向移动 |
C.步骤Ⅲ可推断碱性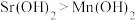 |
D.直接加热 不能得到 不能得到 |
(4)固体Y可与
 溶液反应,写出该反应的离子方程式
溶液反应,写出该反应的离子方程式(5)设计实验方案检验气体中除
 以外的两种主要成分
以外的两种主要成分
您最近半年使用:0次
7 . 半水煤气(含有 、
、 、
、 、
、 ,以及少量的
,以及少量的 、
、 和
和 )经提纯后可获得工业合成氨所需的
)经提纯后可获得工业合成氨所需的 和
和 混合气。过程如下:
混合气。过程如下:
 。
。
② 与
与 反应的方程式为:
反应的方程式为: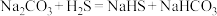 。
。
③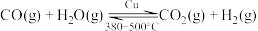
 。请回答:
。请回答:
(1)半水煤气通过___________ 溶液(填化学式)可证明有 气体。
气体。
(2)在“催化转化炉”的后半段补充通入 作“冷激气”,原因是
作“冷激气”,原因是___________ 。
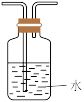
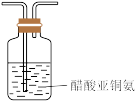
(3)已知:高压下 极易溶于水;用醋酸亚铜氨溶液(易被氧化)溶液可吸收
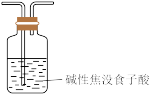
极易溶于水;用醋酸亚铜氨溶液(易被氧化)溶液可吸收 ,碱性焦没食子酸溶液(易受酸性气体影响)可吸收
,碱性焦没食子酸溶液(易受酸性气体影响)可吸收 。“精制过程”需除去混合气体中的
。“精制过程”需除去混合气体中的 、
、 、
、 和
和 ,请排序
,请排序___________ : ___________ ___________
___________ ___________
___________ ___________。
___________。
(4)通过测定“催化转化炉”进出口气体中 体积分数以确定
体积分数以确定 转化率。取标况下
转化率。取标况下 进口或出口气体,经历的实验过程以及反应前后每个装置的质量变化(
进口或出口气体,经历的实验过程以及反应前后每个装置的质量变化(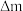 )如下:
)如下:___________
② 体积分数为
体积分数为___________ (用含 及
及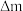 的式子表示,忽略空气影响)。
的式子表示,忽略空气影响)。
(5)下列说法正确的是___________
 、
、 、
、 、
、 ,以及少量的
,以及少量的 、
、 和
和 )经提纯后可获得工业合成氨所需的
)经提纯后可获得工业合成氨所需的 和
和 混合气。过程如下:
混合气。过程如下:

 。
。②
 与
与 反应的方程式为:
反应的方程式为: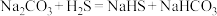 。
。③
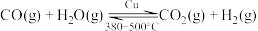
 。请回答:
。请回答:(1)半水煤气通过
 气体。
气体。(2)在“催化转化炉”的后半段补充通入
 作“冷激气”,原因是
作“冷激气”,原因是(3)已知:高压下
 极易溶于水;用醋酸亚铜氨溶液(易被氧化)溶液可吸收
极易溶于水;用醋酸亚铜氨溶液(易被氧化)溶液可吸收 ,碱性焦没食子酸溶液(易受酸性气体影响)可吸收
,碱性焦没食子酸溶液(易受酸性气体影响)可吸收 。“精制过程”需除去混合气体中的
。“精制过程”需除去混合气体中的 、
、 、
、 和
和 ,请排序
,请排序 ___________
___________ ___________
___________ ___________。
___________。
|
|
|
|
| (a) | (b) | (c) | (d) |
(4)通过测定“催化转化炉”进出口气体中
 体积分数以确定
体积分数以确定 转化率。取标况下
转化率。取标况下 进口或出口气体,经历的实验过程以及反应前后每个装置的质量变化(
进口或出口气体,经历的实验过程以及反应前后每个装置的质量变化(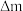 )如下:
)如下:
②
 体积分数为
体积分数为 及
及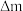 的式子表示,忽略空气影响)。
的式子表示,忽略空气影响)。(5)下列说法正确的是___________
A.“煤气发生炉”应先通 后通 后通 |
B.采用饱和 溶液吸收 溶液吸收 会造成管道堵塞 会造成管道堵塞 |
C.吸收塔内放置空心瓷环可提高 的吸收率 的吸收率 |
D.半水煤气中的 会导致 会导致 催化剂失效 催化剂失效 |
您最近半年使用:0次
2024-04-19更新
|
111次组卷
|
2卷引用:浙江省金华市十校2023-2024学年高三下学期4月模拟考试化学试题
名校
解题方法
8 . 砷的化合物可用于半导体领域,如我国“天宫”空间站的核心舱“天和号”就是采用砷化镓薄膜电池来供电。一种从酸性高浓度含砷废水[砷主要以亚砷酸( )形式存在]中回收砷的工艺流程如下:
)形式存在]中回收砷的工艺流程如下:
Ⅱ.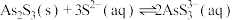
Ⅲ.砷酸( )在酸性条件下有强氧化性
)在酸性条件下有强氧化性
Ⅳ.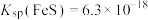 ,
,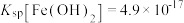
请回答:
(1)从含砷废水到滤液Ⅰ,浓度明显减小的阳离子为__________ (用离子符号表示)。
(2)下列说法正确的是__________。
(3)“沉砷”过程中 是否可用过量的
是否可用过量的 替换
替换__________ (填“是”或“否”);请从平衡移动的角度解释原因__________ 。
(4)砷酸“还原”过程中发生的化学方程式为__________ 。还原后溶液需检验是否仍剩余砷酸,设计检验实验方案__________ 。
 )形式存在]中回收砷的工艺流程如下:
)形式存在]中回收砷的工艺流程如下:

Ⅱ.
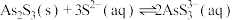
Ⅲ.砷酸(
 )在酸性条件下有强氧化性
)在酸性条件下有强氧化性Ⅳ.
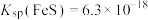 ,
,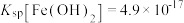
请回答:
(1)从含砷废水到滤液Ⅰ,浓度明显减小的阳离子为
(2)下列说法正确的是__________。
A.沉砷时产生的废气可用 溶液吸收处理 溶液吸收处理 |
B.酸化的目的是增加 价砷的氧化性 价砷的氧化性 |
C. 浸取后所得滤渣的主要成分是 浸取后所得滤渣的主要成分是 ,不含 ,不含 |
D.酸性: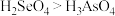 |
(3)“沉砷”过程中
 是否可用过量的
是否可用过量的 替换
替换(4)砷酸“还原”过程中发生的化学方程式为
您最近半年使用:0次
解题方法
9 .  是重要的化工原料,可发生如下转化:
是重要的化工原料,可发生如下转化: ,可得到氮肥硫酸铵,写出该反应的化学方程式
,可得到氮肥硫酸铵,写出该反应的化学方程式______ 。
(2)氨气可经途径II的多步反应制得硝酸,下列有关说法正确的是______。
(3)醋酸(熔点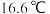 )、硝酸(熔点
)、硝酸(熔点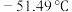 )这两种相对分子质量相近的分子熔沸点相差较大的主要原因是
)这两种相对分子质量相近的分子熔沸点相差较大的主要原因是______ 。
(4) 与
与 性质相似,写出足量
性质相似,写出足量 与稀硫酸反应所得产物的化学式
与稀硫酸反应所得产物的化学式______ 。
(5)途径 中
中 过量,用离子方程式解释途径
过量,用离子方程式解释途径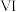 中溶液颜色变化的原因
中溶液颜色变化的原因______ 。
(6) 可与
可与 反应得到化合物
反应得到化合物 和一种无机盐,设计实验验证产物中分离出的化合物
和一种无机盐,设计实验验证产物中分离出的化合物 中含有氮元素
中含有氮元素______ 。
 是重要的化工原料,可发生如下转化:
是重要的化工原料,可发生如下转化: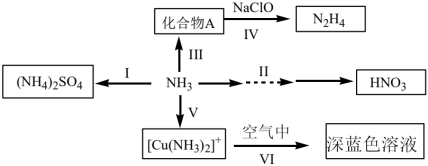
①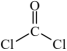
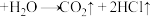 ;②
;② (无色)容易被空气氧化
(无色)容易被空气氧化
 ,可得到氮肥硫酸铵,写出该反应的化学方程式
,可得到氮肥硫酸铵,写出该反应的化学方程式(2)氨气可经途径II的多步反应制得硝酸,下列有关说法正确的是______。
A.工业生产得到的浓硝酸,常因溶解了 而略显黄色 而略显黄色 |
B.氨气先经过催化氧化得到 , , 再与水反应生成硝酸 再与水反应生成硝酸 |
C.浓硝酸与甘油在一定条件下反应生成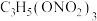 ,该反应为酯化反应 ,该反应为酯化反应 |
| D.工业上常用铁罐车或铝罐车运送浓硝酸,是因为常温下它们和浓硝酸不反应 |
(3)醋酸(熔点
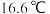 )、硝酸(熔点
)、硝酸(熔点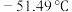 )这两种相对分子质量相近的分子熔沸点相差较大的主要原因是
)这两种相对分子质量相近的分子熔沸点相差较大的主要原因是(4)
 与
与 性质相似,写出足量
性质相似,写出足量 与稀硫酸反应所得产物的化学式
与稀硫酸反应所得产物的化学式(5)途径
 中
中 过量,用离子方程式解释途径
过量,用离子方程式解释途径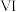 中溶液颜色变化的原因
中溶液颜色变化的原因(6)
 可与
可与 反应得到化合物
反应得到化合物 和一种无机盐,设计实验验证产物中分离出的化合物
和一种无机盐,设计实验验证产物中分离出的化合物 中含有氮元素
中含有氮元素
您最近半年使用:0次
10 . 古代青铜器的出土,体现了古代中国对人类物质文明的巨大贡献。青铜器埋藏会产生多种锈蚀产物,其中 结构致密,可以阻止内部青铜继续被腐蚀,而
结构致密,可以阻止内部青铜继续被腐蚀,而 结构疏松膨胀,可使锈蚀很快蔓延。青铜锈蚀过程大致如下:
结构疏松膨胀,可使锈蚀很快蔓延。青铜锈蚀过程大致如下:不正确 的是
 结构致密,可以阻止内部青铜继续被腐蚀,而
结构致密,可以阻止内部青铜继续被腐蚀,而 结构疏松膨胀,可使锈蚀很快蔓延。青铜锈蚀过程大致如下:
结构疏松膨胀,可使锈蚀很快蔓延。青铜锈蚀过程大致如下:
A.青铜锈蚀Ⅰ过程属于电化学腐蚀,负极的电极反应方程式为: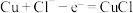 |
B.青铜锈蚀Ⅰ过程中 浓度越大,腐蚀趋势越大 浓度越大,腐蚀趋势越大 |
C.青铜锈蚀Ⅲ生成 的方程式为: 的方程式为: |
| D.青铜器修复可用碳酸钠溶液浸泡一段时间,使其保存更长久 |
您最近半年使用:0次
2024-04-18更新
|
142次组卷
|
2卷引用:浙江绍兴市2023-2024学年高三下学期选考科目适应性考试化学试题