解题方法
1 . 偏磷酸钡Ba(PO3)2具有耐高温、透光性良好等性能,是制备磷酸盐光学玻璃的基础物质。利用湿法磷酸(主要成分为H3PO4,含有少量Mg2+、Fe3+、 、
、 等杂质)制备偏磷酸钡的一种工艺的主要流程如图所示:
等杂质)制备偏磷酸钡的一种工艺的主要流程如图所示: 时:①
时:①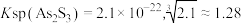 ;
;
②将NH3通入H3PO4溶液中,当pH=3.8~4.5时生成NH4H2PO4,pH=8.0~8.2时生成(NH4)2HPO4。
回答下列问题:
(1)“滤渣1”中含硫化合物的化学式为___________ 。
(2)“滤渣2”的主要成分有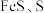 及
及 ,其中生成
,其中生成 的离子方程式为
的离子方程式为___________ ; 下,当
下,当 沉淀完全时,
沉淀完全时, 至少为
至少为___________  [当
[当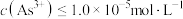 时认为沉淀完全]。
时认为沉淀完全]。
(3)“氨化”的目的之一是通入NH3调节溶液的pH,当溶液pH为4.3时H3PO4转化为___________ (填化学式)。
(4)“脱镁”的目的是生成MgF2沉淀除去Mg2+。若将流程中“氨化”与“脱镁”交换,Mg2+沉淀不完全,原因是___________ 。
(5)“结晶”后得到 晶体,“煅烧”时生成
晶体,“煅烧”时生成 和
和 等物质,其反应的化学方程式为
等物质,其反应的化学方程式为___________ ;比较 键角:
键角: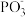
_________  (选填“
(选填“ ”“
”“ ”或“
”或“ ”),其原因是
”),其原因是___________ 。
 、
、 等杂质)制备偏磷酸钡的一种工艺的主要流程如图所示:
等杂质)制备偏磷酸钡的一种工艺的主要流程如图所示:
 时:①
时:①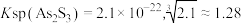 ;
;②将NH3通入H3PO4溶液中,当pH=3.8~4.5时生成NH4H2PO4,pH=8.0~8.2时生成(NH4)2HPO4。
回答下列问题:
(1)“滤渣1”中含硫化合物的化学式为
(2)“滤渣2”的主要成分有
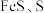 及
及 ,其中生成
,其中生成 的离子方程式为
的离子方程式为 下,当
下,当 沉淀完全时,
沉淀完全时, 至少为
至少为 [当
[当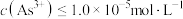 时认为沉淀完全]。
时认为沉淀完全]。(3)“氨化”的目的之一是通入NH3调节溶液的pH,当溶液pH为4.3时H3PO4转化为
(4)“脱镁”的目的是生成MgF2沉淀除去Mg2+。若将流程中“氨化”与“脱镁”交换,Mg2+沉淀不完全,原因是
(5)“结晶”后得到
 晶体,“煅烧”时生成
晶体,“煅烧”时生成 和
和 等物质,其反应的化学方程式为
等物质,其反应的化学方程式为 键角:
键角: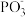
 (选填“
(选填“ ”“
”“ ”或“
”或“ ”),其原因是
”),其原因是
您最近半年使用:0次
7日内更新
|
120次组卷
|
2卷引用:2024届贵州省高三下学期二模化学试题
解题方法
2 . SrCO3可用于金属冶炼和锶盐制备等。以天青石(成分为SrSO4、BaSO4、CaSO4、SiO2)为原料制备SrCO3的工艺流程如图。
回答下列问题:
(1)天青石磨成粉的目的是_______ 。
(2)天青石粉中的SrSO4与氨水、NH4HCO3溶液反应的离子方程式为_____ ;NH4HCO3溶液中c(NH3·H2O)+c(OH-)+c( )
)_____ (填“>”“<”或“=”)c(H2CO3)+c(H+);将滤液1蒸发浓缩、冷却结晶可得副产物_______ (填化学式)。
(3)滤渣的主要成分为_______ (填化学式)。
(4)打浆酸溶后的滤液加热至95~100C.加NaOH溶液调pH=14的目的是_______ 。
(5)碱析后获得Sr(OH)2的操作为_______ 。
(6)以SrCO3和TiO2为原料,在1300~1500℃下煅烧,可制得优良的光学材料及人造宝石SrTiO3.SrTiO3的晶胞结构如图所示,设NA为阿伏加德罗常数的值,晶胞参数为apm。_______ 。
②SrTiO3晶体的密度为_______ 。
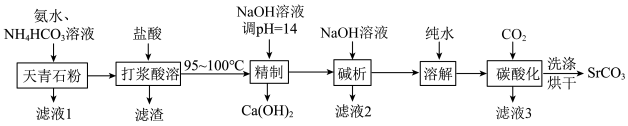
回答下列问题:
(1)天青石磨成粉的目的是
(2)天青石粉中的SrSO4与氨水、NH4HCO3溶液反应的离子方程式为
 )
)(3)滤渣的主要成分为
(4)打浆酸溶后的滤液加热至95~100C.加NaOH溶液调pH=14的目的是
(5)碱析后获得Sr(OH)2的操作为
(6)以SrCO3和TiO2为原料,在1300~1500℃下煅烧,可制得优良的光学材料及人造宝石SrTiO3.SrTiO3的晶胞结构如图所示,设NA为阿伏加德罗常数的值,晶胞参数为apm。
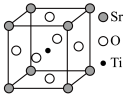
②SrTiO3晶体的密度为
您最近半年使用:0次
名校
解题方法
3 . 以废旧锌锰干电池的炭包(含炭粉、 、
、 和少量
和少量 、
、 等物质)为原料,从中回收
等物质)为原料,从中回收 的工艺流程如下:
的工艺流程如下:
(1)“酸浸”时需将结块的炭包粉碎,目的是_______ 。
(2)“酸浸”过程中, 与稀硝酸反应的离子方程式为
与稀硝酸反应的离子方程式为_______ ,该反应中氧化剂和还原剂的物质的量之比为_______ 。
(3)“溶解”时加入 的作用是
的作用是_______ , 的实际消耗量比理论值高的原因
的实际消耗量比理论值高的原因_______ 。
(4)写出“焙烧”过程的化学反应方程式为_______ 。
(5)碱性锌锰干电池是一种使用广泛的便携式电源,结构如图所示。其电池总反应为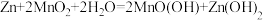 。
。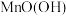 中
中 的化合价为
的化合价为_______ 。
②该电池工作时,负极的反应式为_______ 。
 、
、 和少量
和少量 、
、 等物质)为原料,从中回收
等物质)为原料,从中回收 的工艺流程如下:
的工艺流程如下: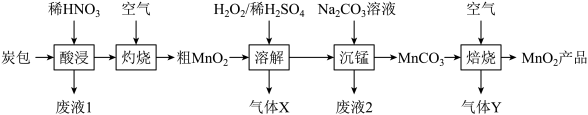
(1)“酸浸”时需将结块的炭包粉碎,目的是
(2)“酸浸”过程中,
 与稀硝酸反应的离子方程式为
与稀硝酸反应的离子方程式为(3)“溶解”时加入
 的作用是
的作用是 的实际消耗量比理论值高的原因
的实际消耗量比理论值高的原因(4)写出“焙烧”过程的化学反应方程式为
(5)碱性锌锰干电池是一种使用广泛的便携式电源,结构如图所示。其电池总反应为
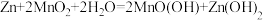 。
。
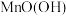 中
中 的化合价为
的化合价为②该电池工作时,负极的反应式为
您最近半年使用:0次
名校
解题方法
4 . 铌 的原子序数为41,其单质具有良好的超导性,可应用于原子能领域。烧绿石精矿可用于冶炼金属铌,某烧绿石精矿的成分为
的原子序数为41,其单质具有良好的超导性,可应用于原子能领域。烧绿石精矿可用于冶炼金属铌,某烧绿石精矿的成分为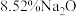 ,
,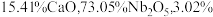 其他不反应的杂质。从烧绿石中提取
其他不反应的杂质。从烧绿石中提取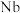 的工艺流程如图所示:
的工艺流程如图所示:
(1)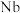 在元素周期表中的位置是
在元素周期表中的位置是___________ 。
(2)上述烧绿石中铌元素的含量为___________ 。
(3)“酸浸”时,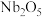 转化为
转化为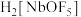 的化学方程式为
的化学方程式为___________ 。
(4)“沉淀”时,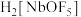 与氨水反应生成
与氨水反应生成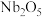 、
、___________ 、 。
。
(5)“还原”时,发生反应的化学方程式为___________ 。
(6)“萃取”“反萃取”后都需要进行的分离操作是___________ 。
(7)废液中的 ,在一定条件可转化为可溶于酸的难溶性盐
,在一定条件可转化为可溶于酸的难溶性盐 。某温度下,用
。某温度下,用 调节
调节 浊液的
浊液的 ,测得体系中
,测得体系中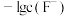 或
或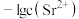 与
与 的关系如图所示。则该温度下难溶盐
的关系如图所示。则该温度下难溶盐 的溶度积常数为
的溶度积常数为___________ 。
 的原子序数为41,其单质具有良好的超导性,可应用于原子能领域。烧绿石精矿可用于冶炼金属铌,某烧绿石精矿的成分为
的原子序数为41,其单质具有良好的超导性,可应用于原子能领域。烧绿石精矿可用于冶炼金属铌,某烧绿石精矿的成分为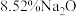 ,
,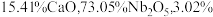 其他不反应的杂质。从烧绿石中提取
其他不反应的杂质。从烧绿石中提取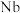 的工艺流程如图所示:
的工艺流程如图所示: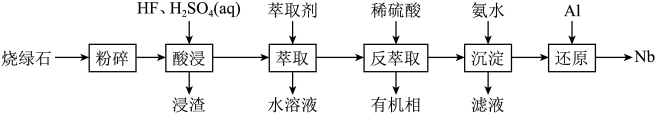
(1)
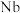 在元素周期表中的位置是
在元素周期表中的位置是(2)上述烧绿石中铌元素的含量为
(3)“酸浸”时,
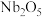 转化为
转化为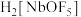 的化学方程式为
的化学方程式为(4)“沉淀”时,
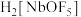 与氨水反应生成
与氨水反应生成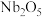 、
、 。
。(5)“还原”时,发生反应的化学方程式为
(6)“萃取”“反萃取”后都需要进行的分离操作是
(7)废液中的
 ,在一定条件可转化为可溶于酸的难溶性盐
,在一定条件可转化为可溶于酸的难溶性盐 。某温度下,用
。某温度下,用 调节
调节 浊液的
浊液的 ,测得体系中
,测得体系中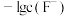 或
或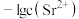 与
与 的关系如图所示。则该温度下难溶盐
的关系如图所示。则该温度下难溶盐 的溶度积常数为
的溶度积常数为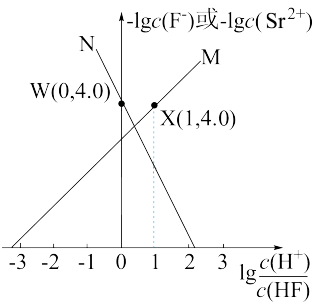
您最近半年使用:0次
名校
5 . 下列离子方程式书写正确的是
A.用高锰酸钾溶液滴定草酸: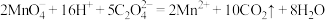 |
B.电解饱和食盐水: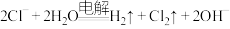 |
C.向 溶液中加入足量稀硝酸: 溶液中加入足量稀硝酸: |
D.将足量 通入 通入 溶液中: 溶液中: |
您最近半年使用:0次
解题方法
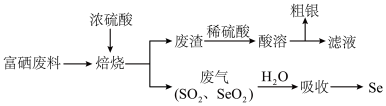
6 . 硒(Se)是一种新型半导体材料。对富硒废料(主要成分为CuSe和Ag2Se)进行综合处理的一种工艺流程如图:
| A.O、S、Se属于同主族元素 |
| B.SeO2既有氧化性又有还原性,其还原性比SO2强 |
C.“焙烧”时的主要反应为CuSe+4H2SO4(浓) CuSO4+SeO2↑+3SO2↑+4H2O CuSO4+SeO2↑+3SO2↑+4H2O |
| D.向“滤液”中滴加过量的氨水,可得到深蓝色的透明溶液 |
您最近半年使用:0次
7 . 宏观辨识与微观探析是化学学科核心素养之一。下列反应的离子方程式书写正确的是
A.将NH3通入稀硝酸中: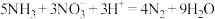 |
B.向FeCl3溶液中加入KSCN溶液: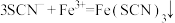 |
C.将Na2SO3溶液与酸性高锰酸钾溶液混合: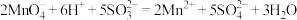 |
D.Mg(OH)2溶于NH4Cl溶液中: |
您最近半年使用:0次
8 . 碱式硫酸铬[ ]主要用于鞣制皮革、作媒染剂及生产氢氧化铬和活性黑染料。以酸性含铬废液(主要含有
]主要用于鞣制皮革、作媒染剂及生产氢氧化铬和活性黑染料。以酸性含铬废液(主要含有 、
、 ,还含有少量
,还含有少量 、
、 、
、 )为原料制备碱式硫酸铬的工艺流程如图所示,回答下列问题:
)为原料制备碱式硫酸铬的工艺流程如图所示,回答下列问题:
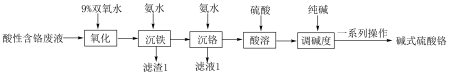
已知:常温下,部分金属阳离子开始沉淀和完全沉淀(离子浓度小于或等于 )时的pH如下表。
)时的pH如下表。
(1)Cr在元素周期表中的位置为_______ 。
(2)加入9%双氧水的作用是_______ (用离子方程式表示)。
(3)“沉铁”时调pH的范围为_______ ~_______ 。
(4)“沉铬”过程发生反应的离子方程式是_______ ,从滤液1中可回收一种氮肥,该物质是_______ (填化学式)。
(5)金属铬的晶胞结构如图,已知晶胞参数为anm。
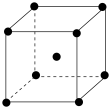
①该晶胞中含铬原子的个数为_______ 。
②铬原子的配位数为_______ 。
③铬原子之间的最短距离为_______ nm(用含a的代数式表示)。
 ]主要用于鞣制皮革、作媒染剂及生产氢氧化铬和活性黑染料。以酸性含铬废液(主要含有
]主要用于鞣制皮革、作媒染剂及生产氢氧化铬和活性黑染料。以酸性含铬废液(主要含有 、
、 ,还含有少量
,还含有少量 、
、 、
、 )为原料制备碱式硫酸铬的工艺流程如图所示,回答下列问题:
)为原料制备碱式硫酸铬的工艺流程如图所示,回答下列问题:
已知:常温下,部分金属阳离子开始沉淀和完全沉淀(离子浓度小于或等于
 )时的pH如下表。
)时的pH如下表。| 离子 |  |  |  |
| 开始沉淀的pH | 7.6 | 1.9 | 4.4 |
| 完全沉淀的pH | 9.6 | 3.1 | 5.6 |
(1)Cr在元素周期表中的位置为
(2)加入9%双氧水的作用是
(3)“沉铁”时调pH的范围为
(4)“沉铬”过程发生反应的离子方程式是
(5)金属铬的晶胞结构如图,已知晶胞参数为anm。

①该晶胞中含铬原子的个数为
②铬原子的配位数为
③铬原子之间的最短距离为
您最近半年使用:0次
解题方法
9 . 以某金属氧化物(用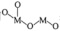 表示)为催化剂,同时消除
表示)为催化剂,同时消除 、NO污染的反应历程如图所示。下列说法错误的是
、NO污染的反应历程如图所示。下列说法错误的是
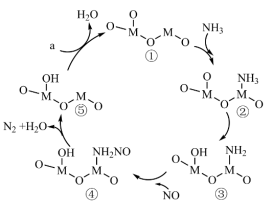
A.在相同条件下, 比NO更易与M形成配位键 比NO更易与M形成配位键 |
| B.反应历程中至少发生3个氧化还原反应 |
| C.通过定量测定发现,反应历程中物质④含量最少,其可能原因是③→④为快反应 |
D.若a为常见非金属单质,则⑤→①的反应可能为 |
您最近半年使用:0次
解题方法
10 . 以硫铁矿(主要成分为 ,含有少量
,含有少量 )为原料制备氯化铁晶体(
)为原料制备氯化铁晶体( )的工艺流程如下:
)的工艺流程如下:
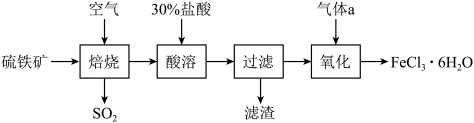
已知:氯化铁晶体受热会生成 ,最后得到
,最后得到 。回答下列问题:
。回答下列问题:
(1)“焙烧”时为加快反应速率可采取的方法有___________ (答出1点即可)。
(2)“焙烧”时反应的化学方程式为 ,则X的化学式为
,则X的化学式为___________ 。“酸溶”时反应的化学方程式为___________ 。
(3)氧化时通入的气体a为___________ (填化学式),反应的离子方程式为___________ 。
(4)焙烧排出的尾气中主要含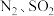 ,可用于尾气处理的试剂有
,可用于尾气处理的试剂有___________ (填标号)。
a.浓硫酸 b. 溶液 c.
溶液 c. 溶液 d.
溶液 d. 溶液
溶液
(5)制取 晶体的操作包括蒸发浓缩、冷却结晶、过滤、洗涤、烘干。烘干时晶体需要减压,原因是
晶体的操作包括蒸发浓缩、冷却结晶、过滤、洗涤、烘干。烘干时晶体需要减压,原因是___________ 。
 ,含有少量
,含有少量 )为原料制备氯化铁晶体(
)为原料制备氯化铁晶体( )的工艺流程如下:
)的工艺流程如下:
已知:氯化铁晶体受热会生成
 ,最后得到
,最后得到 。回答下列问题:
。回答下列问题:(1)“焙烧”时为加快反应速率可采取的方法有
(2)“焙烧”时反应的化学方程式为
 ,则X的化学式为
,则X的化学式为(3)氧化时通入的气体a为
(4)焙烧排出的尾气中主要含
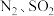 ,可用于尾气处理的试剂有
,可用于尾气处理的试剂有a.浓硫酸 b.
 溶液 c.
溶液 c. 溶液 d.
溶液 d. 溶液
溶液(5)制取
 晶体的操作包括蒸发浓缩、冷却结晶、过滤、洗涤、烘干。烘干时晶体需要减压,原因是
晶体的操作包括蒸发浓缩、冷却结晶、过滤、洗涤、烘干。烘干时晶体需要减压,原因是
您最近半年使用:0次



