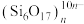以某金属氧化物(用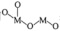 表示)为催化剂,同时消除
表示)为催化剂,同时消除 、NO污染的反应历程如图所示。下列说法错误的是
、NO污染的反应历程如图所示。下列说法错误的是
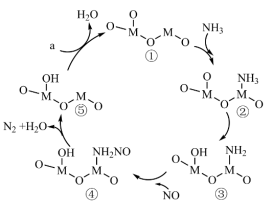
A.在相同条件下, 比NO更易与M形成配位键 比NO更易与M形成配位键 |
| B.反应历程中至少发生3个氧化还原反应 |
| C.通过定量测定发现,反应历程中物质④含量最少,其可能原因是③→④为快反应 |
D.若a为常见非金属单质,则⑤→①的反应可能为 |
更新时间:2024-03-28 22:46:30
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】NaBO3·4H2O的阴离子结构如图所示。硼砂(Na2B4O7)与氢氧化钠的混合溶液中加入双氧水可以制备NaBO3·4H2O。下列说法正确的是
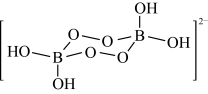
| A.硼砂与氢氧化钠、双氧水的反应为氧化还原反应 |
| B.NaBO3·4H2O不具有杀菌消毒功能与漂白性 |
| C.用浓硫酸处理NaBO3·4H2O可以得到O2 |
| D.分别向同体积的硼砂稀溶液和蒸馏水中加入相同的少量盐酸,前者pH变化大 |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐2】下列叙述正确的有
①CO2、SiO2、P2O5均为酸性氧化物
②Ca(HCO3)2、Fe(OH)3、FeCl2均可由化合反应制得
③碘晶体分散到酒精中、饱和氯化铁溶液滴入沸水中所形成的分散系分别为:溶液、胶体
④灼热的炭与CO2的反应、Ba(OH)2·8H2O与NH4 Cl的反应均既是氧化还原反应,又是吸热反应
⑤需要通电才可进行的有:电离、电解、电镀、电化学腐蚀、电泳
⑥氯化铝溶液与氢氧化铝胶体具有的共同性质是:能透过滤纸,滴加NaOH溶液都能先生成沉淀后沉淀溶解
⑦苛性钾、次氯酸、氯气按顺序分类依次为:强电解质、弱电解质和非电解质
⑧碱石灰、生石灰、玻璃、漂白粉、光导纤维都是混合物
①CO2、SiO2、P2O5均为酸性氧化物
②Ca(HCO3)2、Fe(OH)3、FeCl2均可由化合反应制得
③碘晶体分散到酒精中、饱和氯化铁溶液滴入沸水中所形成的分散系分别为:溶液、胶体
④灼热的炭与CO2的反应、Ba(OH)2·8H2O与NH4 Cl的反应均既是氧化还原反应,又是吸热反应
⑤需要通电才可进行的有:电离、电解、电镀、电化学腐蚀、电泳
⑥氯化铝溶液与氢氧化铝胶体具有的共同性质是:能透过滤纸,滴加NaOH溶液都能先生成沉淀后沉淀溶解
⑦苛性钾、次氯酸、氯气按顺序分类依次为:强电解质、弱电解质和非电解质
⑧碱石灰、生石灰、玻璃、漂白粉、光导纤维都是混合物
| A.3个 | B.4个 | C.5个 | D.6个 |
您最近半年使用:0次
【推荐1】细菌与矿物表面接触,通过酶的作用将金属硫化物氧化为酸溶性的二价金属离子和硫化物的原子团,使矿物溶解。细菌-硫化矿作用机理表述如下:

下列有关说法错误的是

下列有关说法错误的是
A.若MS为 ,1 mol ,1 mol  发生反应转移16 mol e- 发生反应转移16 mol e- |
B.若MS为 ,发生反应: ,发生反应: |
| C.温度越高,反应速率越快,浸出率一定得到提高 |
| D.若MS为CuS,发生反应中消耗的氧化剂与还原剂的物质的量比为2∶1 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】已知溶液中:氧化性IO3—>I2>SO32-。向含3 mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如右图所示,下列说法正确的是


| A.a点反应的还原剂是NaHSO3,被氧化的元素是碘元素 |
| B.b点反应的离子方程式是:3HSO3-+IO3-+3OH-=3SO42-+I-+3H2O |
| C.c点到d点的反应中共转移0.6mol电子 |
| D.往200mL 1 mol/L的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式是:5 HSO3- + 2IO3- == I2+ 5SO42-+ 3H++ H2O |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】黄铁矿(主要成分FeS2),在空气中会被缓慢氧化,氧化过程如图所示。下列说法不正确的是
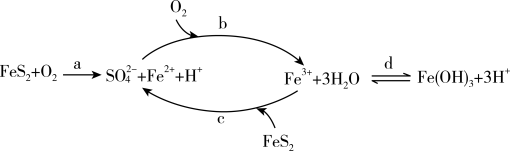

| A.发生反应a时,0.05mol FeS2被氧化时消耗标准状况下空气的体积大约19.6L |
| B.为了验证b过程反应后溶液中含Fe2+,可选用KSCN溶液和氯水 |
| C.c发生反应的离子方程式为:14Fe3+ +FeS2+8H2O=15Fe2++2SO42-+16H+ |
| D.已知25 ℃时,Ksp[Fe(OH)3]=2.79×10-39,则该温度下d逆反应的平衡常数为K=2.79×103 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】已知反应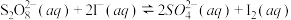 ,若往该溶液中加入含
,若往该溶液中加入含 的某溶液,反应机理:
的某溶液,反应机理:
①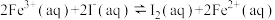
②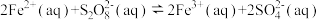
下列说法错误的是
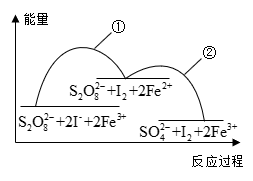
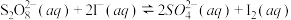 ,若往该溶液中加入含
,若往该溶液中加入含 的某溶液,反应机理:
的某溶液,反应机理:①
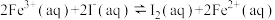
②
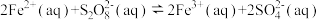
下列说法错误的是

A. 是该反应的催化剂,加入 是该反应的催化剂,加入 后降低了该反应的活化能 后降低了该反应的活化能 |
| B.往该溶液中滴加淀粉溶液,溶液变蓝,适当升温,蓝色加深 |
C.步骤①中 和 和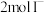 的总能量低于 的总能量低于 和 和 的总能量 的总能量 |
D.增大 浓度或 浓度或 浓度,反应①、反应②的反应速率均加快 浓度,反应①、反应②的反应速率均加快 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】某同学在室温下进行下图所示实验。(已知:H2C2O4为二元弱酸)

试管a、b、c中溶液褪色分别耗时690s、677s、600s。下列说法正确的是

试管a、b、c中溶液褪色分别耗时690s、677s、600s。下列说法正确的是
| A.反应的离子方程式为2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O |
| B.试管c反应至300 s时,溶液中剩余的c(KMnO4)=0.0025 mol/L |
| C.对比试管a、b,得到的结论是H2C2O4水溶液浓度增大,反应速率加快 |
| D.对比试管c、d,可验证H+浓度对反应速率的影响 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】以CO2和H2为原料,在催化剂作用下合成CH3OH的反应为CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H,反应过程中的副反应为CO2(g)+H2(g)
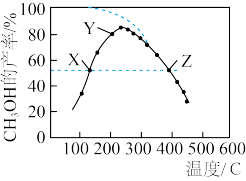
CH3OH(g)+H2O(g) △H,反应过程中的副反应为CO2(g)+H2(g) CO(g)+H2O(g),反应相同时间,测得不同温度下CH3OH的产率如图中实线所示(图中虚线表示相同条件下CH3OH的平衡产率随温度的变化)。下列说法正确的是
CO(g)+H2O(g),反应相同时间,测得不同温度下CH3OH的产率如图中实线所示(图中虚线表示相同条件下CH3OH的平衡产率随温度的变化)。下列说法正确的是
 CH3OH(g)+H2O(g) △H,反应过程中的副反应为CO2(g)+H2(g)
CH3OH(g)+H2O(g) △H,反应过程中的副反应为CO2(g)+H2(g) CO(g)+H2O(g),反应相同时间,测得不同温度下CH3OH的产率如图中实线所示(图中虚线表示相同条件下CH3OH的平衡产率随温度的变化)。下列说法正确的是
CO(g)+H2O(g),反应相同时间,测得不同温度下CH3OH的产率如图中实线所示(图中虚线表示相同条件下CH3OH的平衡产率随温度的变化)。下列说法正确的是
A.CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H>0 CH3OH(g)+H2O(g) △H>0 |
| B.图中X点所示条件下,延长反应时间能提高CH3OH的产率 |
| C.图中X、Z点的正反应速率与其逆反应速率均相等 |
| D.选用合适的催化剂不可以减弱副反应的发生 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】CuCl是白色难溶于水的化合物,溶于较浓盐酸时生成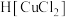 ,其盐酸溶液能吸收CO,形成
,其盐酸溶液能吸收CO,形成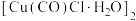 ,其结构为:
,其结构为: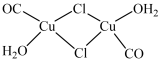 ,此物质可以定量吸收CO,也能吸收O2、PH3、C2H2等气体。下列说法正确的是
,此物质可以定量吸收CO,也能吸收O2、PH3、C2H2等气体。下列说法正确的是
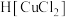 ,其盐酸溶液能吸收CO,形成
,其盐酸溶液能吸收CO,形成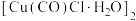 ,其结构为:
,其结构为: ,此物质可以定量吸收CO,也能吸收O2、PH3、C2H2等气体。下列说法正确的是
,此物质可以定量吸收CO,也能吸收O2、PH3、C2H2等气体。下列说法正确的是A.由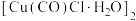 结构可知, 结构可知, 原子不满足8电子稳定结构 原子不满足8电子稳定结构 |
B.测定混合气体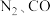 和 和 中 中 的含量时,应先用 的含量时,应先用 的盐酸溶液吸收 的盐酸溶液吸收 |
C.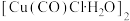 中 中 的化合价为 的化合价为 ,配位数为4 ,配位数为4 |
D.用 与 与 溶液制备 溶液制备 时,反应体系中先加入浓盐酸后期再加水稀释可提高产率 时,反应体系中先加入浓盐酸后期再加水稀释可提高产率 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】FeSO4·7H2O晶体的结构如图所示,下列有关说法不正确 的是
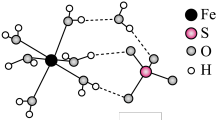

| A.Fe2+的配位数是6 |
| B.1molFeSO4·7H2O中含σ键的数目为18NA |
C.H2O与SO 、H2O与Fe2+之间的作用力类型不同 、H2O与Fe2+之间的作用力类型不同 |
| D.Fe2+的d轨道参与了成键 |
您最近半年使用:0次

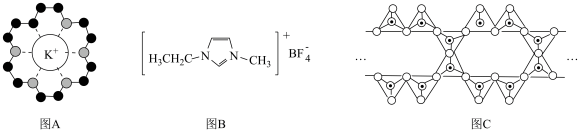
 作用,体现了超分子“分子识别”的特征
作用,体现了超分子“分子识别”的特征 摩尔质量更大,具更高的熔沸点
摩尔质量更大,具更高的熔沸点