名校
解题方法
1 . 细菌可以促使铁、氮两种元素进行氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如下图所示。___________ (填字母序号)。
a.N2转化为氨态氮 b.硝化过程 c.反硝化过程
(2)氨气是生产氮肥的主要原料,工业合成氨的化学方程式为___________ 。
(3)硝化过程中,含氮物质发生___________ (填“氧化”或“还原”)反应。
(4)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02 mol氮气时,转移的电子的物质的量为___________ mol。
(5)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),用离子方程式说明利用土壤中的铁循环脱除水体中氨态氮的原理:___________ 。

a.N2转化为氨态氮 b.硝化过程 c.反硝化过程
(2)氨气是生产氮肥的主要原料,工业合成氨的化学方程式为
(3)硝化过程中,含氮物质发生
(4)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02 mol氮气时,转移的电子的物质的量为
(5)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),用离子方程式说明利用土壤中的铁循环脱除水体中氨态氮的原理:
您最近半年使用:0次
名校
解题方法
2 . 氧化钇( )广泛应用于微波、军工、光学玻璃、陶瓷、激光、超导等许多尖端行业。利用废荧光粉(主要成分为ZnO、
)广泛应用于微波、军工、光学玻璃、陶瓷、激光、超导等许多尖端行业。利用废荧光粉(主要成分为ZnO、 ,还含有一定量的
,还含有一定量的 、
、 、MgO)等)为原料生产
、MgO)等)为原料生产 的工艺流程如图所示:
的工艺流程如图所示: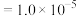 mol⋅L
mol⋅L 时,认为已沉淀完全。
时,认为已沉淀完全。
②常温下,相关金属离子开始沉淀和沉淀完全时的pH如图所示:
(1)“酸浸”时需适当提高浸取液的温度,其目的是_______ ;
采用离子浓度传感器测得相同时间内 的浸取率与浸取溶液温度的关系如图所示,
的浸取率与浸取溶液温度的关系如图所示, ℃后,
℃后, 的浸取率随温度升高而减小的原因是
的浸取率随温度升高而减小的原因是_______ 。_______ (填化学式)。
(3)“沉钇”后的滤液中浓度最大的金属离子是_______ (填离子符号);若常温下测得 恰好沉淀完全时滤液中
恰好沉淀完全时滤液中 mol⋅L
mol⋅L ,则
,则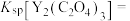
_______ mol⋅L (保留两位有效数字)。
(保留两位有效数字)。
(4)“沉钇”后所得晶体为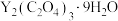 ,其中C元素的化合价为
,其中C元素的化合价为_______ 。
(5)“焙烧”时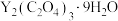 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
 )广泛应用于微波、军工、光学玻璃、陶瓷、激光、超导等许多尖端行业。利用废荧光粉(主要成分为ZnO、
)广泛应用于微波、军工、光学玻璃、陶瓷、激光、超导等许多尖端行业。利用废荧光粉(主要成分为ZnO、 ,还含有一定量的
,还含有一定量的 、
、 、MgO)等)为原料生产
、MgO)等)为原料生产 的工艺流程如图所示:
的工艺流程如图所示: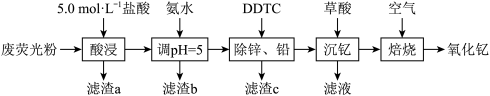
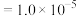 mol⋅L
mol⋅L 时,认为已沉淀完全。
时,认为已沉淀完全。②常温下,相关金属离子开始沉淀和沉淀完全时的pH如图所示:

(1)“酸浸”时需适当提高浸取液的温度,其目的是
采用离子浓度传感器测得相同时间内
 的浸取率与浸取溶液温度的关系如图所示,
的浸取率与浸取溶液温度的关系如图所示, ℃后,
℃后, 的浸取率随温度升高而减小的原因是
的浸取率随温度升高而减小的原因是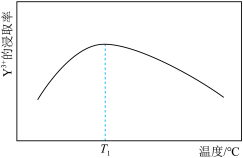
(3)“沉钇”后的滤液中浓度最大的金属离子是
 恰好沉淀完全时滤液中
恰好沉淀完全时滤液中 mol⋅L
mol⋅L ,则
,则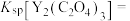
 (保留两位有效数字)。
(保留两位有效数字)。(4)“沉钇”后所得晶体为
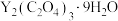 ,其中C元素的化合价为
,其中C元素的化合价为(5)“焙烧”时
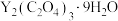 发生反应的化学方程式为
发生反应的化学方程式为
您最近半年使用:0次
名校
解题方法
3 . 亚硝酸钠 是一种化工产品,易溶于水,无漂白性。亚硝酸钠的制备原理为
是一种化工产品,易溶于水,无漂白性。亚硝酸钠的制备原理为
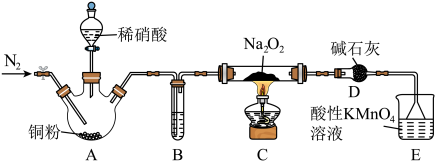
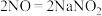 。某小组设计实验制备亚硝酸钠并测定其纯度和探究其性质,装置如图所示。已知:常温下,酸性
。某小组设计实验制备亚硝酸钠并测定其纯度和探究其性质,装置如图所示。已知:常温下,酸性 溶液能吸收
溶液能吸收 生成无色的
生成无色的 和
和 。
。
(1) 装置的作用是
装置的作用是___________ 。
(2)写出 装置中发生反应的化学方程式:
装置中发生反应的化学方程式:___________ 。
(3) 装置中紫红色变为无色,发生反应的离子方程式为
装置中紫红色变为无色,发生反应的离子方程式为___________ 。
(4)实验完毕,设计实验证明产品是否含有 :
:___________ 。
(5)为了探究 的性质,设计如下实验:
的性质,设计如下实验:
上述实验能证明 具有氧化性的是
具有氧化性的是___________ (填“I”或“II”)。
(6)取
 产品溶于水配制成
产品溶于水配制成 溶液,准确量取
溶液,准确量取 所配溶液于锥形瓶中,恰好与
所配溶液于锥形瓶中,恰好与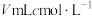 酸性
酸性 溶液完全反应。该产品中
溶液完全反应。该产品中 的质量分数为
的质量分数为___________ (已知: 和酸性
和酸性 溶液反应生成
溶液反应生成 和
和 )。
)。
 是一种化工产品,易溶于水,无漂白性。亚硝酸钠的制备原理为
是一种化工产品,易溶于水,无漂白性。亚硝酸钠的制备原理为
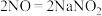 。某小组设计实验制备亚硝酸钠并测定其纯度和探究其性质,装置如图所示。已知:常温下,酸性
。某小组设计实验制备亚硝酸钠并测定其纯度和探究其性质,装置如图所示。已知:常温下,酸性 溶液能吸收
溶液能吸收 生成无色的
生成无色的 和
和 。
。
(1)
 装置的作用是
装置的作用是(2)写出
 装置中发生反应的化学方程式:
装置中发生反应的化学方程式:(3)
 装置中紫红色变为无色,发生反应的离子方程式为
装置中紫红色变为无色,发生反应的离子方程式为(4)实验完毕,设计实验证明产品是否含有
 :
:(5)为了探究
 的性质,设计如下实验:
的性质,设计如下实验:| 序号 | 操作 | 现象 |
| I | 取少量 溶于水,滴加酚酞溶液 溶于水,滴加酚酞溶液 | 溶液变红色 |
| II | 取少量  溶于水,滴加稀硫酸和 溶于水,滴加稀硫酸和 溶液,再滴加淀粉溶液 溶液,再滴加淀粉溶液 | 溶液变蓝色 |
 具有氧化性的是
具有氧化性的是(6)取

 产品溶于水配制成
产品溶于水配制成 溶液,准确量取
溶液,准确量取 所配溶液于锥形瓶中,恰好与
所配溶液于锥形瓶中,恰好与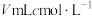 酸性
酸性 溶液完全反应。该产品中
溶液完全反应。该产品中 的质量分数为
的质量分数为 和酸性
和酸性 溶液反应生成
溶液反应生成 和
和 )。
)。
您最近半年使用:0次
名校
解题方法
4 . 氨氮废水中的氮多以 和NH3∙H2O形式存在。某工厂处理氨氮废水流程如下:
和NH3∙H2O形式存在。某工厂处理氨氮废水流程如下:
(1)过程I的目的是将 转化为NH3,其离子方程式为
转化为NH3,其离子方程式为___________ ,鼓入热空气能将氨吹出的原因是___________ 。
(2)过程II加入NaClO溶液可将废水中残留的NH3∙H2O转化为无污染气体,该反应的化学方程式为___________ 。
(3)含余氯废水的主要成分是NaClO以及HClO,X可选用以下哪种溶液以达到将余氯转化为无毒物质的目的___________ (填字母)。
a.KOH b.Na2SO3 c.KMnO4 d.NaCl
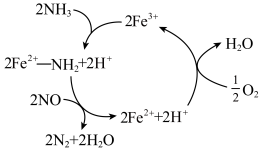
(4)有氧条件下,NH3催化还原NO是主要的烟气脱硝技术。在以Fe2O3为主的催化剂上可能发生的反应过程如图。写出总反应的化学方程式:___________ 。
 和NH3∙H2O形式存在。某工厂处理氨氮废水流程如下:
和NH3∙H2O形式存在。某工厂处理氨氮废水流程如下:
(1)过程I的目的是将
 转化为NH3,其离子方程式为
转化为NH3,其离子方程式为(2)过程II加入NaClO溶液可将废水中残留的NH3∙H2O转化为无污染气体,该反应的化学方程式为
(3)含余氯废水的主要成分是NaClO以及HClO,X可选用以下哪种溶液以达到将余氯转化为无毒物质的目的
a.KOH b.Na2SO3 c.KMnO4 d.NaCl
(4)有氧条件下,NH3催化还原NO是主要的烟气脱硝技术。在以Fe2O3为主的催化剂上可能发生的反应过程如图。写出总反应的化学方程式:
您最近半年使用:0次
解题方法
5 . 草酸(H2C2O4)是一种具有还原性的弱酸。某小组在浓硫酸催化下,用硝酸氧化葡萄糖制草酸,设计实验装置(加热、搅拌和仪器固定装置均已略去)如图所示。
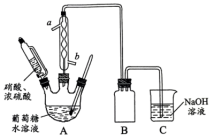
(1)球形冷凝管的a端___________ (填“进水”或“出水”)。装置B瓶的作用是___________ 。
(2)配制硝酸和浓硫酸的混合液时,加入酸的先后顺序是___________ 。
(3)55~60℃时,装置A中生成 ,同时生成氮的氧化物。
,同时生成氮的氧化物。
①该实验采用的加热方式为___________ 。
②当尾气中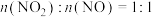 时,装置C中的
时,装置C中的 溶液能将NO、
溶液能将NO、 吸收转化为
吸收转化为 ,反应的离子方程式为
,反应的离子方程式为___________ 。
(4)若浓硫酸用量过多,会导致草酸产率降低的原因是___________ 。
(5)用高锰酸钾标准溶液可滴定草酸的浓度,滴定前需润洗的仪器为___________ ;滴定终点的判定方法是___________ 。

(1)球形冷凝管的a端
(2)配制硝酸和浓硫酸的混合液时,加入酸的先后顺序是
(3)55~60℃时,装置A中生成
 ,同时生成氮的氧化物。
,同时生成氮的氧化物。①该实验采用的加热方式为
②当尾气中
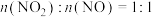 时,装置C中的
时,装置C中的 溶液能将NO、
溶液能将NO、 吸收转化为
吸收转化为 ,反应的离子方程式为
,反应的离子方程式为(4)若浓硫酸用量过多,会导致草酸产率降低的原因是
(5)用高锰酸钾标准溶液可滴定草酸的浓度,滴定前需润洗的仪器为
您最近半年使用:0次
6 . 实验室中可用MnO2或KMnO4固体制备氯气,反应的化学方程式如下:
①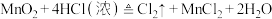
②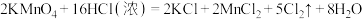
回答下列问题:
(1)对比反应①和②的反应原理,下列作为反应②的发生装置的是_______ (填字母序号)。

(2)反应①和②中,浓盐酸均体现出_______ 性和_______ 性。
(3)用双线桥法,标出下列反应中的电子转移情况_______ 。
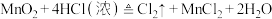
(4)若反应②在水溶液中进行,将反应②改写成离子方程式_______ 。
(5)化学实验中经常提到“酸性高锰酸钾溶液”,这里的“酸性”是因为配制高锰酸钾溶液时加入了_______ (填“硫酸”或“盐酸”)的缘故。
(6)1868年狄肯和洪特发明了用氯化铜作催化剂,在加热到450℃时,用空气中的氧气来氧化氯化氢气体制取氯气的方法——地康法。根据信息,写出该反应的化学方程式_______ 。
①
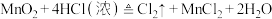
②
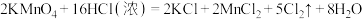
回答下列问题:
(1)对比反应①和②的反应原理,下列作为反应②的发生装置的是

(2)反应①和②中,浓盐酸均体现出
(3)用双线桥法,标出下列反应中的电子转移情况
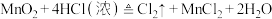
(4)若反应②在水溶液中进行,将反应②改写成离子方程式
(5)化学实验中经常提到“酸性高锰酸钾溶液”,这里的“酸性”是因为配制高锰酸钾溶液时加入了
(6)1868年狄肯和洪特发明了用氯化铜作催化剂,在加热到450℃时,用空气中的氧气来氧化氯化氢气体制取氯气的方法——地康法。根据信息,写出该反应的化学方程式
您最近半年使用:0次
7 . 化学源于生活,她与我们生活息息相关。
Ⅰ.我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要过程如下图所示(部分物质已略去)。
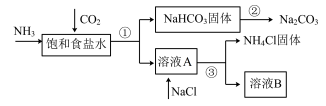
(1)①~③所涉及的操作方法中,包含过滤的是_______ (填序号)。
(2)根据上图,将化学方程式补充完整:
_______ 
_______ 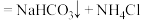
(3)煅烧 固体的化学方程式是
固体的化学方程式是_______ 。
(4)关于上述过程,下列说法中正确的是_______ (填字母)。
a. 不可循环使用
不可循环使用
b.副产物 可用作肥料
可用作肥料
c.反应过程中应先通入极易溶于水的 ,使溶液显碱性,然后再通入
,使溶液显碱性,然后再通入 气体
气体
Ⅱ.氧化还原反应是一类重要的化学反应,广泛应用于生产和生活中。
(5)氢化钠( )在野外被用作生氢剂,其原理是
)在野外被用作生氢剂,其原理是 ,该反应中氧化剂是
,该反应中氧化剂是_______ ,还原剂是_______ ;被氧化与被还原元素的物质的量之比为:_______ 。
(6)某离子反应中涉及 、
、 、
、 、
、 、
、 、
、 六种微粒。其中
六种微粒。其中 、
、 的物质的量随时间变化的曲线如图所示。下列判断不正确的是
的物质的量随时间变化的曲线如图所示。下列判断不正确的是_______ 。
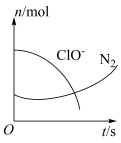
a.该反应的氧化剂是
b.消耗 还原剂,转移
还原剂,转移 电子
电子
c.氧化剂与还原剂的物质的量之比为
d.当生成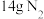 时,消耗的
时,消耗的 为
为
e.氧化性: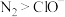
(7)高铁酸钠( ),易溶于水,是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。工业上制备高铁酸钠有多种方法。在次氯酸钠溶液中加入氢氧化钠和硫酸铁可制备高铁酸钠,此法被称为次氯酸盐氧化法。高铁酸钠(
),易溶于水,是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。工业上制备高铁酸钠有多种方法。在次氯酸钠溶液中加入氢氧化钠和硫酸铁可制备高铁酸钠,此法被称为次氯酸盐氧化法。高铁酸钠( )中铁元素的价态为
)中铁元素的价态为_______ ;写出制备高铁酸钠的离子方程式_______ 。
Ⅰ.我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要过程如下图所示(部分物质已略去)。

(1)①~③所涉及的操作方法中,包含过滤的是
(2)根据上图,将化学方程式补充完整:


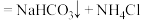
(3)煅烧
 固体的化学方程式是
固体的化学方程式是(4)关于上述过程,下列说法中正确的是
a.
 不可循环使用
不可循环使用b.副产物
 可用作肥料
可用作肥料c.反应过程中应先通入极易溶于水的
 ,使溶液显碱性,然后再通入
,使溶液显碱性,然后再通入 气体
气体Ⅱ.氧化还原反应是一类重要的化学反应,广泛应用于生产和生活中。
(5)氢化钠(
 )在野外被用作生氢剂,其原理是
)在野外被用作生氢剂,其原理是 ,该反应中氧化剂是
,该反应中氧化剂是(6)某离子反应中涉及
 、
、 、
、 、
、 、
、 、
、 六种微粒。其中
六种微粒。其中 、
、 的物质的量随时间变化的曲线如图所示。下列判断不正确的是
的物质的量随时间变化的曲线如图所示。下列判断不正确的是
a.该反应的氧化剂是

b.消耗
 还原剂,转移
还原剂,转移 电子
电子c.氧化剂与还原剂的物质的量之比为

d.当生成
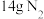 时,消耗的
时,消耗的 为
为
e.氧化性:
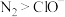
(7)高铁酸钠(
 ),易溶于水,是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。工业上制备高铁酸钠有多种方法。在次氯酸钠溶液中加入氢氧化钠和硫酸铁可制备高铁酸钠,此法被称为次氯酸盐氧化法。高铁酸钠(
),易溶于水,是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。工业上制备高铁酸钠有多种方法。在次氯酸钠溶液中加入氢氧化钠和硫酸铁可制备高铁酸钠,此法被称为次氯酸盐氧化法。高铁酸钠( )中铁元素的价态为
)中铁元素的价态为
您最近半年使用:0次
解题方法
8 . 以黄铁矿(主要成分 )为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所示。
)为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所示。

回答问题:
(1)写出黄铁矿煅烧的化学方程式_______ 。
(2)由炉渣制备还原铁粉的化学方程式为_______ 。
(3)欲得到更纯的 ,反应①应通入
,反应①应通入_______ (填“过量”或“不足量”)的 气体。
气体。
(4)因为 具有
具有_______ 性,导致商品 中不可避免地存在
中不可避免地存在 检验其中含有
检验其中含有 的方法是
的方法是_______ 。
 )为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所示。
)为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所示。
回答问题:
(1)写出黄铁矿煅烧的化学方程式
(2)由炉渣制备还原铁粉的化学方程式为
(3)欲得到更纯的
 ,反应①应通入
,反应①应通入 气体。
气体。(4)因为
 具有
具有 中不可避免地存在
中不可避免地存在 检验其中含有
检验其中含有 的方法是
的方法是
您最近半年使用:0次
9 . 根据题意,完成问题。
(1)碳酸氢钠受热易分解,可用作膨松剂,请写出相应反应的化学方程式:________ 。
(2)过氧化钠可在呼吸面具中作为氧气来源,请写出相应反应的化学方程式:________ 。
(3)钠与钾在元素周期表中的同一主族,化学性质相似,请写出钾与硫酸铜溶液反应的离子方程式:________ 。
(4)84消毒液与洁厕灵(主要成分为HCl)混用,产生有毒气体,请写出该反应的离子方程式:________ 。
(5)在一定条件下,下列粒子的还原性强弱顺序为 ,在
,在 溶液中通入
溶液中通入 请写出该反应的离子方程式:
请写出该反应的离子方程式:________ 。
(6)________ _______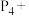 ________
________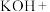 ________
________ ________
________ ________
________
(7)_______ ________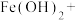 ________
________ ________
________ ________
________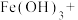 ________
________
(1)碳酸氢钠受热易分解,可用作膨松剂,请写出相应反应的化学方程式:
(2)过氧化钠可在呼吸面具中作为氧气来源,请写出相应反应的化学方程式:
(3)钠与钾在元素周期表中的同一主族,化学性质相似,请写出钾与硫酸铜溶液反应的离子方程式:
(4)84消毒液与洁厕灵(主要成分为HCl)混用,产生有毒气体,请写出该反应的离子方程式:
(5)在一定条件下,下列粒子的还原性强弱顺序为
 ,在
,在 溶液中通入
溶液中通入 请写出该反应的离子方程式:
请写出该反应的离子方程式:(6)
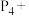 ________
________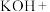 ________
________ ________
________ ________
________
(7)
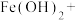 ________
________ ________
________ ________
________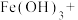 ________
________
您最近半年使用:0次
名校
10 . 亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊 法制备亚氯酸钠的流程如图:
法制备亚氯酸钠的流程如图:
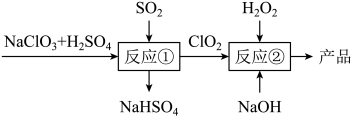
(1)反应①的化学方程式为: ,该反应的还原产物是
,该反应的还原产物是___________ (写化学式)。
(2)在□补充反应②另一种产物,并配平此离子方程式,然后用单线桥法分析此化学反应。___________
________ClO2+ ________H2O2+ ________OH-=________ +________H2O+ _______□
+________H2O+ _______□
(3)NaClO2中Cl的化合价为___________ ,H2O2在反应②中___________ (填字母)。
A.只能作氧化剂 B.只能作还原剂 C.既能作氧化剂也能作还原剂
(4)实验室采用马蒂逊 法制备NaClO2的实验装置如图甲所示:
法制备NaClO2的实验装置如图甲所示:

已知:①ClO2的熔点为-59℃,沸点为 11℃,H2O2的沸点为150℃。
②当温度低于38℃时,NaClO2饱和溶液中析出的晶体是NaClO2∙3H2O;当温度在 38~60℃时,析出NaClO2;温度高于 60℃时,NaClO2分解。
C中将装置浸入冰水浴中的目的是___________ 。
 法制备亚氯酸钠的流程如图:
法制备亚氯酸钠的流程如图:
(1)反应①的化学方程式为:
 ,该反应的还原产物是
,该反应的还原产物是(2)在□补充反应②另一种产物,并配平此离子方程式,然后用单线桥法分析此化学反应。
________ClO2+ ________H2O2+ ________OH-=________
 +________H2O+ _______□
+________H2O+ _______□(3)NaClO2中Cl的化合价为
A.只能作氧化剂 B.只能作还原剂 C.既能作氧化剂也能作还原剂
(4)实验室采用马蒂逊
 法制备NaClO2的实验装置如图甲所示:
法制备NaClO2的实验装置如图甲所示:
已知:①ClO2的熔点为-59℃,沸点为 11℃,H2O2的沸点为150℃。
②当温度低于38℃时,NaClO2饱和溶液中析出的晶体是NaClO2∙3H2O;当温度在 38~60℃时,析出NaClO2;温度高于 60℃时,NaClO2分解。
C中将装置浸入冰水浴中的目的是
您最近半年使用:0次



