名校
解题方法
1 . 研究小组以 (绿色固体)、
(绿色固体)、 、THF(四氯呋喃,液体)等物质为原料制备固体配合物
、THF(四氯呋喃,液体)等物质为原料制备固体配合物 ,该配合物可作为有机反应的催化剂
,该配合物可作为有机反应的催化剂
(1)无水 (紫色固体,易升华)的制备装置如图所示(夹持装置略)。
(紫色固体,易升华)的制备装置如图所示(夹持装置略)。

①仪器a的名称为________ 。
②本实验持续通入 的目的有赶走体系中原有的空气、
的目的有赶走体系中原有的空气、________ 。
③反应管的温度升到660℃时发生反应,生成 和
和 (光气),其化学方程式为
(光气),其化学方程式为________ 。 有剧毒,与水反应生成两种酸性气体,b装置中生成的盐是
有剧毒,与水反应生成两种酸性气体,b装置中生成的盐是________ (填化学式)。
④反应管右端有15cm在加热炉外,其作用是________________ 。
(2) 的合成装置如图所示(搅拌和夹持装置咯)
的合成装置如图所示(搅拌和夹持装置咯)

将制备的无水 和极少量锌粉放入滤纸套筒内,双颈烧瓶中加入足量无水THF。制备反应的原理为
和极少量锌粉放入滤纸套筒内,双颈烧瓶中加入足量无水THF。制备反应的原理为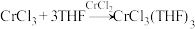 。
。
实验时烧瓶中THF受热蒸发,蒸汽沿蒸汽导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,与滤纸套筒内的物质接触。当液面达到虹吸管3顶端时,经虹吸管3返回双颈烧瓶.从而实现了THF与 的连续反应及产物的连续萃取。
的连续反应及产物的连续萃取。
①锌粉的作用是________________ (用化学方程式表示)。
② 和
和 在THF的溶解性分别为
在THF的溶解性分别为________ 、________ (填“溶”或“不溶”)。
③合成反应完成后,取下双颈烧瓶,蒸发THF得到固体产品6.7410g。则该实验的产率为________ %。[已知: 的摩尔质量为152g/mol;
的摩尔质量为152g/mol; 的摩尔质量为374.5g/mol]
的摩尔质量为374.5g/mol]
 (绿色固体)、
(绿色固体)、 、THF(四氯呋喃,液体)等物质为原料制备固体配合物
、THF(四氯呋喃,液体)等物质为原料制备固体配合物 ,该配合物可作为有机反应的催化剂
,该配合物可作为有机反应的催化剂(1)无水
 (紫色固体,易升华)的制备装置如图所示(夹持装置略)。
(紫色固体,易升华)的制备装置如图所示(夹持装置略)。
①仪器a的名称为
②本实验持续通入
 的目的有赶走体系中原有的空气、
的目的有赶走体系中原有的空气、③反应管的温度升到660℃时发生反应,生成
 和
和 (光气),其化学方程式为
(光气),其化学方程式为 有剧毒,与水反应生成两种酸性气体,b装置中生成的盐是
有剧毒,与水反应生成两种酸性气体,b装置中生成的盐是④反应管右端有15cm在加热炉外,其作用是
(2)
 的合成装置如图所示(搅拌和夹持装置咯)
的合成装置如图所示(搅拌和夹持装置咯)
将制备的无水
 和极少量锌粉放入滤纸套筒内,双颈烧瓶中加入足量无水THF。制备反应的原理为
和极少量锌粉放入滤纸套筒内,双颈烧瓶中加入足量无水THF。制备反应的原理为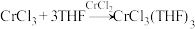 。
。实验时烧瓶中THF受热蒸发,蒸汽沿蒸汽导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,与滤纸套筒内的物质接触。当液面达到虹吸管3顶端时,经虹吸管3返回双颈烧瓶.从而实现了THF与
 的连续反应及产物的连续萃取。
的连续反应及产物的连续萃取。①锌粉的作用是
②
 和
和 在THF的溶解性分别为
在THF的溶解性分别为③合成反应完成后,取下双颈烧瓶,蒸发THF得到固体产品6.7410g。则该实验的产率为
 的摩尔质量为152g/mol;
的摩尔质量为152g/mol; 的摩尔质量为374.5g/mol]
的摩尔质量为374.5g/mol]
您最近一年使用:0次
2023-03-14更新
|
689次组卷
|
4卷引用:宁夏回族自治区银川一中2023-2024学年高三上学期第五次月考理科综合试题
名校
2 . 高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:
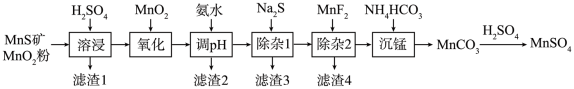
相关金属离子[c0(Mn+)=0.1 mol·L−1]形成氢氧化物沉淀的pH范围如下:
(1)“滤渣1”含有S和________________ ;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式_______ 。
(2)“氧化”中添加适量的MnO2的作用是将________________________ 。
(3)“调pH”除铁和铝,溶液的pH范围应调节为_______ ~6之间。
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是______________ 。
(5)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是______
(6)写出“沉锰”的离子方程式_____________________________________ 。

相关金属离子[c0(Mn+)=0.1 mol·L−1]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(2)“氧化”中添加适量的MnO2的作用是将
(3)“调pH”除铁和铝,溶液的pH范围应调节为
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是
(5)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是
(6)写出“沉锰”的离子方程式
您最近一年使用:0次
2019-09-07更新
|
362次组卷
|
7卷引用:宁夏石嘴山市第三中学2020届高三上学期第一次适应性(开学)考试化学试题



