名校
解题方法
1 . X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如表:
(1)X和W的元素符号分别为___ 、___ 。
(2)X与Y形成的原子个数比为2∶1的化合物中,Y原子最外层为8电子结构,请写出该化合物的电子式___ ,工业合成Y的氢化物的化学方程式为___ 。
(3)X和Z组成的化合物中,既含有极性共价键又含有非极性共价键的是___ 。此化合物还可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为___ 。
| 元素 | 相关信息 |
| X | X的单质为密度最小的气体 |
| Y | Y的氢化物的水溶液呈碱性 |
| Z | Z是地壳中含量最高的元素 |
| W | W的一种核素的质量数为35,中子数为18 |
(2)X与Y形成的原子个数比为2∶1的化合物中,Y原子最外层为8电子结构,请写出该化合物的电子式
(3)X和Z组成的化合物中,既含有极性共价键又含有非极性共价键的是
您最近一年使用:0次
名校
解题方法
2 . 铬铁矿的主要成分可表示为FeO·Cr2O3,还含有MgO、Al2O3、Fe2O3等杂质,图为以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的流程图:

已知:①Na2CO3+Al2O3 2NaAlO2+CO2↑;②Cr2O
2NaAlO2+CO2↑;②Cr2O +H2O
+H2O 2CrO
2CrO +2H+。
+2H+。
根据题意回答下列问题:
(1)已知焙烧时FeO·Cr2O3转化为Na2CrO4和Fe2O3,写出焙烧时反应的化学方程式_______ 。焙烧时要将铬铁矿石粉碎的目的是_______ 。
(2)固体X中主要含有_______ (填写化学式);酸化步骤用醋酸调节溶液pH<5,其目的是_______ 。
(3)写出生成Y的离子方程式_______ 。
(4)表是相关物质的溶解度数据,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl=K2Cr2O7↓+2NaCl,该反应在溶液中能发生的理由是_______ 。
(5)操作Ⅲ由多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体._______ 、_______ 、过滤、洗涤、干燥。

已知:①Na2CO3+Al2O3
 2NaAlO2+CO2↑;②Cr2O
2NaAlO2+CO2↑;②Cr2O +H2O
+H2O 2CrO
2CrO +2H+。
+2H+。根据题意回答下列问题:
(1)已知焙烧时FeO·Cr2O3转化为Na2CrO4和Fe2O3,写出焙烧时反应的化学方程式
(2)固体X中主要含有
(3)写出生成Y的离子方程式
(4)表是相关物质的溶解度数据,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl=K2Cr2O7↓+2NaCl,该反应在溶液中能发生的理由是
| 物质 | KCl | NaCl | K2Cr2O7 | Na2Cr2O7 | |
| 溶解度(g/100 g水) | 0 ℃ | 28 | 35.7 | 4.7 | 163 |
| 40 ℃ | 40.1 | 36.4 | 26.3 | 215 | |
| 80℃ | 51.3 | 38 | 73 | 376 | |
您最近一年使用:0次
名校
解题方法
3 . 高铁酸钾(K2FeO4)是一种环保、高效、多功能饮用水处理剂,制备流程如图所示:
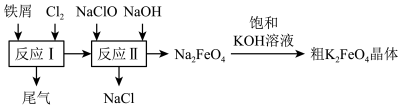
下列叙述错误的是

下列叙述错误的是
| A.该生产条件下,物质的溶解性:Na2FeO4> K2FeO4 |
| B.可用FeCl2溶液作为反应I中尾气吸收剂,且反应后溶液能在上述流程中利用 |
| C.反应II中氧化剂与还原剂的物质的量之比为2∶3 |
| D.用K2FeO4对饮用水杀菌消毒的同时可产生胶体吸附杂质净化水 |
您最近一年使用:0次
2020-12-14更新
|
313次组卷
|
4卷引用:甘肃省嘉峪关市第一中学2021届高三上学期三模考试化学试题
名校
解题方法
4 . 氧化还原反应是一类重要的化学反应,在工农业生产、日常生活中都有广泛的用途。亚硝酸钠(NaNO2)像食盐一样有咸味,但有很强的毒性,误食NaNO2会使人中毒。已知亚硝酸钠能发生如下反应: 2NaNO2+4HI=2NO↑+2NaI+I2+2H2O
(1)用双线桥法标出该反应中电子转移的方向及数目:_______ ,被氧化的原子与被还原的原子数目之比为______ 。
(2)自来水中的 对人类健康会产生危害,碱性条件下用Al粉还原
对人类健康会产生危害,碱性条件下用Al粉还原 ,产物是N2,发生的反应可表示如下,完成方程式并配平。
,产物是N2,发生的反应可表示如下,完成方程式并配平。
____ Al+___  +
+_____ =____  +
+____ N2↑+____
(1)用双线桥法标出该反应中电子转移的方向及数目:
(2)自来水中的
 对人类健康会产生危害,碱性条件下用Al粉还原
对人类健康会产生危害,碱性条件下用Al粉还原 ,产物是N2,发生的反应可表示如下,完成方程式并配平。
,产物是N2,发生的反应可表示如下,完成方程式并配平。 +
+ +
+
您最近一年使用:0次
2020-09-16更新
|
248次组卷
|
2卷引用:甘肃省嘉峪关市第一中学2021届高三上学期一模考试化学试卷



