铬铁矿的主要成分可表示为FeO·Cr2O3,还含有MgO、Al2O3、Fe2O3等杂质,图为以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的流程图:

已知:①Na2CO3+Al2O3 2NaAlO2+CO2↑;②Cr2O
2NaAlO2+CO2↑;②Cr2O +H2O
+H2O 2CrO
2CrO +2H+。
+2H+。
根据题意回答下列问题:
(1)已知焙烧时FeO·Cr2O3转化为Na2CrO4和Fe2O3,写出焙烧时反应的化学方程式_______ 。焙烧时要将铬铁矿石粉碎的目的是_______ 。
(2)固体X中主要含有_______ (填写化学式);酸化步骤用醋酸调节溶液pH<5,其目的是_______ 。
(3)写出生成Y的离子方程式_______ 。
(4)表是相关物质的溶解度数据,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl=K2Cr2O7↓+2NaCl,该反应在溶液中能发生的理由是_______ 。
(5)操作Ⅲ由多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体._______ 、_______ 、过滤、洗涤、干燥。

已知:①Na2CO3+Al2O3
 2NaAlO2+CO2↑;②Cr2O
2NaAlO2+CO2↑;②Cr2O +H2O
+H2O 2CrO
2CrO +2H+。
+2H+。根据题意回答下列问题:
(1)已知焙烧时FeO·Cr2O3转化为Na2CrO4和Fe2O3,写出焙烧时反应的化学方程式
(2)固体X中主要含有
(3)写出生成Y的离子方程式
(4)表是相关物质的溶解度数据,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl=K2Cr2O7↓+2NaCl,该反应在溶液中能发生的理由是
| 物质 | KCl | NaCl | K2Cr2O7 | Na2Cr2O7 | |
| 溶解度(g/100 g水) | 0 ℃ | 28 | 35.7 | 4.7 | 163 |
| 40 ℃ | 40.1 | 36.4 | 26.3 | 215 | |
| 80℃ | 51.3 | 38 | 73 | 376 | |
更新时间:2021-09-07 20:03:13
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
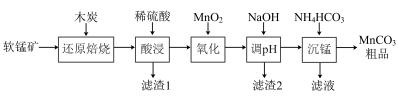
【推荐1】碳酸锰(MnCO3)是制造电信器材的软磁铁氧体,也用作含锰的催化剂,瓷釉、涂料和清漆的颜料等。利用软锰矿(主要成分是MnO2还含有Fe2O3、CaCO3、CuO等杂质)制备碳酸锰的流程如下图所示:
②部分阳离子以氢氧化物形式沉淀时溶液的pH范围如下表:
(1)“还原焙烧”中,MnO2转化为MnO,如果是在实验室中进行该项操作,装软锰矿的仪器名称是___________ 。
(2)滤渣1的主要成分有木炭、___________ 、___________ 。
(3)“调pH”时, pH控制的范围为______ ≤pH<______ 。
(4)“沉锰”时发生反应的离子方程式为___________ ; 此步骤需加热, 温度不能太高也不能太低, 原因是___________ 。
(5) 中存在过氧键(-O-O-),
中存在过氧键(-O-O-),  中S的化合价为
中S的化合价为___________ ;实验室可以用  溶液来检验 Mn2+是否完全发生反应,写出对应的离子方程式
溶液来检验 Mn2+是否完全发生反应,写出对应的离子方程式___________ 。
(6)在600~700℃下,将一定量的 MnCO3置于空气中加热至恒重,此时测得固体的质量残留率为68.70%,则该反应中固体产物的化学式为___________ 。

②部分阳离子以氢氧化物形式沉淀时溶液的pH范围如下表:
| 沉淀物 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | Mn(OH)2 |
| 开始沉淀时的 pH | 7.5 | 2.7 | 4.2 | 8.3 |
| 完全沉淀时的pH | 9.7 | 3.7 | 7.4 | 9.8 |
(1)“还原焙烧”中,MnO2转化为MnO,如果是在实验室中进行该项操作,装软锰矿的仪器名称是
(2)滤渣1的主要成分有木炭、
(3)“调pH”时, pH控制的范围为
(4)“沉锰”时发生反应的离子方程式为
(5)
 中存在过氧键(-O-O-),
中存在过氧键(-O-O-),  中S的化合价为
中S的化合价为 溶液来检验 Mn2+是否完全发生反应,写出对应的离子方程式
溶液来检验 Mn2+是否完全发生反应,写出对应的离子方程式(6)在600~700℃下,将一定量的 MnCO3置于空气中加热至恒重,此时测得固体的质量残留率为68.70%,则该反应中固体产物的化学式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
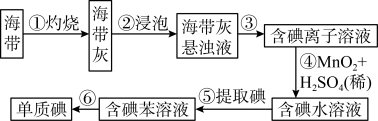
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是_______ (从下列仪器中选出所需的一些仪器,用标号字母填写在空白处)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤③的实验操作名称是______________ ;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是______________ 。
(3)步骤④反应的离子方程式为_______________________________________ 。

请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤③的实验操作名称是
(3)步骤④反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】钛酸钡(BaTiO3)是电子陶瓷器件的重要基础原料。工业上以钛精矿(主要成分为TiO2)和BaCl2为主要原料制备钛酸钡粉体的工艺流程如下:
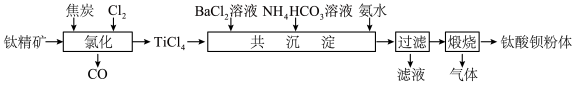
已知:①TiCl4水解生成H2TiO3沉淀;
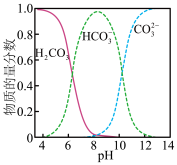
②水溶液中含碳微粒随pH的分布如图所示。
(1) “氯化”在800 ℃时进行,其反应的化学方程式为________ 。
(2) “共沉淀”时,需控制溶液pH为10~11,其原因是:①___________ ;② ________ 。
(3) “滤液”中溶质的主要成分为________ (填化学式)。过滤得到的固体通常用一定浓度的NH4HCO3溶液进行洗涤,其主要原因是___________ 。
(4) “煅烧”得到的钛酸钡粉体中钡钛质量比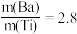 ,钛酸钡粉体中可能含有的杂质为
,钛酸钡粉体中可能含有的杂质为____________ (填化学式)。

已知:①TiCl4水解生成H2TiO3沉淀;
②水溶液中含碳微粒随pH的分布如图所示。

(1) “氯化”在800 ℃时进行,其反应的化学方程式为
(2) “共沉淀”时,需控制溶液pH为10~11,其原因是:①
(3) “滤液”中溶质的主要成分为
(4) “煅烧”得到的钛酸钡粉体中钡钛质量比
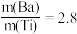 ,钛酸钡粉体中可能含有的杂质为
,钛酸钡粉体中可能含有的杂质为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】高铝粉煤灰是火力发电厂燃煤锅炉排放出的固体废物,含有较多的Al2O3,少量MgO、CaO、 铁的氧化物及其他不溶性杂质。从粉煤灰中提取Al2O3的工艺流程如图。
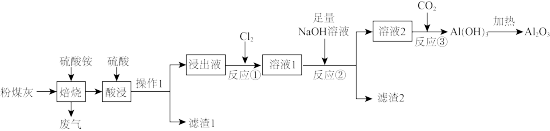
(1)操作1的名称是_______ , 滤渣1中除了原不溶性杂质外,还有_______ 。
(2)检验浸出液中含有Fe2+的操作与现象是_______ 。
(3)反应①的离子方程式为_______ ,反应①中还可以用_______ (填试剂化学式)替代Cl2。
(4)滤渣2的主要成分有_______ 。
(5)溶液2中含铝元素的化合物与过量CO2反应的化学方程式为_______ 。
(6)实验室配制100mL 2.00mol/L H2SO4溶液。
①需要18.00mol/L浓H2SO4的体积为_______ mL。(计算结果保留1位小数)
②下列仪器中,需要的有_______ (填标号),还缺少的玻璃仪器为_______ 。(填仪器名称)
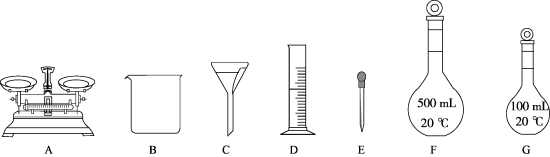

(1)操作1的名称是
(2)检验浸出液中含有Fe2+的操作与现象是
(3)反应①的离子方程式为
(4)滤渣2的主要成分有
(5)溶液2中含铝元素的化合物与过量CO2反应的化学方程式为
(6)实验室配制100mL 2.00mol/L H2SO4溶液。
①需要18.00mol/L浓H2SO4的体积为
②下列仪器中,需要的有

您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】工业上用铝土矿(含氧化铝、氧化铁)制取铝的过程如图:
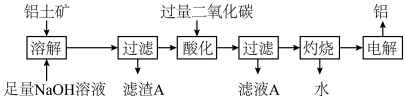
请回答下列问题:
(1)“滤渣A”的化学式为_____ ,该物质除了用于冶炼金属以外,还可用作____ 。
(2)通入“过量二氧化碳”时生成沉淀的离子方程式为________ 。
(3)往“滤液A”中加入适量的CaO后过滤,所得滤液可以加入___ 过程中循环利用。
(4)若铝土矿中还含有二氧化硅,则“灼烧”后所得固体中混有的杂质为___ (填化学式)。

请回答下列问题:
(1)“滤渣A”的化学式为
(2)通入“过量二氧化碳”时生成沉淀的离子方程式为
(3)往“滤液A”中加入适量的CaO后过滤,所得滤液可以加入
(4)若铝土矿中还含有二氧化硅,则“灼烧”后所得固体中混有的杂质为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】石墨在材料领域有重要应用,某初级石墨中含 (7.8%)、
(7.8%)、 (5.1%)和
(5.1%)和 (3.1%)等杂质,提纯与综合利用工艺流程如下:
(3.1%)等杂质,提纯与综合利用工艺流程如下:
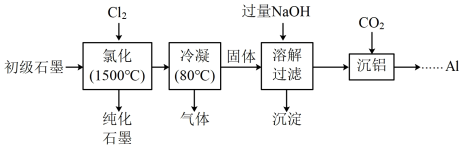
已知:
①氯化后,石墨中氧化物杂质均转变为相应的氯化物;
② 的沸点为57.6℃,金属氯化物的沸点均高于150℃。
的沸点为57.6℃,金属氯化物的沸点均高于150℃。
(1)“氯化”时,先向反应器中通入 一段时间,再加热,主要目的是
一段时间,再加热,主要目的是___________ 。
(2)“冷凝”后,所得“气体”的成分有 和
和___________ (填化学式)。
(3)“溶解过滤”时,加过量NaOH溶液的目的是___________ 。取少量滤液于试管中,___________ (实验操作及现象),证明沉淀已完全。
(4)写出Al的一种用途___________ 。
 (7.8%)、
(7.8%)、 (5.1%)和
(5.1%)和 (3.1%)等杂质,提纯与综合利用工艺流程如下:
(3.1%)等杂质,提纯与综合利用工艺流程如下:
已知:
①氯化后,石墨中氧化物杂质均转变为相应的氯化物;
②
 的沸点为57.6℃,金属氯化物的沸点均高于150℃。
的沸点为57.6℃,金属氯化物的沸点均高于150℃。(1)“氯化”时,先向反应器中通入
 一段时间,再加热,主要目的是
一段时间,再加热,主要目的是(2)“冷凝”后,所得“气体”的成分有
 和
和(3)“溶解过滤”时,加过量NaOH溶液的目的是
(4)写出Al的一种用途
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐1】一种利用含Co废渣(主要含金属Co,还含有Fe、Zn)制取CoCO3的流程如下图所示:

已知:部分金属离子开始生成氢氧化物沉淀和沉淀完全的pH如下表所示:
(1)酸浸时,不改变H2SO4的浓度和体积,任写出一种可以加快反应速率的方法:_______ 。
(2)酸浸后所得溶液中含Co2+、Fe2+、Zn2+,基态Co2+的电子排布式为_______ 。
(3)加入ZnO调pH的目的是促进Fe3+水解转化为Fe(OH)3沉淀,调pH的范围为_______ ,加入ZnO将Fe3+转化为Fe(OH)3沉淀的离子方程式为_______ 。
(4)写出沉钴反应的离子方程式:_______ 。

已知:部分金属离子开始生成氢氧化物沉淀和沉淀完全的pH如下表所示:
| Fe3+ | Zn2+ | Fe2+ | Co2+ | |
| 开始沉淀的pH | 1.5 | 5.4 | 5.8 | 6.6 |
| 沉淀完全的pH | 3.2 | 8.2 | 8.8 | 9.4 |
(2)酸浸后所得溶液中含Co2+、Fe2+、Zn2+,基态Co2+的电子排布式为
(3)加入ZnO调pH的目的是促进Fe3+水解转化为Fe(OH)3沉淀,调pH的范围为
(4)写出沉钴反应的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】镍氢电池是一种新型绿色电池,利用废旧镍氢电池的金属电极芯[主要成分为Ni(OH)2、Co(OH)2及少量铁、铝的氧化物等]生产硫酸镍、碳酸钴的工艺流程如图。

已知:部分金属阳离子以氢氧化物的形式沉淀时溶液的pH见表:
回答下列问题:
(1)步骤①用稀硫酸浸取金属电极芯前,提高浸取率方法_______ (写两种)。
(2)沉淀A的主要成分_______ ,步骤②调pH的范围为_______ 。
(3)将“母液1”的pH调至3~4,再加入NaClO,NaClO的作用是_______ 。
(4)步骤④离子方程式_______ ,若用盐酸代替H2SO4和H2O2的混合液也能达到目的,从环保角度分析不采用盐酸的原因:_______ 。
(5)步骤⑤中“母液3”与NaHCO3溶液反应的离子方程式为_______ 。

已知:部分金属阳离子以氢氧化物的形式沉淀时溶液的pH见表:
| 金属阳离子 | Fe2+ | Fe3+ | Al3+ | Ni2+ | Co2+ |
| 开始沉淀时pH | 6.3 | 1.5 | 3.4 | 6.2 | 7.15 |
| 完全沉淀时pH(金属阳离子浓度<10-5mol/L) | 9.0 | 3.2 | 4.7 | 9.2 | 9.15 |
(1)步骤①用稀硫酸浸取金属电极芯前,提高浸取率方法
(2)沉淀A的主要成分
(3)将“母液1”的pH调至3~4,再加入NaClO,NaClO的作用是
(4)步骤④离子方程式
(5)步骤⑤中“母液3”与NaHCO3溶液反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】四川含有非常丰富的矿产资源。以川西铝土矿(主要成分为Al2O3、Fe2O3、SiO2、少量FeS2)为原料,生产Fe3O4的部分工艺流程如下:

(1)Fe3O4_______ (填“属于”或“不属于”)碱性氧化物。
(2)为了提高碱浸效率,常采用的方法有_______ 。(写出一条即可)
(3)已知上述流程中两次焙烧均会产生SO2,滤渣中含大量的Fe2O3。
①矿粉焙烧过程中还原剂和氧化剂物质的量之比为_______ ,该过程加入少量CaO的目的是_______ ,用NaOH溶液吸收处理SO2的离子方程式为_______ 。
②“过滤”得到的滤液中含有的阴离子有OH-、_______ 、_______ 。
③Fe2O3与FeS2混合后焙烧(缺氧条件下)反应的化学方程式为_______ 。

(1)Fe3O4
(2)为了提高碱浸效率,常采用的方法有
(3)已知上述流程中两次焙烧均会产生SO2,滤渣中含大量的Fe2O3。
①矿粉焙烧过程中还原剂和氧化剂物质的量之比为
②“过滤”得到的滤液中含有的阴离子有OH-、
③Fe2O3与FeS2混合后焙烧(缺氧条件下)反应的化学方程式为
您最近一年使用:0次
【推荐1】工业上可由菱锌矿(主要成分为 ,还含有Ni、Cd、Fe、Mn等元素)制备ZnO。工艺如图所示:
,还含有Ni、Cd、Fe、Mn等元素)制备ZnO。工艺如图所示:
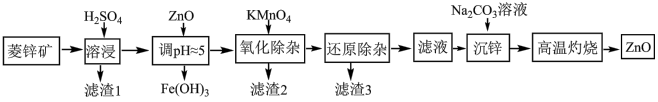
相关金属离子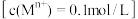 形成氢氧化物沉淀的pH范围如下:
形成氢氧化物沉淀的pH范围如下:
已知①“溶浸”后的溶液 ,所含金属离子主要有:
,所含金属离子主要有: 、
、 、
、 、
、 、
、 。
。
②弱酸性溶液中 氧化
氧化 时,产物中含Mn元素物质只有
时,产物中含Mn元素物质只有 。
。
③氧化性强弱顺序:
(1)基态Zn原子的简化电子排布式为[Ar]______ ,
(2)①“溶浸”过程中,为了提高浸出率,可采取的措施是______ 。(写一条即可)
②“调pH”时,可替代ZnO的一种含锌化合物是______ 。(用化学式表示)
③“调pH”时,若 ,此时溶液中
,此时溶液中 的最大浓度
的最大浓度
______  。
。
(3)写出“氧化除杂”时 溶液与
溶液与 反应的离子方程式
反应的离子方程式_______ 。
(4)“还原除杂”除去的离子是______ ;
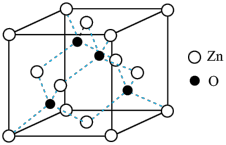
(5)氧化锌的一种晶体的晶胞是立方晶胞(如图所示),请在图中画出该晶胞沿z轴方向的平面投影图______

 ,还含有Ni、Cd、Fe、Mn等元素)制备ZnO。工艺如图所示:
,还含有Ni、Cd、Fe、Mn等元素)制备ZnO。工艺如图所示: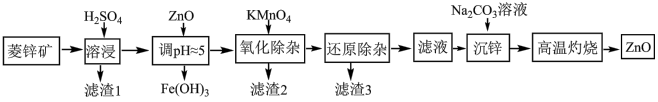
相关金属离子
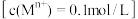 形成氢氧化物沉淀的pH范围如下:
形成氢氧化物沉淀的pH范围如下:金属离子 |
|
|
|
|
|
|
开始沉淀的pH | 1.5 | 6.3 | 6.0 | 7.4 | 8.1 | 6.9 |
沉淀完全的pH | 2.8 | 8.3 | 8.0 | 9.4 | 10.1 | 8.9 |
 ,所含金属离子主要有:
,所含金属离子主要有: 、
、 、
、 、
、 、
、 。
。②弱酸性溶液中
 氧化
氧化 时,产物中含Mn元素物质只有
时,产物中含Mn元素物质只有 。
。③氧化性强弱顺序:

(1)基态Zn原子的简化电子排布式为[Ar]
(2)①“溶浸”过程中,为了提高浸出率,可采取的措施是
②“调pH”时,可替代ZnO的一种含锌化合物是
③“调pH”时,若
 ,此时溶液中
,此时溶液中 的最大浓度
的最大浓度
 。
。(3)写出“氧化除杂”时
 溶液与
溶液与 反应的离子方程式
反应的离子方程式(4)“还原除杂”除去的离子是
(5)氧化锌的一种晶体的晶胞是立方晶胞(如图所示),请在图中画出该晶胞沿z轴方向的平面投影图


您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】三氯氧磷( )和氯化亚砜(
)和氯化亚砜( )均为重要的化工产品。现以氯气、二氧化硫和三氯化磷为原料,采用二级间歇式反应装置联合制备三氯氧磷和氯化亚砜。实验过程中,控制氯气和二氧化硫通入的体积比为1:1,实验过程示意图如图:
)均为重要的化工产品。现以氯气、二氧化硫和三氯化磷为原料,采用二级间歇式反应装置联合制备三氯氧磷和氯化亚砜。实验过程中,控制氯气和二氧化硫通入的体积比为1:1,实验过程示意图如图:
(1)实验室制备氯气或二氧化硫时均可能用到的仪器有_______。
(2)A装置的作用为:_______ 、______ 、使气体充分混合。
(3)B中发生反应的化学方程式是__________ ,反应结束后,B瓶中的物质可采用_______ (填实验方法)使其分离。
(4)实验开始时需水浴加热,一段时间后改为冷水浴,其原因是_________ 。
(5)反应5~6小时后,暂停通入气体。将B瓶拆下,C瓶装在图中B瓶处,并在原C瓶处重新装上一个盛有 的圆底烧瓶。继续通气反应一段时间后重复以上步骤,上述操作的优点是
的圆底烧瓶。继续通气反应一段时间后重复以上步骤,上述操作的优点是________ 。
(6)已知反应前加入三氯化磷 ,最终得到
,最终得到 氯化亚砜,则三氯氧磷的产率为
氯化亚砜,则三氯氧磷的产率为________ 。
 )和氯化亚砜(
)和氯化亚砜( )均为重要的化工产品。现以氯气、二氧化硫和三氯化磷为原料,采用二级间歇式反应装置联合制备三氯氧磷和氯化亚砜。实验过程中,控制氯气和二氧化硫通入的体积比为1:1,实验过程示意图如图:
)均为重要的化工产品。现以氯气、二氧化硫和三氯化磷为原料,采用二级间歇式反应装置联合制备三氯氧磷和氯化亚砜。实验过程中,控制氯气和二氧化硫通入的体积比为1:1,实验过程示意图如图:
| 名称 | 熔点/℃ | 沸点/℃ | 溶解性 | 理化性质 |
| 三氯氧磷 | 2 | 105.3 | 可溶于有机溶剂 | 遇水分解 |
| 氯化亚砜 | 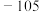 | 78.8 | 可溶于有机溶剂 | 遇水分解,加热分解 |
(1)实验室制备氯气或二氧化硫时均可能用到的仪器有_______。
| A.温度计 | B.酒精灯 | C.牛角管 | D.圆底烧瓶 |
(2)A装置的作用为:
(3)B中发生反应的化学方程式是
(4)实验开始时需水浴加热,一段时间后改为冷水浴,其原因是
(5)反应5~6小时后,暂停通入气体。将B瓶拆下,C瓶装在图中B瓶处,并在原C瓶处重新装上一个盛有
 的圆底烧瓶。继续通气反应一段时间后重复以上步骤,上述操作的优点是
的圆底烧瓶。继续通气反应一段时间后重复以上步骤,上述操作的优点是(6)已知反应前加入三氯化磷
 ,最终得到
,最终得到 氯化亚砜,则三氯氧磷的产率为
氯化亚砜,则三氯氧磷的产率为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】某研究性学习小组查阅资料:“氯气与硫在加热条件下生成二氯化硫(S2Cl2),该物质遇水迅速反应,他们利用如下仪器和药品制取纯净的氯气与硫反应来制备S2Cl2
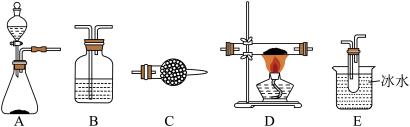
实验过程所提供的药品有:浓盐酸、浓H2SO4、MnO2、KMnO4(H+)、饱和NaHCO3溶液、碱石灰、硫磺、NaOH溶液、冰水、饱和食盐水。回答下列问题:
(1)利用所提供的设备和药品,写出制备Cl2的离子方程式:_______
(2)在该实验过程中两次用到仪器B,第一次装置B中的药品是_______ ,第二次装置B的作用是_______ 。
(3)能否省略装置C_______ (填“能”或“否”),原因是_______ 。
(4)实验开始后,当_______ (填现象),点燃D处的酒精灯。
(5)某学生利用装置A测定Cu、Zn合金中Zn的含量。用排水法收集到合金和稀硫酸反应生成的气体的体积总比预期的要多,他经过认真分析后,认为应对装置A略作改进,你认为怎样改进:_______ 。

实验过程所提供的药品有:浓盐酸、浓H2SO4、MnO2、KMnO4(H+)、饱和NaHCO3溶液、碱石灰、硫磺、NaOH溶液、冰水、饱和食盐水。回答下列问题:
(1)利用所提供的设备和药品,写出制备Cl2的离子方程式:
(2)在该实验过程中两次用到仪器B,第一次装置B中的药品是
(3)能否省略装置C
(4)实验开始后,当
(5)某学生利用装置A测定Cu、Zn合金中Zn的含量。用排水法收集到合金和稀硫酸反应生成的气体的体积总比预期的要多,他经过认真分析后,认为应对装置A略作改进,你认为怎样改进:
您最近一年使用:0次




