1 . 五氯化锑(SbCl5)主要用作氟化工的催化剂、纺织工业织物的阻燃剂、染料工业的中间体。实验室根据反应 ,利用如下装置制备SbCl5 (加热及夹持装置略)。
,利用如下装置制备SbCl5 (加热及夹持装置略)。
实验室制备SbCl5的步骤如下:
ⅰ.保持80℃的条件,在盛有SbCl3的三颈烧瓶中通入Cl2,反应生成SbCl5;
ⅱ.将三颈烧瓶中的反应混合物转移到双颈烧瓶中;
ⅲ.减压蒸馏,收集目标物质。
回答下列问题:
(1)写出用K2MnO4和浓盐酸制备Cl2的离子方程式___________ ,其中体现还原性和酸性的HCl的物质的量之比为___________ 。
(2)实验装置中,两个冷凝管___________ (填“能”或“不能”)交换使用,步骤ⅰ中对三颈烧瓶进行加热的最佳方式是___________ 加热。
(3)写出图示实验装置存在的一处弊端:___________ 。
(4)步骤ⅱ将反应后混合液转移至双颈烧瓶中的方法:在b处连接减压装置,使三颈烧瓶中的液体流入双颈烧瓶。进行该操作前,需___________ (填活塞1和2的开、关的情况)。
(5)步骤ⅲ采用减压蒸馏,而不是常压蒸馏的原因是___________ ;调节减压装置至1.86kPa,收集___________ ℃左右的馏分。减压蒸馏时,玻璃毛细管的作用有___________ (填字母)。
a.防止暴沸 b.搅拌 c.连通大气,保持常压
 ,利用如下装置制备SbCl5 (加热及夹持装置略)。
,利用如下装置制备SbCl5 (加热及夹持装置略)。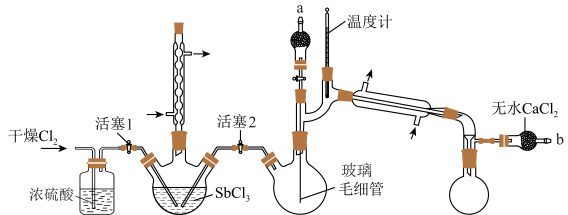
| 物质 | 熔点/℃ | 沸点/℃ | 性质 |
| SbCl3 | 73.4 | 223(101.3kPa) | 均极易水解 |
| SbCl5 | 2.8 | 176(101.3kPa,140℃)时分解 | |
| 68(1.86kPa)、79(2.90kPa) |
ⅰ.保持80℃的条件,在盛有SbCl3的三颈烧瓶中通入Cl2,反应生成SbCl5;
ⅱ.将三颈烧瓶中的反应混合物转移到双颈烧瓶中;
ⅲ.减压蒸馏,收集目标物质。
回答下列问题:
(1)写出用K2MnO4和浓盐酸制备Cl2的离子方程式
(2)实验装置中,两个冷凝管
(3)写出图示实验装置存在的一处弊端:
(4)步骤ⅱ将反应后混合液转移至双颈烧瓶中的方法:在b处连接减压装置,使三颈烧瓶中的液体流入双颈烧瓶。进行该操作前,需
(5)步骤ⅲ采用减压蒸馏,而不是常压蒸馏的原因是
a.防止暴沸 b.搅拌 c.连通大气,保持常压
您最近一年使用:0次
解题方法
2 . 广泛用于火箭、原子能、电子工业等领域。以矿石(主要成分是Be2SiO4,含少量MnO等)为原料制备Be的工艺流程如图所示。
(1)“烧结”之前,将铍矿石粉碎成粉末,其目的是_____ 。
(2)“除锰”时发生反应的离子方程式为_____ 。“除锰”时温度不宜过高,原因是_____ 。
(3)制备无水 过程如下:将
过程如下:将 溶于盐酸,蒸发浓缩、冷却结晶得到
溶于盐酸,蒸发浓缩、冷却结晶得到 ;加热
;加热 和
和 的混合物得到无水
的混合物得到无水 ,该化学方程式为
,该化学方程式为_____ 。也可以用 固体替代
固体替代 ,
, 的作用是
的作用是_____ 。
(4)1828年德国化学家维勒用金属钾还原熔融的氯化铍而得到 。若将这个反应设计成原电池,则在电池的
。若将这个反应设计成原电池,则在电池的_____ (填“正”或“负”)极得到Be。
(5)铍和铝的化学性质相似,下列叙述错误的是_____ (填字母)。
A.铍是一种轻金属,能与冷水反应
B.常温下,BeCl2溶液的pH<7
C.氧化铍的熔点高、耐酸碱腐蚀

(1)“烧结”之前,将铍矿石粉碎成粉末,其目的是
(2)“除锰”时发生反应的离子方程式为
(3)制备无水
 过程如下:将
过程如下:将 溶于盐酸,蒸发浓缩、冷却结晶得到
溶于盐酸,蒸发浓缩、冷却结晶得到 ;加热
;加热 和
和 的混合物得到无水
的混合物得到无水 ,该化学方程式为
,该化学方程式为 固体替代
固体替代 ,
, 的作用是
的作用是(4)1828年德国化学家维勒用金属钾还原熔融的氯化铍而得到
 。若将这个反应设计成原电池,则在电池的
。若将这个反应设计成原电池,则在电池的(5)铍和铝的化学性质相似,下列叙述错误的是
A.铍是一种轻金属,能与冷水反应
B.常温下,BeCl2溶液的pH<7
C.氧化铍的熔点高、耐酸碱腐蚀
您最近一年使用:0次
2024·陕西榆林·三模
名校
3 .  (三氯化六氨合钴,
(三氯化六氨合钴,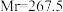 )是合成其他含钴配合物的重要原料,实验室中可由金属钴及其他原料制备
)是合成其他含钴配合物的重要原料,实验室中可由金属钴及其他原料制备 。
。
已知:①在 时,
时, 恰好完全沉淀为
恰好完全沉淀为 ;
;
②不同温度下 在水中的溶解度如图所示;
在水中的溶解度如图所示; 易潮解,Co(Ⅲ)的氧化性强于
易潮解,Co(Ⅲ)的氧化性强于 。
。
制备步骤如下:
Ⅰ. 的制备:用金属钴与氯气反应制备
的制备:用金属钴与氯气反应制备 ,实验中利用如图装置(连接处橡胶管省略)进行制备。
,实验中利用如图装置(连接处橡胶管省略)进行制备。 锥形瓶内加入
锥形瓶内加入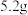 研细的
研细的 、
、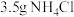 和
和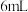 水,加热溶解后加入
水,加热溶解后加入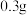 活性炭作催化剂。
活性炭作催化剂。
Ⅲ.冷却后,加入浓氨水混合均匀。控制温度在10℃以下并缓慢加入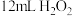 溶液。
溶液。
Ⅳ.在60℃下反应一段时间后,经过___________、过滤、洗涤、干燥等操作,得到橙黄色的 晶体
晶体 。
。
请回答下列问题:
(1)仪器a的名称为___________ 。
(2)用图中的装置组合制备 ,仪器的连接顺序为
,仪器的连接顺序为___________ 。装置B的作用是___________ 。
(3)制备三氯化六氨合钴的反应方程式为___________ 。
(4)在制备 时,加入浓氨水前,需在步骤Ⅱ中加入
时,加入浓氨水前,需在步骤Ⅱ中加入 ,请结合平衡移动原理解释原因
,请结合平衡移动原理解释原因___________ 。
(5)步骤Ⅲ中在加入 溶液时,控制温度在10℃以下缓慢加入的目的是
溶液时,控制温度在10℃以下缓慢加入的目的是___________ 。
(6)在步骤Ⅳ中过滤、洗涤、干燥之前的操作为___________ 、___________ 。
(7)制得 产品的产率为
产品的产率为___________ %(精确到0.1%)。
 (三氯化六氨合钴,
(三氯化六氨合钴,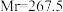 )是合成其他含钴配合物的重要原料,实验室中可由金属钴及其他原料制备
)是合成其他含钴配合物的重要原料,实验室中可由金属钴及其他原料制备 。
。已知:①在
 时,
时, 恰好完全沉淀为
恰好完全沉淀为 ;
;②不同温度下
 在水中的溶解度如图所示;
在水中的溶解度如图所示;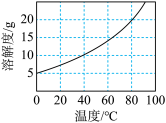
 易潮解,Co(Ⅲ)的氧化性强于
易潮解,Co(Ⅲ)的氧化性强于 。
。制备步骤如下:
Ⅰ.
 的制备:用金属钴与氯气反应制备
的制备:用金属钴与氯气反应制备 ,实验中利用如图装置(连接处橡胶管省略)进行制备。
,实验中利用如图装置(连接处橡胶管省略)进行制备。
 锥形瓶内加入
锥形瓶内加入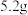 研细的
研细的 、
、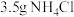 和
和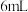 水,加热溶解后加入
水,加热溶解后加入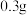 活性炭作催化剂。
活性炭作催化剂。Ⅲ.冷却后,加入浓氨水混合均匀。控制温度在10℃以下并缓慢加入
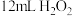 溶液。
溶液。Ⅳ.在60℃下反应一段时间后,经过___________、过滤、洗涤、干燥等操作,得到橙黄色的
 晶体
晶体 。
。请回答下列问题:
(1)仪器a的名称为
(2)用图中的装置组合制备
 ,仪器的连接顺序为
,仪器的连接顺序为(3)制备三氯化六氨合钴的反应方程式为
(4)在制备
 时,加入浓氨水前,需在步骤Ⅱ中加入
时,加入浓氨水前,需在步骤Ⅱ中加入 ,请结合平衡移动原理解释原因
,请结合平衡移动原理解释原因(5)步骤Ⅲ中在加入
 溶液时,控制温度在10℃以下缓慢加入的目的是
溶液时,控制温度在10℃以下缓慢加入的目的是(6)在步骤Ⅳ中过滤、洗涤、干燥之前的操作为
(7)制得
 产品的产率为
产品的产率为
您最近一年使用:0次
4 . 亚氯酸钠是一种高效漂白剂和氧化剂,常用于纸浆和纤维的漂白、饮水净化和污水处理等。温度高于60℃时, 会分解成
会分解成 和NaCl。某化学实验探究小组设计如图实验制备亚氯酸钠(
和NaCl。某化学实验探究小组设计如图实验制备亚氯酸钠( )晶体。
)晶体。
①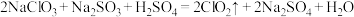 。
。
② 极易溶于水而不与水反应,几乎不发生水解,沸点11℃。
极易溶于水而不与水反应,几乎不发生水解,沸点11℃。
③ 饱和溶液在低于38℃时析出
饱和溶液在低于38℃时析出 ,高于38℃时析出
,高于38℃时析出 。
。
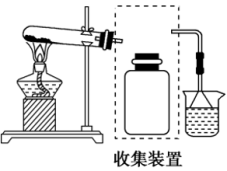
(1)C装置仪器名称是___________ ,它的作用是___________ 。
(2)B中使用浓硫酸而不用稀硫酸的原因是___________ 。
(3)向B中加入浓硫酸的操作方法是___________ 。
(4) 气体与装置D中混合溶液反应生成
气体与装置D中混合溶液反应生成 ,生成
,生成 的离子方程式为
的离子方程式为___________ 。
(5)反应后,经___________ 等步骤可从装置D的溶液获得 晶体。干燥时通常要求低温晾干,温度过高可能导致产品中混有的杂质是
晶体。干燥时通常要求低温晾干,温度过高可能导致产品中混有的杂质是___________ 。
(6)测定样品中 的纯度(假设杂质不参与反应)。测定时进行如下实验:准确称取0.200 g的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生反应:
的纯度(假设杂质不参与反应)。测定时进行如下实验:准确称取0.200 g的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生反应: ,将所得混合液稀释成100 mL待测溶液。取25.00 mL待测溶液,加入淀粉溶液做指示剂,用0.1 mol⋅L
,将所得混合液稀释成100 mL待测溶液。取25.00 mL待测溶液,加入淀粉溶液做指示剂,用0.1 mol⋅L
 标准液滴定至终点,测得消耗标准溶液体积的平均值为20.00 mL(已知:
标准液滴定至终点,测得消耗标准溶液体积的平均值为20.00 mL(已知: )。
)。
所称取的样品中 的质量分数为
的质量分数为___________ 。
 会分解成
会分解成 和NaCl。某化学实验探究小组设计如图实验制备亚氯酸钠(
和NaCl。某化学实验探究小组设计如图实验制备亚氯酸钠( )晶体。
)晶体。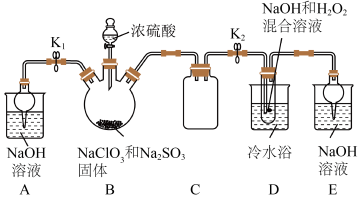
①
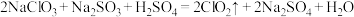 。
。②
 极易溶于水而不与水反应,几乎不发生水解,沸点11℃。
极易溶于水而不与水反应,几乎不发生水解,沸点11℃。③
 饱和溶液在低于38℃时析出
饱和溶液在低于38℃时析出 ,高于38℃时析出
,高于38℃时析出 。
。(1)C装置仪器名称是
(2)B中使用浓硫酸而不用稀硫酸的原因是
(3)向B中加入浓硫酸的操作方法是
(4)
 气体与装置D中混合溶液反应生成
气体与装置D中混合溶液反应生成 ,生成
,生成 的离子方程式为
的离子方程式为(5)反应后,经
 晶体。干燥时通常要求低温晾干,温度过高可能导致产品中混有的杂质是
晶体。干燥时通常要求低温晾干,温度过高可能导致产品中混有的杂质是(6)测定样品中
 的纯度(假设杂质不参与反应)。测定时进行如下实验:准确称取0.200 g的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生反应:
的纯度(假设杂质不参与反应)。测定时进行如下实验:准确称取0.200 g的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生反应: ,将所得混合液稀释成100 mL待测溶液。取25.00 mL待测溶液,加入淀粉溶液做指示剂,用0.1 mol⋅L
,将所得混合液稀释成100 mL待测溶液。取25.00 mL待测溶液,加入淀粉溶液做指示剂,用0.1 mol⋅L
 标准液滴定至终点,测得消耗标准溶液体积的平均值为20.00 mL(已知:
标准液滴定至终点,测得消耗标准溶液体积的平均值为20.00 mL(已知: )。
)。所称取的样品中
 的质量分数为
的质量分数为
您最近一年使用:0次
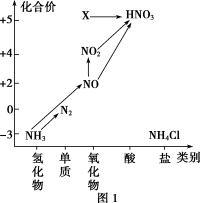
5 . 依据下图中氮元素及其化合物的转化关系,回答下列问题:_______ 。
(2)若要收集一瓶氨,请将下列装置补充完整,在虚框内画出连接图_______ 。_______ 。
A.浓硫酸 B.碱石灰 C.NaOH固体
(4)工业上以NH3、空气、水为原料生产硝酸分为三步:
①NH3→NO:化学方程式为_______ 。
②NO→NO2:实验现象是_______ 。
③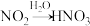 :氧化剂与还原剂的物质的量之比为
:氧化剂与还原剂的物质的量之比为_______ 。
(5)图1中,只用一种物质将NO直接转化为硝酸且绿色环保,则该物质的化学式为_______ 。
(6)图1中,X的化学式为_______ ,从物质性质上看,X属于_______ 氧化物。
(2)若要收集一瓶氨,请将下列装置补充完整,在虚框内画出连接图
A.浓硫酸 B.碱石灰 C.NaOH固体
(4)工业上以NH3、空气、水为原料生产硝酸分为三步:
①NH3→NO:化学方程式为
②NO→NO2:实验现象是
③
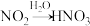 :氧化剂与还原剂的物质的量之比为
:氧化剂与还原剂的物质的量之比为(5)图1中,只用一种物质将NO直接转化为硝酸且绿色环保,则该物质的化学式为
(6)图1中,X的化学式为
您最近一年使用:0次
6 .  (钒酸铋)是一种黄色颜料。某小组以辉铋矿(含77.1%
(钒酸铋)是一种黄色颜料。某小组以辉铋矿(含77.1% 、19.5%Fe和3.4%
、19.5%Fe和3.4% )为原料制备钒酸铋,并回收
)为原料制备钒酸铋,并回收 制备食品抗氧化剂
制备食品抗氧化剂 的流程如下:
的流程如下: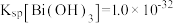 ,
,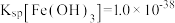 ;当金属离子浓度
;当金属离子浓度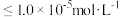 时,认为该离子已沉淀完全。请回答下列问题:
时,认为该离子已沉淀完全。请回答下列问题:
(1)“焙烧”中采用高压空气的目的是_______ , 转化成
转化成 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
(2)浸渣的主要成分是_______ (填化学式)。
(3)“酸浸”得到的浸液中 ,则“除铁”调节pH的范围为
,则“除铁”调节pH的范围为_______ 。
(4)“合成”过程中将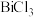 溶液和
溶液和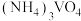 溶液混合容易形成
溶液混合容易形成 胶体,导致过滤困难。为防止生成胶体可采用的措施为
胶体,导致过滤困难。为防止生成胶体可采用的措施为_______ (答一条)。
(5)向饱和碳酸钠溶液中通入过量 可制得
可制得 ,发生反应的化学方程式为
,发生反应的化学方程式为_______ 。 易变质生成
易变质生成 ,设计简单实验证明产品是否变质:
,设计简单实验证明产品是否变质:_______ 。(已知: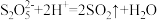 )
)
(6)某工厂用20吨该辉铋矿,最终得到18.468吨 ,则该过程中Bi的损耗率为
,则该过程中Bi的损耗率为______ %。
 (钒酸铋)是一种黄色颜料。某小组以辉铋矿(含77.1%
(钒酸铋)是一种黄色颜料。某小组以辉铋矿(含77.1% 、19.5%Fe和3.4%
、19.5%Fe和3.4% )为原料制备钒酸铋,并回收
)为原料制备钒酸铋,并回收 制备食品抗氧化剂
制备食品抗氧化剂 的流程如下:
的流程如下:
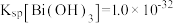 ,
,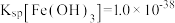 ;当金属离子浓度
;当金属离子浓度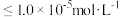 时,认为该离子已沉淀完全。请回答下列问题:
时,认为该离子已沉淀完全。请回答下列问题:(1)“焙烧”中采用高压空气的目的是
 转化成
转化成 发生反应的化学方程式为
发生反应的化学方程式为(2)浸渣的主要成分是
(3)“酸浸”得到的浸液中
 ,则“除铁”调节pH的范围为
,则“除铁”调节pH的范围为(4)“合成”过程中将
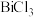 溶液和
溶液和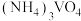 溶液混合容易形成
溶液混合容易形成 胶体,导致过滤困难。为防止生成胶体可采用的措施为
胶体,导致过滤困难。为防止生成胶体可采用的措施为(5)向饱和碳酸钠溶液中通入过量
 可制得
可制得 ,发生反应的化学方程式为
,发生反应的化学方程式为 易变质生成
易变质生成 ,设计简单实验证明产品是否变质:
,设计简单实验证明产品是否变质: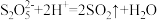 )
)(6)某工厂用20吨该辉铋矿,最终得到18.468吨
 ,则该过程中Bi的损耗率为
,则该过程中Bi的损耗率为
您最近一年使用:0次
名校
7 . 为测定草酸钴晶体(CoC2O4·2H2O)样品的纯度,某实验小组进行如下实验:
Ⅰ.取草酸钴晶体样品3.000 g,加稀H2SO4溶解,再加入100.00 mL 0.1000 mol/L酸性KMnO4溶液,充分反应至不再有CO2气体产生(常温下,草酸钴晶体难溶于水,该条件下Co2+不被氧化,杂质也不参与反应)。
Ⅱ.将溶液冷却,加水稀释定容至250 mL。
Ⅲ.取25.00 mL溶液,用0.1000 mol/L FeSO4标准溶液滴定。
Ⅳ.再重复步骤Ⅲ中的实验过程两次,三次的实验数据如表:
(1)步骤Ⅰ中加酸性KMnO4溶液时发生反应的离子方程式为______________ 。
(2)实验室使用的酸性KMnO4溶液一般是用________ 酸化(填酸的化学式)。
(3)步骤Ⅱ中,不会用到下列仪器中的_______ (填标号)。_______ (填“酸式”或“碱式”)滴定管;某次滴定中,开始时滴定管读数正确,结束时仰视,则所测草酸钴晶体样品的纯度会_______ (填“偏大”“偏小”或“不变”)﹔某次实验中所有实验操作和读数均无误,所测草酸钴晶体样品的纯度的误差却偏小,则可能的原因是___________ 。
(5)草酸钴晶体样品的纯度为______ %。
Ⅰ.取草酸钴晶体样品3.000 g,加稀H2SO4溶解,再加入100.00 mL 0.1000 mol/L酸性KMnO4溶液,充分反应至不再有CO2气体产生(常温下,草酸钴晶体难溶于水,该条件下Co2+不被氧化,杂质也不参与反应)。
Ⅱ.将溶液冷却,加水稀释定容至250 mL。
Ⅲ.取25.00 mL溶液,用0.1000 mol/L FeSO4标准溶液滴定。
Ⅳ.再重复步骤Ⅲ中的实验过程两次,三次的实验数据如表:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗FeSO4溶液标准的体积/mL | 18.96 | 18.03 | 17.97 |
(1)步骤Ⅰ中加酸性KMnO4溶液时发生反应的离子方程式为
(2)实验室使用的酸性KMnO4溶液一般是用
(3)步骤Ⅱ中,不会用到下列仪器中的
a.  b.
b.  c.
c.  d.
d.
(5)草酸钴晶体样品的纯度为
您最近一年使用:0次
名校
解题方法
8 . 钛白粉(纳米级 )广泛用作功能陶瓷、催化剂、化妆品和光敏材料等白色无机颜料,是白色颜料中着色力最强的一种,具有优良的遮盖力和着色牢度,适用于不透明的白色制品。以钛铁矿(主要成分为
)广泛用作功能陶瓷、催化剂、化妆品和光敏材料等白色无机颜料,是白色颜料中着色力最强的一种,具有优良的遮盖力和着色牢度,适用于不透明的白色制品。以钛铁矿(主要成分为 、MgO)为原料制备高纯度钛白粉,同时得到绿矾的工艺流程如图。
、MgO)为原料制备高纯度钛白粉,同时得到绿矾的工艺流程如图。 不反应。钛元素在整个流程中化合价没有变化。
不反应。钛元素在整个流程中化合价没有变化。
(1)稀硫酸浸出的目的是_______ 。
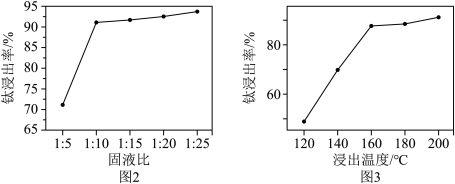
(2)下图分别为不同固液比、温度下滤渣与热浓硫酸反应时的Ti浸出率,据图分析,最适合的固液比和温度分别是_______ 、_______ 。 ,则浓硫酸与
,则浓硫酸与 反应的化学方程式为
反应的化学方程式为_______ 。
(4)“一系列操作”包括_______ ,过滤,洗涤,干燥。得到的绿矾先用稀钛液洗涤,再用冰水洗涤。用冰水洗涤的优点是_______ 。
(5)将钛液加热煮沸的目的是_______ 。
(6)若取10kg钛铁矿( 的质量分数为95%,)经过上述流程(钛元素在整个流程中损失率为5%),则可制得钛白粉固体的质量为
的质量分数为95%,)经过上述流程(钛元素在整个流程中损失率为5%),则可制得钛白粉固体的质量为_______ kg。
 )广泛用作功能陶瓷、催化剂、化妆品和光敏材料等白色无机颜料,是白色颜料中着色力最强的一种,具有优良的遮盖力和着色牢度,适用于不透明的白色制品。以钛铁矿(主要成分为
)广泛用作功能陶瓷、催化剂、化妆品和光敏材料等白色无机颜料,是白色颜料中着色力最强的一种,具有优良的遮盖力和着色牢度,适用于不透明的白色制品。以钛铁矿(主要成分为 、MgO)为原料制备高纯度钛白粉,同时得到绿矾的工艺流程如图。
、MgO)为原料制备高纯度钛白粉,同时得到绿矾的工艺流程如图。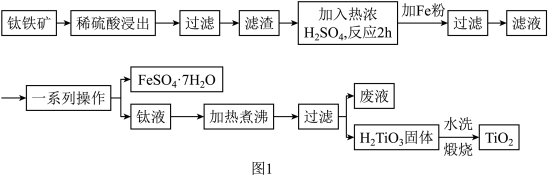
 不反应。钛元素在整个流程中化合价没有变化。
不反应。钛元素在整个流程中化合价没有变化。(1)稀硫酸浸出的目的是
(2)下图分别为不同固液比、温度下滤渣与热浓硫酸反应时的Ti浸出率,据图分析,最适合的固液比和温度分别是
 ,则浓硫酸与
,则浓硫酸与 反应的化学方程式为
反应的化学方程式为(4)“一系列操作”包括
(5)将钛液加热煮沸的目的是
(6)若取10kg钛铁矿(
 的质量分数为95%,)经过上述流程(钛元素在整个流程中损失率为5%),则可制得钛白粉固体的质量为
的质量分数为95%,)经过上述流程(钛元素在整个流程中损失率为5%),则可制得钛白粉固体的质量为
您最近一年使用:0次
9 . 铜(Ⅰ)配合物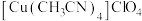 的制备及纯度分析步骤如下。
的制备及纯度分析步骤如下。
1.制备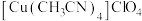
将乙腈的 ,
, ,过量钢材混合于圆底烧瓶,控温85°C、磁力搅拌,至反应完全(装置如图),经一系列操作,得到白色固体产品。
,过量钢材混合于圆底烧瓶,控温85°C、磁力搅拌,至反应完全(装置如图),经一系列操作,得到白色固体产品。
取 产品完全溶解于足量浓硝酸中,再加水、醋酸钠溶液配成250.0mL溶液。取25.0mL溶液,加入指示剂后,再用
产品完全溶解于足量浓硝酸中,再加水、醋酸钠溶液配成250.0mL溶液。取25.0mL溶液,加入指示剂后,再用 EDTA标准溶液滴定至终点。平行滴定三次,消耗EDTA溶液的平均体积为
EDTA标准溶液滴定至终点。平行滴定三次,消耗EDTA溶液的平均体积为 。
。
已知:① 沸点为81℃.酸性条件下遇水生成
沸点为81℃.酸性条件下遇水生成
②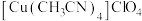 (
(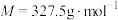 )较易被空气氧化:
)较易被空气氧化:
③EDTA与 形成1:1配合物:
形成1:1配合物:
④滴定需在弱碱性条件下进行。
回答下列问题:
(1)图中仪器 的作用是
的作用是______ , 中应加入
中应加入______ 作为最佳传热介质。
(2)加入过量铜粉能提高产物的纯度,可能的原因是______ .
(3)“一系列操作”依次为过滤分离出滤液、______ 冷却结晶、过滤、洗涤、干燥。
(4) 与足量浓硝酸发生反应的离子方程式为
与足量浓硝酸发生反应的离子方程式为______ .
(5)加入醋酸钠溶液的主要目的是______ .
(6)测得产品的纯度为______ (用含 、
、 、
、 的代数式表示)。
的代数式表示)。
(7)下列情况会导致产品纯度测定结果偏高的有______.
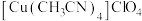 的制备及纯度分析步骤如下。
的制备及纯度分析步骤如下。1.制备
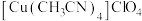
将乙腈的
 ,
, ,过量钢材混合于圆底烧瓶,控温85°C、磁力搅拌,至反应完全(装置如图),经一系列操作,得到白色固体产品。
,过量钢材混合于圆底烧瓶,控温85°C、磁力搅拌,至反应完全(装置如图),经一系列操作,得到白色固体产品。
取
 产品完全溶解于足量浓硝酸中,再加水、醋酸钠溶液配成250.0mL溶液。取25.0mL溶液,加入指示剂后,再用
产品完全溶解于足量浓硝酸中,再加水、醋酸钠溶液配成250.0mL溶液。取25.0mL溶液,加入指示剂后,再用 EDTA标准溶液滴定至终点。平行滴定三次,消耗EDTA溶液的平均体积为
EDTA标准溶液滴定至终点。平行滴定三次,消耗EDTA溶液的平均体积为 。
。已知:①
 沸点为81℃.酸性条件下遇水生成
沸点为81℃.酸性条件下遇水生成
②
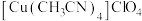 (
(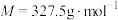 )较易被空气氧化:
)较易被空气氧化:③EDTA与
 形成1:1配合物:
形成1:1配合物:④滴定需在弱碱性条件下进行。
回答下列问题:
(1)图中仪器
 的作用是
的作用是 中应加入
中应加入(2)加入过量铜粉能提高产物的纯度,可能的原因是
(3)“一系列操作”依次为过滤分离出滤液、
(4)
 与足量浓硝酸发生反应的离子方程式为
与足量浓硝酸发生反应的离子方程式为(5)加入醋酸钠溶液的主要目的是
(6)测得产品的纯度为
 、
、 、
、 的代数式表示)。
的代数式表示)。(7)下列情况会导致产品纯度测定结果偏高的有______.
A.产品中含有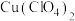 | B.滴定终点时俯视读数 |
| C.盛装EDTA溶液的滴定管未润洗 | D.产品干燥不充分 |
您最近一年使用:0次
10 . 钛酸钡( )因其优良的电学性能被广泛应用于多层陶瓷电容器(MLCC)等电子元器件。某同学以
)因其优良的电学性能被广泛应用于多层陶瓷电容器(MLCC)等电子元器件。某同学以 和高活性偏钛酸(
和高活性偏钛酸( )为原料,在实验室中采用低温固相法制备亚微米级钛酸钡粉体。
)为原料,在实验室中采用低温固相法制备亚微米级钛酸钡粉体。
已知:①氧化性: ;
; 。
。
②四氯化钛极易水解,易挥发。
I.制备偏钛酸(装置如图) 固体于三颈烧瓶中,加入浓盐酸配成
固体于三颈烧瓶中,加入浓盐酸配成 溶液,然后加水稀释转化成一定浓度的
溶液,然后加水稀释转化成一定浓度的 溶液,最后将装在仪器B中的氨水缓慢滴入
溶液,最后将装在仪器B中的氨水缓慢滴入 溶液中,搅拌,析出
溶液中,搅拌,析出 。反应过程中注意控制温度,以免反应过于剧烈。
。反应过程中注意控制温度,以免反应过于剧烈。
(1)仪器B的名称是_______ 。
(2)仪器A的作用是_______ ,冷凝水从_______ (填“a”或“b”)口通入。
(3)写出氨水与 溶液反应产生
溶液反应产生 的化学方程式
的化学方程式_______ 。
Ⅱ.制备钛酸钡
将上述制得的作为反应原料,与按照物质的量之比为 混合后放入球磨罐中,放置于“罐磨机”上按照700r/min罐磨5h后倒入坩埚中,并置于烘箱中
混合后放入球磨罐中,放置于“罐磨机”上按照700r/min罐磨5h后倒入坩埚中,并置于烘箱中 反应3h,得到亚微米级白色钛酸钡样品粉体。
反应3h,得到亚微米级白色钛酸钡样品粉体。
(4)写出 与
与 反应的化学方程式
反应的化学方程式_______ 。
(5)在固相反应过程中,会经历“接触扩散—化学反应—成核—晶粒生长”的历程,则“罐磨机”的作用是_______ ,若想获得比亚微米级钛酸钡晶体更大颗粒的晶体,应置于_______ (填“<”或“>”)100℃的烘箱中反应3h。
Ⅲ.测定产品纯度
取 产品溶于稍过量的稀硫酸中配制成250mL溶液,取25.00mL溶液于锥形瓶中,加入过量
产品溶于稍过量的稀硫酸中配制成250mL溶液,取25.00mL溶液于锥形瓶中,加入过量 溶液,充分反应后,用
溶液,充分反应后,用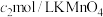 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 。(
。( 的摩尔质量为Mg/mol)
的摩尔质量为Mg/mol)
(6)实验中所用滴定管为_______ (填“酸式”或“碱式”或“酸式和碱式”)滴定管。
(7)产品的纯度为_______ %。
 )因其优良的电学性能被广泛应用于多层陶瓷电容器(MLCC)等电子元器件。某同学以
)因其优良的电学性能被广泛应用于多层陶瓷电容器(MLCC)等电子元器件。某同学以 和高活性偏钛酸(
和高活性偏钛酸( )为原料,在实验室中采用低温固相法制备亚微米级钛酸钡粉体。
)为原料,在实验室中采用低温固相法制备亚微米级钛酸钡粉体。已知:①氧化性:
 ;
; 。
。②四氯化钛极易水解,易挥发。
I.制备偏钛酸(装置如图)

 固体于三颈烧瓶中,加入浓盐酸配成
固体于三颈烧瓶中,加入浓盐酸配成 溶液,然后加水稀释转化成一定浓度的
溶液,然后加水稀释转化成一定浓度的 溶液,最后将装在仪器B中的氨水缓慢滴入
溶液,最后将装在仪器B中的氨水缓慢滴入 溶液中,搅拌,析出
溶液中,搅拌,析出 。反应过程中注意控制温度,以免反应过于剧烈。
。反应过程中注意控制温度,以免反应过于剧烈。(1)仪器B的名称是
(2)仪器A的作用是
(3)写出氨水与
 溶液反应产生
溶液反应产生 的化学方程式
的化学方程式Ⅱ.制备钛酸钡
将上述制得的作为反应原料,与按照物质的量之比为
 混合后放入球磨罐中,放置于“罐磨机”上按照700r/min罐磨5h后倒入坩埚中,并置于烘箱中
混合后放入球磨罐中,放置于“罐磨机”上按照700r/min罐磨5h后倒入坩埚中,并置于烘箱中 反应3h,得到亚微米级白色钛酸钡样品粉体。
反应3h,得到亚微米级白色钛酸钡样品粉体。(4)写出
 与
与 反应的化学方程式
反应的化学方程式(5)在固相反应过程中,会经历“接触扩散—化学反应—成核—晶粒生长”的历程,则“罐磨机”的作用是
Ⅲ.测定产品纯度
取
 产品溶于稍过量的稀硫酸中配制成250mL溶液,取25.00mL溶液于锥形瓶中,加入过量
产品溶于稍过量的稀硫酸中配制成250mL溶液,取25.00mL溶液于锥形瓶中,加入过量 溶液,充分反应后,用
溶液,充分反应后,用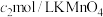 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 。(
。( 的摩尔质量为Mg/mol)
的摩尔质量为Mg/mol)(6)实验中所用滴定管为
(7)产品的纯度为
您最近一年使用:0次



