名校
1 . 某工业废催化剂主要成份为: 和
和 ,还有少量的
,还有少量的 和FeO,利用该废催化剂回收Cr和V的简化工业流程如下图所示:
和FeO,利用该废催化剂回收Cr和V的简化工业流程如下图所示:_______ (填化学式)。
(2)水浸渣的主要成份是_______ (填化学式)。
(3)“沉淀”的化学式_______ 。生成该沉淀的化学方程式_______ 。
(4)“沉钒”中需要加入过量的浓 ,结合离子方程式说明原因是
,结合离子方程式说明原因是_______ 。写出生成 的化学方程式
的化学方程式_______ 。
(5)淀粉水解液中_______ (填化学式)起还原作用,用焦亚硫酸钠( )溶液代替淀粉水解液效果相同,写出反应的离子方程式
)溶液代替淀粉水解液效果相同,写出反应的离子方程式_______ 。
(6)利用生物燃料电池原理研究室温下氨的合成,电池工作时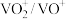 在电极与酶之间传递电子,示意图如图所示。
在电极与酶之间传递电子,示意图如图所示。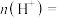
_______ mol。
 和
和 ,还有少量的
,还有少量的 和FeO,利用该废催化剂回收Cr和V的简化工业流程如下图所示:
和FeO,利用该废催化剂回收Cr和V的简化工业流程如下图所示: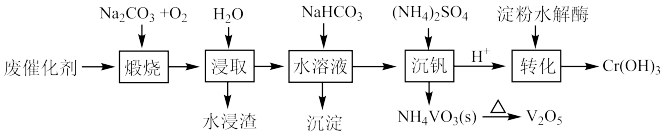
(2)水浸渣的主要成份是
(3)“沉淀”的化学式
(4)“沉钒”中需要加入过量的浓
 ,结合离子方程式说明原因是
,结合离子方程式说明原因是 的化学方程式
的化学方程式(5)淀粉水解液中
 )溶液代替淀粉水解液效果相同,写出反应的离子方程式
)溶液代替淀粉水解液效果相同,写出反应的离子方程式(6)利用生物燃料电池原理研究室温下氨的合成,电池工作时
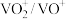 在电极与酶之间传递电子,示意图如图所示。
在电极与酶之间传递电子,示意图如图所示。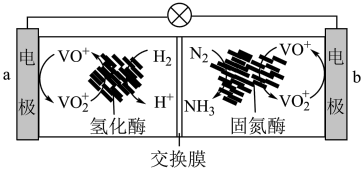
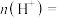
您最近一年使用:0次
名校
解题方法
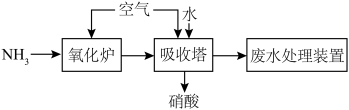
2 . I.氨催化氧化制硝酸的流程示意图如下。___________ 。
(2)“吸收塔”中生成硝酸的化学方程式为___________ 。(写出一个即可)
(3)为避免硝酸工业废气中 污染环境,常用NaOH溶液吸收,其反应原理如下:
污染环境,常用NaOH溶液吸收,其反应原理如下:
①
②
现有一定条件下0.5mo1 和0.1mol NO的混合气体恰好被300mL NaOH溶液完全吸收,则NaOH溶液的物质的量浓度为
和0.1mol NO的混合气体恰好被300mL NaOH溶液完全吸收,则NaOH溶液的物质的量浓度为___________ mol/L。
Ⅱ.研究炼油、钢铁等工业,上高浓度氨氮废水的处理,流程如下: 与NaOH溶液反应的离子方程式
与NaOH溶液反应的离子方程式___________ 。
(5)过程②:在微生物的作用下实现 ,转化、称为硝化过程。硝化过程需加入的物质可以为
,转化、称为硝化过程。硝化过程需加入的物质可以为___________ 。(填相应的字母)
A. B.
B. C.
C.
(6)过程③:在一定条件下向废水中加入甲醇( ),实现
),实现 转化,称为反硝化过程。将含硝酸废水中的
转化,称为反硝化过程。将含硝酸废水中的 进行反硝化转化过程中,当收集到11.2L
进行反硝化转化过程中,当收集到11.2L  (标况)时,转移电子的总数为
(标况)时,转移电子的总数为___________ 。
(2)“吸收塔”中生成硝酸的化学方程式为
(3)为避免硝酸工业废气中
 污染环境,常用NaOH溶液吸收,其反应原理如下:
污染环境,常用NaOH溶液吸收,其反应原理如下:①

②

现有一定条件下0.5mo1
 和0.1mol NO的混合气体恰好被300mL NaOH溶液完全吸收,则NaOH溶液的物质的量浓度为
和0.1mol NO的混合气体恰好被300mL NaOH溶液完全吸收,则NaOH溶液的物质的量浓度为Ⅱ.研究炼油、钢铁等工业,上高浓度氨氮废水的处理,流程如下:

 与NaOH溶液反应的离子方程式
与NaOH溶液反应的离子方程式(5)过程②:在微生物的作用下实现
 ,转化、称为硝化过程。硝化过程需加入的物质可以为
,转化、称为硝化过程。硝化过程需加入的物质可以为A.
 B.
B. C.
C.
(6)过程③:在一定条件下向废水中加入甲醇(
 ),实现
),实现 转化,称为反硝化过程。将含硝酸废水中的
转化,称为反硝化过程。将含硝酸废水中的 进行反硝化转化过程中,当收集到11.2L
进行反硝化转化过程中,当收集到11.2L  (标况)时,转移电子的总数为
(标况)时,转移电子的总数为
您最近一年使用:0次
名校
解题方法
3 . 工业上以辉铋矿粉(主要成分是 ,含少量
,含少量 、
、 、
、 等杂质)为原料制备
等杂质)为原料制备 (铋酸钠,浅黄色不溶于冷水的固体,是常用试剂),流程如下:
(铋酸钠,浅黄色不溶于冷水的固体,是常用试剂),流程如下: 难溶于水;
难溶于水;
②酸浸后,矿粉中的硫元素完全变为硫单质;
回答下列问题:
(1) 中Cu的化合价为
中Cu的化合价为___________ ,酸浸过程中, 反应的离子方程式
反应的离子方程式___________ 。
(2)检验“酸浸”液中是否含 ,可选择
,可选择 溶液。能证明不存在
溶液。能证明不存在 的实验现象是
的实验现象是___________ 。
(3)氧化后,从反应体系中分离出 粗产品的操作名称是
粗产品的操作名称是___________ 。
(4)上述流程中,基态原子未成对电子数最多的金属元素名称是___________ 。
(5)向 和
和 混合溶液中通入氯气制备
混合溶液中通入氯气制备 的离子方程式
的离子方程式___________ 。
(6)已知常温下, ,调节FeCl3溶液至
,调节FeCl3溶液至 ,所得溶液中c(Fe3+)=
,所得溶液中c(Fe3+)=___________ 。
 ,含少量
,含少量 、
、 、
、 等杂质)为原料制备
等杂质)为原料制备 (铋酸钠,浅黄色不溶于冷水的固体,是常用试剂),流程如下:
(铋酸钠,浅黄色不溶于冷水的固体,是常用试剂),流程如下: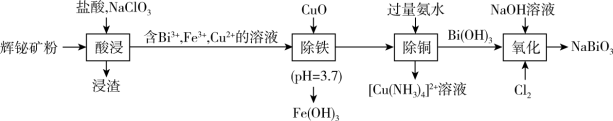
 难溶于水;
难溶于水;②酸浸后,矿粉中的硫元素完全变为硫单质;
回答下列问题:
(1)
 中Cu的化合价为
中Cu的化合价为 反应的离子方程式
反应的离子方程式(2)检验“酸浸”液中是否含
 ,可选择
,可选择 溶液。能证明不存在
溶液。能证明不存在 的实验现象是
的实验现象是(3)氧化后,从反应体系中分离出
 粗产品的操作名称是
粗产品的操作名称是(4)上述流程中,基态原子未成对电子数最多的金属元素名称是
(5)向
 和
和 混合溶液中通入氯气制备
混合溶液中通入氯气制备 的离子方程式
的离子方程式(6)已知常温下,
 ,调节FeCl3溶液至
,调节FeCl3溶液至 ,所得溶液中c(Fe3+)=
,所得溶液中c(Fe3+)=
您最近一年使用:0次
名校
解题方法
4 . 某课外活动小组在实验室制备氨气、验证氨气的某些性质。
Ⅰ.氨气的制备
(1)图中三套装置中能制备干燥NH3的装置和发生的化学方程式分别是____ 。_____ 。
(3)B中试剂为___________ ,NaOH溶液的作用是___________ 。
(4)控制氨气和氧气的比例是制备硝酸的关键。
①当比例不合适时,A中不仅有红棕色气体产生,还伴有白烟。红棕色气体的化学式是___________ ,白烟的化学式是___________ 。
②欲使氨气尽可能完全转化为硝酸,理论上n(NH3):n(O2)的最佳比例为___________ 。
Ⅰ.氨气的制备
(1)图中三套装置中能制备干燥NH3的装置和发生的化学方程式分别是


(3)B中试剂为
(4)控制氨气和氧气的比例是制备硝酸的关键。
①当比例不合适时,A中不仅有红棕色气体产生,还伴有白烟。红棕色气体的化学式是
②欲使氨气尽可能完全转化为硝酸,理论上n(NH3):n(O2)的最佳比例为
您最近一年使用:0次
名校
解题方法
5 . 叠氮化钠(NaN3)是一种无色晶体,易溶于水,微溶于乙醇,不溶于乙醚,广泛应用于汽车安全气囊。某硝酸工厂拟通过下列方法处理尾气并制备叠氮化钠。___________ 。
(2)已知NaN3阳离子与阴离子个数比为1:1,则NaN3中所含的化学键为___________ ,1mol该阴离子中所含的电子总数为___________ mol
(3)汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3 K2O+5Na2O+16N2↑。假定汽车中某个安全气囊容积为56L。
K2O+5Na2O+16N2↑。假定汽车中某个安全气囊容积为56L。
①该反应中的还原剂为___________ (填化学式)。
②欲使气囊中充满标准状况下氮气,则该安全气囊中生成的K2O和Na2O的总质量为多少克___________ ?(写出计算过程,保留一位小数,不考虑固体的体积)。
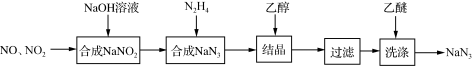
(2)已知NaN3阳离子与阴离子个数比为1:1,则NaN3中所含的化学键为
(3)汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3
 K2O+5Na2O+16N2↑。假定汽车中某个安全气囊容积为56L。
K2O+5Na2O+16N2↑。假定汽车中某个安全气囊容积为56L。①该反应中的还原剂为
②欲使气囊中充满标准状况下氮气,则该安全气囊中生成的K2O和Na2O的总质量为多少克
您最近一年使用:0次
名校
解题方法
6 . 以铁镍合金(含少量铜)为原料,生产电极材粗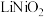 的部分工艺流程如下:
的部分工艺流程如下:

已知:常温下,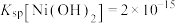 ,
,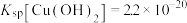 ,
,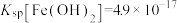 ,
,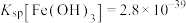 。
。
回答下列问题:
(1)基态Ni原子价层电子轨道表示式是_______ ;Cu原子位于周期表中_______ 区。
(2)“酸溶”时Ni转化为 ,该过程中温度控制在70~80℃的原因是
,该过程中温度控制在70~80℃的原因是_______ 。
(3)“氧化”时 的作用是(用离子方程式表示)
的作用是(用离子方程式表示)_______ 。
(4)“除铜”时若选用NaOH溶液,会导致部分 也产生沉淀,当常温时溶液中
也产生沉淀,当常温时溶液中 、
、 沉淀同时存在时,溶液中
沉淀同时存在时,溶液中
_______ 。
(5)“沉镍”时得到碳酸镍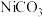 沉淀。在空气中碳酸镍与碳酸锂共同“煅烧”可制得
沉淀。在空气中碳酸镍与碳酸锂共同“煅烧”可制得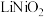 ,该反应的化学方程式是
,该反应的化学方程式是_______ 。
(6)金属镍的配合物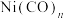 用途广泛,其中配体CO与
用途广泛,其中配体CO与 结构相似,CO分子内σ键与π键个数之比为
结构相似,CO分子内σ键与π键个数之比为_______ 。
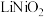 的部分工艺流程如下:
的部分工艺流程如下:
已知:常温下,
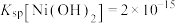 ,
,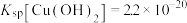 ,
,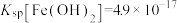 ,
,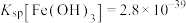 。
。回答下列问题:
(1)基态Ni原子价层电子轨道表示式是
(2)“酸溶”时Ni转化为
 ,该过程中温度控制在70~80℃的原因是
,该过程中温度控制在70~80℃的原因是(3)“氧化”时
 的作用是(用离子方程式表示)
的作用是(用离子方程式表示)(4)“除铜”时若选用NaOH溶液,会导致部分
 也产生沉淀,当常温时溶液中
也产生沉淀,当常温时溶液中 、
、 沉淀同时存在时,溶液中
沉淀同时存在时,溶液中
(5)“沉镍”时得到碳酸镍
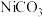 沉淀。在空气中碳酸镍与碳酸锂共同“煅烧”可制得
沉淀。在空气中碳酸镍与碳酸锂共同“煅烧”可制得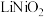 ,该反应的化学方程式是
,该反应的化学方程式是(6)金属镍的配合物
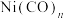 用途广泛,其中配体CO与
用途广泛,其中配体CO与 结构相似,CO分子内σ键与π键个数之比为
结构相似,CO分子内σ键与π键个数之比为
您最近一年使用:0次
名校
7 . 下列化学方程式或离子方程式书写正确的是
A.氨的催化氧化: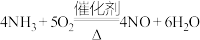 |
B.向 溶液中通入过量 溶液中通入过量 : : |
C.稀硝酸与过量的铁屑反应: |
D.向碳酸氢铵溶液中加入足量石灰水: |
您最近一年使用:0次
名校
8 . 氯化亚铜(CuCl)难溶于醇和水,在潮湿空气中易水解氧化,广泛应用于冶金工业,以铜为原料生产 的流程如下:
的流程如下:错误 的是
 的流程如下:
的流程如下: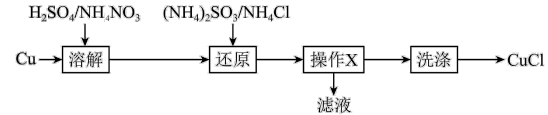
A.“溶解”时可能发生的反应: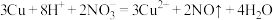 |
B.“还原”反应的氧化产物是 或 或 |
| C.“操作X”是过滤 |
| D.“洗涤”时先用硝酸洗,再用乙醇洗 |
您最近一年使用:0次
2024-03-14更新
|
523次组卷
|
4卷引用:陕西省西安市航天中学2023-2024学年高一下学期第一次月考化学试题
名校
解题方法
9 . 下列化学实验操作过程中的离子方程式书写正确的是
A.用酸性高锰酸钾溶液滴定草酸溶液: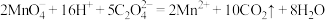 |
B.向 溶液中滴加过量氨水: 溶液中滴加过量氨水: |
C.用惰性电极电解 溶液: 溶液: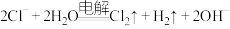 |
D.向 溶液中滴加过量溴水: 溶液中滴加过量溴水: |
您最近一年使用:0次
2024-03-08更新
|
157次组卷
|
3卷引用:陕西省西安工业大学附属中学2023-2024学年高三下学期3月月考理科综合试题-高中化学
名校
10 . 海水中有丰富的资源。从海水中可以获得淡水、食盐,并提取溴。回答下列问题。
(1)初步提纯后的粗盐中含有 、
、 、
、 等杂质,精制时一般步骤如下:
等杂质,精制时一般步骤如下:
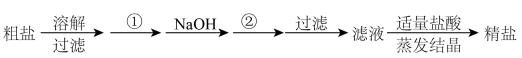
加入的试剂①、②分别是:___________ 、___________ 。
(2)工业上以晒盐后的卤水为原料进行提溴,主要流程如下:
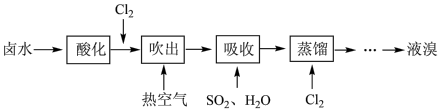
①卤水呈碱性,在通入 前需先酸化,原因是
前需先酸化,原因是___________ 。
②向酸化后的卤水中通入Cl2时主要发生反应的离子方程式为___________ 。
③“吹出”步骤中主要利用了溴的___________ 性。
④设立“吸收”步骤的目的是___________ 。
⑤吸收步骤中发生反应的化学方程式为___________ 。
⑥已知常压下 的沸点是59℃。蒸馏过程中,温度应控制在
的沸点是59℃。蒸馏过程中,温度应控制在___________ (填字母)范围内较合适。
a.20℃~30℃ B.45℃~55℃ C.75℃~85℃ D.100℃~110℃
⑦经该方法处理后, 海水最终得到
海水最终得到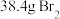 ,若总提取率为60%,则原海水中
,若总提取率为60%,则原海水中 的浓度是
的浓度是___________ 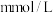 。
。
(1)初步提纯后的粗盐中含有
 、
、 、
、 等杂质,精制时一般步骤如下:
等杂质,精制时一般步骤如下:
加入的试剂①、②分别是:
(2)工业上以晒盐后的卤水为原料进行提溴,主要流程如下:

①卤水呈碱性,在通入
 前需先酸化,原因是
前需先酸化,原因是②向酸化后的卤水中通入Cl2时主要发生反应的离子方程式为
③“吹出”步骤中主要利用了溴的
④设立“吸收”步骤的目的是
⑤吸收步骤中发生反应的化学方程式为
⑥已知常压下
 的沸点是59℃。蒸馏过程中,温度应控制在
的沸点是59℃。蒸馏过程中,温度应控制在a.20℃~30℃ B.45℃~55℃ C.75℃~85℃ D.100℃~110℃
⑦经该方法处理后,
 海水最终得到
海水最终得到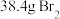 ,若总提取率为60%,则原海水中
,若总提取率为60%,则原海水中 的浓度是
的浓度是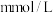 。
。
您最近一年使用:0次



