1 . 已知HNO2在低温下较稳定,酸性比醋酸略强,既有还原性又有氧化性,其氧化产物、还原产物与溶液pH的关系如下表。下列有关说法错误的是
| pH范围 | >7 | <7 |
| 产物 |  | NO、N2O、N2中的一种 |
A.碱性条件下,NaNO2与NaClO反应的离子方程式为 + ClO- = + ClO- = +Cl- +Cl- |
| B.向冷的NaNO2溶液中加入滴有淀粉的氢碘酸,若溶液变蓝色,则证明氧化性:HNO2>I2 |
| C.向冷的NaNO2溶液中通入SO2最终可得到HNO2 |
| D.低温时不用其他试剂即可区分HNO2溶液与Na2CO3溶液 |
您最近一年使用:0次
2022-01-22更新
|
132次组卷
|
2卷引用: 山西省太原市2021-2022学年高三上学期期末考试化学试题
名校
2 . 工业上由粗锰粉(主要杂质为Fe、Ni、Pb等金属单质)制备高纯碳酸锰。其主要工艺流程如图:
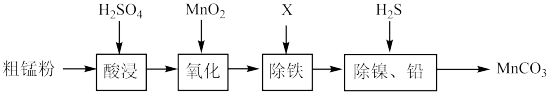
下列有关说法不正确 的是

下列有关说法
| A.可以通过搅拌的方式提高“酸浸”时粗锰粉的浸取率 |
| B.向酸浸后的滤液中加入MnO2,反应的离子方程式为:Mn4++2Fe2+=2Fe3++Mn2+ |
| C.除铁时加入的物质X作用是调节溶液的pH值,使Fe3+转化为Fe(OH)3沉淀而除去 |
| D.取除铁后的滤液,加入几滴KSCN溶液,无明显现象证明Fe3+已除尽 |
您最近一年使用:0次
2022-04-15更新
|
850次组卷
|
5卷引用:江苏省盐城市阜宁中学等四校2021-2022学年高一下学期期中考试化学试题
江苏省盐城市阜宁中学等四校2021-2022学年高一下学期期中考试化学试题江苏省海州高级中学2021-2022学年高一下学期期中考试化学试题(已下线)微专题17 热点金属及其化合物制备流程(V、Cr、Mn、Co、Ni)-备战2023年高考化学一轮复习考点微专题江苏省常熟市海虞高级中学2021-2022学年高一下学期线上期中考试化学试题(已下线)考点12 金属材料(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
名校
解题方法
3 . 以废旧铅蓄电池中的含铅废料( 、
、 、
、 、
、 及炭黑等)和
及炭黑等)和 为原料,可以制备高纯
为原料,可以制备高纯 ,实现铅的再生利用,其工艺流程如下:
,实现铅的再生利用,其工艺流程如下:
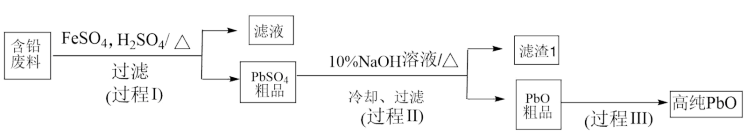
在过程Ⅰ涉及两个反应:
①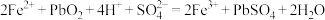 ;
;
②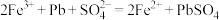 。下列说法错误的是
。下列说法错误的是
 、
、 、
、 、
、 及炭黑等)和
及炭黑等)和 为原料,可以制备高纯
为原料,可以制备高纯 ,实现铅的再生利用,其工艺流程如下:
,实现铅的再生利用,其工艺流程如下:
在过程Ⅰ涉及两个反应:
①
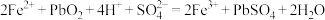 ;
;②
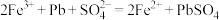 。下列说法错误的是
。下列说法错误的是A.在过程Ⅰ中, 起催化作用 起催化作用 |
B.在过程Ⅰ中生成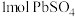 时,转移的电子数为 时,转移的电子数为 个 个 |
C.在过程Ⅰ中若改为加入 也能起到催化作用 也能起到催化作用 |
D.要证明过程Ⅰ中 起催化作用,加入 起催化作用,加入 溶液,溶液不变红色即可 溶液,溶液不变红色即可 |
您最近一年使用:0次
2022-01-20更新
|
149次组卷
|
4卷引用:湖南省湖湘名校联盟2021-2022学年高二上学期期末考试化学试题
名校
4 . 食盐中所加的碘以碘酸钾(KIO3)形式存在。根据反应:IO +I-+H+→I2+H2O(未配平),可用KI淀粉试纸和食醋进行实验,证明加碘食盐中存在IO
+I-+H+→I2+H2O(未配平),可用KI淀粉试纸和食醋进行实验,证明加碘食盐中存在IO 。下列说法不正确的是
。下列说法不正确的是
 +I-+H+→I2+H2O(未配平),可用KI淀粉试纸和食醋进行实验,证明加碘食盐中存在IO
+I-+H+→I2+H2O(未配平),可用KI淀粉试纸和食醋进行实验,证明加碘食盐中存在IO 。下列说法不正确的是
。下列说法不正确的是| A.上述反应中氧化剂和还原剂的物质的量之比为1∶5 |
| B.实验时可观察到试纸变蓝 |
| C.实验可证明该条件下I-的还原性强于Cl- |
| D.食醋中含有的乙酸是强酸,它能提供反应所需的H+ |
您最近一年使用:0次
2020-07-04更新
|
322次组卷
|
5卷引用:北京市东城区北京景山学校2019~2020学年高一下学期期末考试化学试题
北京市东城区北京景山学校2019~2020学年高一下学期期末考试化学试题贵州省铜仁市伟才学校2019-2020学年高一下学期期末考试化学(理)试题黑龙江省大庆市肇州县第二中学2019-2020学年高一下学期期末考试化学试题(已下线)1.3.4 氧化还原反应方程式的配平-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)江西省南昌市豫章中学20212-2022学年高一下学期第一次月考化学试题
名校
5 . 下列反应对应的离子方程式正确的是
A.乙酰胺与盐酸混合共热: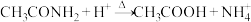 |
B.硫化钠溶液在空气中氧化变质: |
C.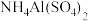 溶液与足量 溶液与足量 溶液反应: 溶液反应: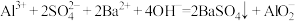 |
D.证明 、 、 、 、 三者的酸性强弱: 三者的酸性强弱: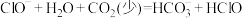 |
您最近一年使用:0次
2024-04-22更新
|
452次组卷
|
2卷引用:2024届河北省邢台市部分高中高三下学期二模化学试题
名校
6 . 能正确表示下列反应的离子方程式是
A.向 溶液中加过量 溶液中加过量 溶液: 溶液: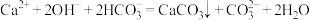 |
B.用酸性 溶液与 溶液与 反应,证明 反应,证明 具有还原性: 具有还原性: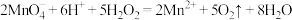 |
C.用铜做电极电解 溶液: 溶液: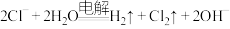 |
D.将 加入到足量 加入到足量 溶液中: 溶液中: |
您最近一年使用:0次
2023-05-04更新
|
150次组卷
|
2卷引用:湖北省部分重点中学2022-2023学年高三下学期2月质量检测化学试题
名校
7 . 常温下,在 溶液中滴加少量稀硝酸,溶液变为浅黄色。下列有关推断错误的是
溶液中滴加少量稀硝酸,溶液变为浅黄色。下列有关推断错误的是
 溶液中滴加少量稀硝酸,溶液变为浅黄色。下列有关推断错误的是
溶液中滴加少量稀硝酸,溶液变为浅黄色。下列有关推断错误的是A. 、 、 、 、 、 、 能大量共存 能大量共存 |
| B.在上述浅黄色溶液中滴加少量KSCN溶液,溶液为红色 |
C.在上述浅黄色溶液中滴加少量 溶液,紫色褪去,证明 溶液,紫色褪去,证明 有剩余 有剩余 |
D.在溶液中滴加稀硝酸反应的离子方程式: |
您最近一年使用:0次
解题方法
8 . 下列离子方程式正确 且符合题意的是
| A.向Ba (NO3)2溶液中通入SO2,产生白色沉淀,发生的离子反应为Ba2+ +SO2+H2O= BaSO3↓ +2H+ |
B.等体积、等物质的量浓度的Ba (OH) 2与NaHSO4溶液反应: Ba2+ +OH- +H++ - =BaSO4↓+H2O - =BaSO4↓+H2O |
C.向酸化的KMnO4溶液中加入少量Na2S,再滴加BaCl2溶液,产生白色沉淀,证明一定发生离子反应:8 +5S2- +24H+= 8Mn2++5 +5S2- +24H+= 8Mn2++5 +12H2O +12H2O |
| D.向FeI2溶液中滴加少量氯水,溶液变黄色: 2Fe2++Cl2= 2Fe3++2Cl- |
您最近一年使用:0次
名校
解题方法
9 . 已知氢化钠(NaH)可由氢气和钠在高温下化合形成,NaH遇水放出 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是A.取钠与氢气反应后的产物,加水若产生 ,即可证明产物为纯净的NaH ,即可证明产物为纯净的NaH |
B.NaH与水反应产生的 ,通过盛有碱石灰的干燥管,再用向上排空气法收集 ,通过盛有碱石灰的干燥管,再用向上排空气法收集 |
C.高温下NaH将四氯化钛( )还原成金属钛的原理为 )还原成金属钛的原理为 |
D.NaH在无水条件下除去钢铁表面铁锈的原理为 |
您最近一年使用:0次
10 . 亚氯酸钠 是一种重要的含氯消毒剂。马蒂逊法制备亚氯酸钠的流程如图,下列说法错误的是
是一种重要的含氯消毒剂。马蒂逊法制备亚氯酸钠的流程如图,下列说法错误的是
 是一种重要的含氯消毒剂。马蒂逊法制备亚氯酸钠的流程如图,下列说法错误的是
是一种重要的含氯消毒剂。马蒂逊法制备亚氯酸钠的流程如图,下列说法错误的是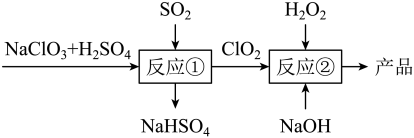
A.反应①阶段,参加反应的 和 和 的物质的量之比为2:1 的物质的量之比为2:1 |
B.反应②条件下, 的氧化性大于 的氧化性大于 |
C.反应②中的 可用 可用 代替 代替 |
D.若反应①通过原电池来实现,则 是正极产物 是正极产物 |
您最近一年使用:0次



