解题方法
1 . 下列物质不能由两种单质直接化合生成的是
A. | B. | C. | D. |
您最近一年使用:0次
名校
2 . 碳、氮、硫、氯是典型的非金属元素,下列有关碳、氮、硫、氯单质及其化合物的离子方程式书写正确的是
A.向浓硝酸中加入少量 粉末: 粉末: |
B.向 溶液中滴加醋酸溶液: 溶液中滴加醋酸溶液: |
C.实验室用 溶液检验 溶液检验 : : |
D. 溶解于水: 溶解于水: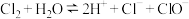 |
您最近一年使用:0次
2023-08-20更新
|
150次组卷
|
2卷引用:海南省部分学校2022-2023学年高一下学期7月期末考试化学试题
名校
解题方法
3 . 氯乙酸通常指一氯乙酸(俗称MCA),沸点为189℃,熔点为61~63℃,易溶于水,是有机合成的中间体。氯化法制备氯乙酸的原理如下:
主反应
副反应 、
、
某小组在实验室条件下制备氯乙酸并检验产物的装置如图1所示(夹持及加热装置省略):

已知: (X表示卤素原子)。
(X表示卤素原子)。
回答下列问题:
(1)盛装浓盐酸的分液漏斗中橡胶管的作用是_______ 。
(2)装置A中发生反应的离子方程式为_______ 。
(3)装置B的作用是_______ ,装置C中盛放的试剂是_______ 。
(4)利用下图装置从三颈烧瓶中分离MCA,控制过滤速率的操作方法是_______ 。

(5)测定产品纯度,准确称取9.45 g产品溶于蒸馏水中,加入适量NaOH溶液,煮沸,充分反应后,冷却至室温,加入过量试剂R,再加入过量AgNO3溶液,充分反应后,过滤、洗涤、干燥,得到m g沉淀,试剂R是_______ (填名称);当m=_______ 时,产品中不含Cl2CHCOOH等杂质。
主反应

副反应
 、
、
某小组在实验室条件下制备氯乙酸并检验产物的装置如图1所示(夹持及加热装置省略):

已知:
 (X表示卤素原子)。
(X表示卤素原子)。回答下列问题:
(1)盛装浓盐酸的分液漏斗中橡胶管的作用是
(2)装置A中发生反应的离子方程式为
(3)装置B的作用是
(4)利用下图装置从三颈烧瓶中分离MCA,控制过滤速率的操作方法是

(5)测定产品纯度,准确称取9.45 g产品溶于蒸馏水中,加入适量NaOH溶液,煮沸,充分反应后,冷却至室温,加入过量试剂R,再加入过量AgNO3溶液,充分反应后,过滤、洗涤、干燥,得到m g沉淀,试剂R是
您最近一年使用:0次
2023-08-14更新
|
118次组卷
|
2卷引用:海南省海口市等5地琼中黎族苗族自治县琼中中学等2校2022-2023学年高三上学期12月期末化学试题
4 . 实验装置、实验步骤的科学设计是实验达到预期目的的关键。下列说法正确的是
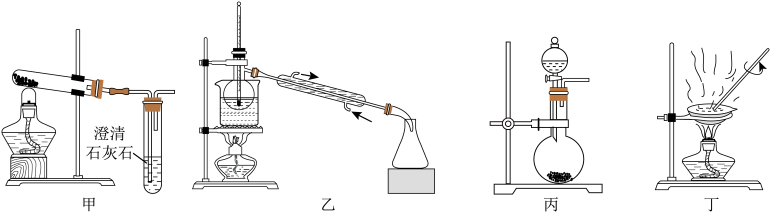

| A.用装置甲探究NaHCO3的稳定性 |
| B.用装置乙分离溴苯中溶解的少量苯 |
| C.用MnO2和浓HCl为原料制Cl2时,可在装置丙中进行 |
D.由FeCl3溶液制备 ,可在装置丁中进行 ,可在装置丁中进行 |
您最近一年使用:0次
5 . FeCl3能用于金属蚀刻、污水处理、印染工业,易潮解,加热易升华。某化学研究性学习小组模拟工业生产流程制备氯化铁并对产物做如下探究实验(部分夹持装置省略)。

(1)盛放MnO2的仪器名称为___________
(2)装置A中制氯气反应的离子方程式为___________ 。
(3)若缺少装置E,对本实验造成的影响是___________ 。
(4)将铁粉分散到石棉绒中的优点是___________ ,当硬质玻璃管中___________ 时,开始点燃D处的酒精灯。
(5)实验结束并冷却后,将收集器中的固体物质转移至锥形瓶中,进行如下实验:

查阅资料可知:SCN-能被氧化剂氧化。该小组对红色褪去的原因进行探究:
假设1:O2将SCN-氧化。
假设2:H2O2将SCN-氧化
通过设计如下实验得出假设2成立,请在下表空格中填写现象:

(1)盛放MnO2的仪器名称为
(2)装置A中制氯气反应的离子方程式为
(3)若缺少装置E,对本实验造成的影响是
(4)将铁粉分散到石棉绒中的优点是
(5)实验结束并冷却后,将收集器中的固体物质转移至锥形瓶中,进行如下实验:

查阅资料可知:SCN-能被氧化剂氧化。该小组对红色褪去的原因进行探究:
假设1:O2将SCN-氧化。
假设2:H2O2将SCN-氧化
通过设计如下实验得出假设2成立,请在下表空格中填写现象:
| 实验 | 操作 | 现象 | |
| 实验I(取褪色后的溶液2等份) | 第1份 | 滴加FeCl3溶液 | 无明显变化 |
| 第2份 | 滴加过量KSCN溶液 | ||
| 实验Ⅱ | 向实验Ⅰ的第2份溶液中再通入O2 | ||
您最近一年使用:0次
6 . 实验室处理尾气中的氯气,方法合理的是
| A.硫酸吸收 | B.碱液吸收 | C.燃烧除去 | D.直接排放 |
您最近一年使用:0次
2023-07-13更新
|
380次组卷
|
5卷引用:2022年海南省普通高中学业水平合格性考试化学试题
2022年海南省普通高中学业水平合格性考试化学试题海南省海口市秀英区某校2023-2024学年高一上学期期中检测化学试题(已下线)专题十一 氯及其化合物(已下线)合格考真题汇编10氯元素及其化合物(已下线)合格考真题汇编10氯元素及其化合物
22-23高三上·广东韶关·阶段练习
解题方法
7 . 无水AlCl3是一种重要的有机合成催化剂,该物质在183℃时升华,遇潮湿空气即产生大量白雾。某中学化学兴趣小组拟利用中学常见仪器设计实验制备无水AlCl3,实验装置如图所示。请回答下列问题。

(1)制备实验开始时,先检查装置的气密性,接下来的操作依次是_______ 。
a.加入MnO2粉末 b.点燃A中酒精灯 c.加入浓盐酸 d.点燃D处酒精灯
(2)写出A装置中发生反应的离子方程式:________ 。
(3)装置B和C中的试剂分别是_______ 、________ 。
(4)甲同学认为F和G可以用一种仪器替代,且加入一种药品即可达到相同效果,这种药品可以是_______ 。
(5)E中得到少量白色粉末,打开软木塞后可明显观察到锥形瓶中有白雾产生,用化学方程式表示其原因_______ 。
(6)制备过程中随着盐酸的浓度下降,氯气的制取反应会停止。为测定残余液中盐酸的浓度,某同学量取残余液10.00mL,加水稀释到250.00mL,然后从中取出20.00mL,用0.1000mol•L-1的NaOH标准溶液进行滴定,终点时消耗NaOH溶液24.00mL,则该残余液体中盐酸的浓度为________ 。

(1)制备实验开始时,先检查装置的气密性,接下来的操作依次是
a.加入MnO2粉末 b.点燃A中酒精灯 c.加入浓盐酸 d.点燃D处酒精灯
(2)写出A装置中发生反应的离子方程式:
(3)装置B和C中的试剂分别是
(4)甲同学认为F和G可以用一种仪器替代,且加入一种药品即可达到相同效果,这种药品可以是
(5)E中得到少量白色粉末,打开软木塞后可明显观察到锥形瓶中有白雾产生,用化学方程式表示其原因
(6)制备过程中随着盐酸的浓度下降,氯气的制取反应会停止。为测定残余液中盐酸的浓度,某同学量取残余液10.00mL,加水稀释到250.00mL,然后从中取出20.00mL,用0.1000mol•L-1的NaOH标准溶液进行滴定,终点时消耗NaOH溶液24.00mL,则该残余液体中盐酸的浓度为
您最近一年使用:0次
8 . 钛白粉( )广泛用于颜料、油漆和造纸等。某小组以钛铁矿粉(
)广泛用于颜料、油漆和造纸等。某小组以钛铁矿粉( )和金红石粉(
)和金红石粉( )为原料制备高纯度
)为原料制备高纯度 的流程如图所示:
的流程如图所示:

已知: 遇水极易水解。
遇水极易水解。
(1)在实验室进行操作A,装固体的仪器是___________ (填“坩埚”或“蒸发皿”)。
(2)写出钛铁矿与焦炭、氯气在高温下反应的化学方程式:___________ 。
(3)测定样品中 的纯度。取2.000g
的纯度。取2.000g 样品,在酸性条件下充分溶解,加入适量铝粉将
样品,在酸性条件下充分溶解,加入适量铝粉将 还原为T13+。过滤并洗涤,将所得滤液和洗涤液合并配制成250mL溶液,取25.00mL该溶液于锥形瓶中,滴入几滴KSCN溶液,用0.1000
还原为T13+。过滤并洗涤,将所得滤液和洗涤液合并配制成250mL溶液,取25.00mL该溶液于锥形瓶中,滴入几滴KSCN溶液,用0.1000
 标准溶液滴定,将
标准溶液滴定,将 转化成
转化成 ,消耗23.00mL标准溶液,杂质在整个过程中不反应。
,消耗23.00mL标准溶液,杂质在整个过程中不反应。
①该样品中 的质量分数为
的质量分数为___________ 。
②若开始时俯视滴定管读数,滴定终点时仰视滴定管读数,测得结果会___________ (填“偏高”“偏低”或“无影响”)。
(4)通过直接氯化法, 能用于制备
能用于制备 粗产品,其制备装置如图所示。
粗产品,其制备装置如图所示。

①若用 和浓盐酸制备氯气,写出装置A中反应的离子方程式:
和浓盐酸制备氯气,写出装置A中反应的离子方程式:___________ 。
②装置B中试剂的名称是___________ 。
③从环境保护角度考虑,本实验不足之处是___________ 。
 )广泛用于颜料、油漆和造纸等。某小组以钛铁矿粉(
)广泛用于颜料、油漆和造纸等。某小组以钛铁矿粉( )和金红石粉(
)和金红石粉( )为原料制备高纯度
)为原料制备高纯度 的流程如图所示:
的流程如图所示:
已知:
 遇水极易水解。
遇水极易水解。(1)在实验室进行操作A,装固体的仪器是
(2)写出钛铁矿与焦炭、氯气在高温下反应的化学方程式:
(3)测定样品中
 的纯度。取2.000g
的纯度。取2.000g 样品,在酸性条件下充分溶解,加入适量铝粉将
样品,在酸性条件下充分溶解,加入适量铝粉将 还原为T13+。过滤并洗涤,将所得滤液和洗涤液合并配制成250mL溶液,取25.00mL该溶液于锥形瓶中,滴入几滴KSCN溶液,用0.1000
还原为T13+。过滤并洗涤,将所得滤液和洗涤液合并配制成250mL溶液,取25.00mL该溶液于锥形瓶中,滴入几滴KSCN溶液,用0.1000
 标准溶液滴定,将
标准溶液滴定,将 转化成
转化成 ,消耗23.00mL标准溶液,杂质在整个过程中不反应。
,消耗23.00mL标准溶液,杂质在整个过程中不反应。①该样品中
 的质量分数为
的质量分数为②若开始时俯视滴定管读数,滴定终点时仰视滴定管读数,测得结果会
(4)通过直接氯化法,
 能用于制备
能用于制备 粗产品,其制备装置如图所示。
粗产品,其制备装置如图所示。
①若用
 和浓盐酸制备氯气,写出装置A中反应的离子方程式:
和浓盐酸制备氯气,写出装置A中反应的离子方程式:②装置B中试剂的名称是
③从环境保护角度考虑,本实验不足之处是
您最近一年使用:0次
9 . 下列装置或操作不能达到实验目的的是
A | B | C | D | |
装置或操作 | 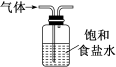 |  | 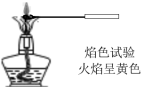 | 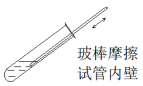 |
实验目的 | 除去 中少量的 中少量的 气体 气体 | 检验溴乙烷中溴原子 | 证明溶液中存在 |  晶体制备 晶体制备 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
10 . 次氯酸钠是家庭洗涤剂中的含“氯”漂白剂。某兴趣小组用如图所示装置(在冰水浴条件下)制备 溶液并对产品成分含量进行测定。
溶液并对产品成分含量进行测定。
回答下列问题:
Ⅰ.制备 溶液:
溶液:

(1)仪器X的名称为___________ ;按照气流方向,装置正确的连接顺序为a___________ (填小写字母)。
(2)装置A中反应的化学方程式为___________ 。
(3)装置E中各生成物的物质的量和溶液的温度随时间的变化如图所示,若发现装置E中温度计的温度上升过快,可能导致产物中存在杂质,为避免此状况,装置A应进行的操作为___________ 。

Ⅱ.测定产品中有效成分含量:
①取10mL仪器X中的产品于碘量瓶中,加入50mL蒸馏水、足量KI溶液和稀硫酸,迅速盖紧瓶塞后,在暗处静置5min;
②加入指示剂,用 标准溶液滴定至终点,平行测定三次,
标准溶液滴定至终点,平行测定三次, 标准溶液的平均用量为48.00mL。(已知:
标准溶液的平均用量为48.00mL。(已知: ,杂质不参与反应)
,杂质不参与反应)
(4)步骤①中反应的离子方程式为___________ 。
(5)步骤②中加入的指示剂为___________ ;达到滴定终点时的判断依据为___________ 。
(6)产品中
___________  。
。
 溶液并对产品成分含量进行测定。
溶液并对产品成分含量进行测定。回答下列问题:
Ⅰ.制备
 溶液:
溶液:
(1)仪器X的名称为
(2)装置A中反应的化学方程式为
(3)装置E中各生成物的物质的量和溶液的温度随时间的变化如图所示,若发现装置E中温度计的温度上升过快,可能导致产物中存在杂质,为避免此状况,装置A应进行的操作为

Ⅱ.测定产品中有效成分含量:
①取10mL仪器X中的产品于碘量瓶中,加入50mL蒸馏水、足量KI溶液和稀硫酸,迅速盖紧瓶塞后,在暗处静置5min;
②加入指示剂,用
 标准溶液滴定至终点,平行测定三次,
标准溶液滴定至终点,平行测定三次, 标准溶液的平均用量为48.00mL。(已知:
标准溶液的平均用量为48.00mL。(已知: ,杂质不参与反应)
,杂质不参与反应)(4)步骤①中反应的离子方程式为
(5)步骤②中加入的指示剂为
(6)产品中

 。
。
您最近一年使用:0次
2023-05-11更新
|
498次组卷
|
6卷引用:海南省农垦中学2023-2024学年高二上学期第一次月考化学试题
海南省农垦中学2023-2024学年高二上学期第一次月考化学试题湖南省衡阳市名校协作体2023届高三第三次模拟考试化学试题湖北省2023届高三5月联考化学试题陕西省西安市长安区第一中学2022-2023学年高二下学期期末考试化学试题(已下线)考点巩固卷13 化学实验基础(二)(3个考点30题)-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)实验综合题



