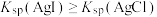A.用 溶液可检验 溶液可检验 |
B.用 溶液和稀盐酸可检验 溶液和稀盐酸可检验 |
C.用干燥的 试纸可测得氯水的 试纸可测得氯水的 为4 为4 |
D.用 溶液和湿润的红色石蕊试纸可检验 溶液和湿润的红色石蕊试纸可检验 |
 的过程中有水蒸气和
的过程中有水蒸气和 挥发出来,同时证明
挥发出来,同时证明 的某些性质。甲同学设计了如图所示的实验装置(部分支撑用的铁架台省略)。
的某些性质。甲同学设计了如图所示的实验装置(部分支撑用的铁架台省略)。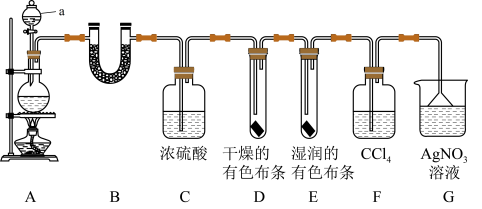
 仪器的名称是
仪器的名称是 反应制取
反应制取 的化学反应方程式为:
的化学反应方程式为:(2)①装置
 中盛放的试剂名称为
中盛放的试剂名称为②装置
 和
和 中出现的不同现象说明的问题是
中出现的不同现象说明的问题是③装置
 的作用是
的作用是④写出装置
 中发生反应的离子方程式
中发生反应的离子方程式(3)乙同学认为甲同学设计的实验有缺陷,不能确保最终通入
 溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入
溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入 溶液中的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在
溶液中的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在 与
与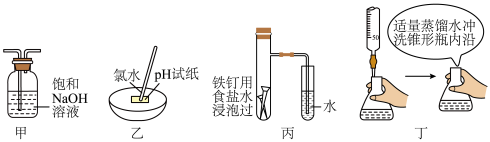
| A.甲装置可以除氯气中的氯化氢气体 |
| B.乙装置用来测新制氯水的pH值 |
| C.丙装置可以验证铁的吸氧腐蚀 |
| D.丁装置为用高锰酸钾溶液滴定草酸接近终点的操作 |
|
|
| A.测定中和反应反应热 | B.探究温度对 溶解度的影响 溶解度的影响 |
|
|
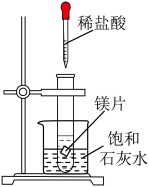
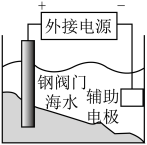
| C.测定氯水的pH | D.外加电流法保护钢阀门 |
| A.A | B.B | C.C | D.D |
5 . 下列实验设计、现象和结论都正确的是
选项 | 实验 | 现象 | 结论 |
A | 将CO2通入BaCl2溶液中 | 有白色沉淀生成 | 白色沉淀是BaCO3 |
B | 向两支试管中各加入1 mL 1 mol/L的酸性KMnO4溶液,再向两支试管分别加入2 mL 1 mol/L的H2C2O4溶液和2mL0.5mol/L的H2C2O4溶液,记录高锰酸钾溶液褪色所需时间 | 1 mol/L的H2C2O4溶液中高锰酸钾溶液褪色快 | 浓度越大,反应速率越快 |
C | 向含AgCl和AgBr的饱和溶液中加入足量浓AgNO3溶液 | 产生两种颜色沉淀,但以白色为主 |
|
D | 向滴有酚酞的氨水中滴加氯水 | 溶液的红色褪去 | 氯水具有漂白性 |
| A.A | B.B | C.C | D.D |
6 . 下列实验操作、实验现象及根据现象得出的结论,都正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 用食醋浸泡水垢,水垢主要成分:CaCO3与Mg(OH)2 | 水垢溶解,有无色气泡产生 | 碱性:CH3COONa>Na2CO3 |
B | 向浓度均为0.1 mol/L的NaCl和NaI混合溶液中滴加少量AgNO3溶液 | 先出现黄色沉淀 |
|
C | 向CH3COONa溶液中滴加酚酞,加热 | 溶液红色加深 | 水解是吸热过程 |
D | 用广泛pH试纸测定新制氯水的pH | pH=3.0 | 氯水呈酸性 |
| A.A | B.B | C.C | D.D |
| 选项 | 实验操作 | 现象和结论 |
| A | 室温下分别测定 溶液和 溶液和 溶液的 溶液的 | 两者 都大于7,且 都大于7,且 溶液的 溶液的 大,说明 大,说明 的水解能力强于 的水解能力强于 |
| B | 取两份新制氯水,分别滴加 溶液和淀粉 溶液和淀粉 溶液 溶液 | 前者有白色沉淀,后者溶液变蓝色,说明 与 与 反应存在限度 反应存在限度 |
| C | 测定均为离子化合物的 和 和 的熔点 的熔点 |  的熔点更高,说明 的熔点更高,说明 中离子键强于 中离子键强于 |
| D | 向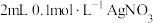 溶液中先滴加4滴 溶液中先滴加4滴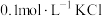 溶液,再滴加4滴 溶液,再滴加4滴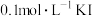 溶液 溶液 | 先产生白色沉淀,再产生黄色沉淀。说明 转化为 转化为 , , 溶解度小于 溶解度小于 |
| A.A | B.B | C.C | D.D |
| A.红棕色的NO2体系加压后,颜色先变深后逐渐变浅 |
| B.将0.01mol/LFeCl3溶液加热,溶液的颜色加深 |
| C.H2、I2、HI平衡混合气加压后颜色变深 |
| D.新制的氯水在光照下颜色变浅 |
(1)可逆反应
 是炼铁工业中一个重要反应,其温度与平衡常数K的关系如下表:
是炼铁工业中一个重要反应,其温度与平衡常数K的关系如下表: | 938 | 1100 |
 | 0.68 | 0.40 |
(2)已知:
 ,反应
,反应 的平衡常数
的平衡常数 。保持温度在
。保持温度在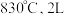 恒容反应器中发生上述反应同时充入以下物质:
恒容反应器中发生上述反应同时充入以下物质: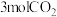 、
、 ,此时反应向
,此时反应向(3)常温下浓度均为
 的下列六种溶液的
的下列六种溶液的 如下表:
如下表:| 溶质 |  |  |  |  |  |
 | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
②根据表中数据判断:浓度均为
 的下列四种物质的溶液中,酸性最强的是
的下列四种物质的溶液中,酸性最强的是 变化最小的是
变化最小的是A.
 B.
B. C.
C. D.
D.
③据上表数据,请你判断下列反应不能成立的是
A.

B.

C.

(4)要增大氯水中
 的浓度,可向氯水中加入少量的碳酸钠溶液,反应的离子方程式为
的浓度,可向氯水中加入少量的碳酸钠溶液,反应的离子方程式为 。氯水具有多种性质,研究小组同学用氯水分别与紫色石蕊溶液,
。氯水具有多种性质,研究小组同学用氯水分别与紫色石蕊溶液, 溶液反应。请完成下列问题:
溶液反应。请完成下列问题:(1)向紫色石蕊溶液中滴加氯水的现象是
(2)向
 溶液中滴加少量氯水,证明氯水有氧化性的实验方案是:取适量反应后溶液于试管中,
溶液中滴加少量氯水,证明氯水有氧化性的实验方案是:取适量反应后溶液于试管中,(3)氯水光照时黄绿色会逐渐变浅直至消失,并产生无色气体,请用平衡理论解释黄绿色变浅的原因: