名校
1 . 某家用防疫用品“84消毒液”的包装说明如下,请回答下列问题:
(1)“84”消毒液可由Cl2与NaOH溶液反应制得,Cl2与NaOH溶液反应的化学方程式为___________
(2)欲将“84消毒液”原液稀释配制成450mL c(NaClO)=0.100mol·L-1的溶液。
①配制过程中,需要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、___________ 、___________ 。
②配制时,需要取用___________ mL“84消毒液”原液。
③下列操作会使溶液中NaClO浓度偏低的是___________ 。
A.取用的“84消毒液”原液是久置的
B.定容操作时,俯视刻度线
C.量取“84消毒液”原液时,仰视读数
D.定容摇匀后,液面低于刻度线,再加水至刻度线
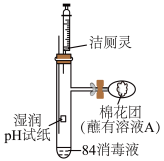
(3)利用如图装置探究84消毒液与洁厕灵(主要成分为盐酸)的反应,当注射器中的洁厕灵注入试管中时,装置内产生黄绿色气体,可观察到pH试纸的现象是___________
| 【产品名称】84消毒液 【有效成分】NaClO 【规格】1000mL 【物质的量浓度】4.0  注:①按一定比例稀释后使用 ②不得与酸性产品(如洁厕灵)同时使用。 |
(2)欲将“84消毒液”原液稀释配制成450mL c(NaClO)=0.100mol·L-1的溶液。
①配制过程中,需要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、
②配制时,需要取用
③下列操作会使溶液中NaClO浓度偏低的是
A.取用的“84消毒液”原液是久置的
B.定容操作时,俯视刻度线
C.量取“84消毒液”原液时,仰视读数
D.定容摇匀后,液面低于刻度线,再加水至刻度线
(3)利用如图装置探究84消毒液与洁厕灵(主要成分为盐酸)的反应,当注射器中的洁厕灵注入试管中时,装置内产生黄绿色气体,可观察到pH试纸的现象是

您最近一年使用:0次
2023-11-11更新
|
221次组卷
|
4卷引用:河南省焦作市博爱县第一中学2023-2024学年高二上学期11月期中化学试题
河南省焦作市博爱县第一中学2023-2024学年高二上学期11月期中化学试题福建省福州市八县一中2023-2024学年高一上学期11月期中化学试题(已下线)【精品卷】2.3.3 物质的量浓度课堂例题-人教版2023-2024学年必修第一册福建省泉州市惠南中学2023-2024学年高一上学期12月月考化学试题
2 . 海洋蕴藏着中极为丰富的化学资源,如海水中就有80多种元素,所含的盐大部分是氯化钠。十九世纪末工业上开始通过电解饱和食盐水的方法制备氯气、氨气和烧碱,并以它们为原料生产一系列含氯、含钠产品(氯碱工业),请回答下列问题:
(1)天原化工厂是我国最早的氯碱企业,其创始人是______(单选)
(2)电解饱和食盐水时,与电源正极相连的电极叫阳极,阳极产物是氯气,可以用______ 检验,现象为______ ,写出检验氯气的离子方程式_____________________
(3)工业上用氯气与消石灰制成漂白粉,漂白粉的有效成分为______(单选)
(4)新制氧水呈浅黄绿色,是因为氯水中存在______(单选)
(5)有两组学生根据不同的反应原理在实验室制取氯气。

①请按要求填表。
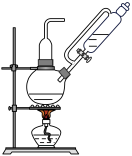
②有同学建议第一组使用图所示装置作为氯气的发生装置,请谈谈你的看法______ 。
氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用如图表示。
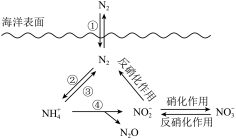
(6)海洋中的氮循环属于固氮作用的一步是______ (填图中的数字序号)。
(7)下列关于海洋氮循环的说法正确的是______(双选)。
(8)有氧时,在硝化细菌作用下, 可实现过程④的转化,方程式如下,请标出该反应的电子转移的方向与数目。
可实现过程④的转化,方程式如下,请标出该反应的电子转移的方向与数目。_______ 。

(9)有人研究了温度对海洋硝化细菌去除氯氮效果的影响.下表为对 人工海水样本的监测数据.硝化细菌去除氨氮的最佳反应温度是
人工海水样本的监测数据.硝化细菌去除氨氮的最佳反应温度是______ ,在最佳反应温度时, 内去除氨氮反应的平均速率是
内去除氨氮反应的平均速率是____ 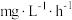 。
。
(1)天原化工厂是我国最早的氯碱企业,其创始人是______(单选)
| A.侯德榜 | B.吴蕴初 | C.荣毅仁 | D.戴安邦 |
(3)工业上用氯气与消石灰制成漂白粉,漂白粉的有效成分为______(单选)
A. | B. | C. | D. |
A. | B. | C. | D. |

①请按要求填表。
实验组 | 实验原理 | 发生装置(填编号) |
第一组 |  | |
第二组 | 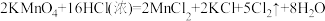 |

氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用如图表示。

(6)海洋中的氮循环属于固氮作用的一步是
(7)下列关于海洋氮循环的说法正确的是______(双选)。
| A.海洋中存在游离态的氮 |
| B.海洋中的氮循环起始于氮的氧化 |
C.向海洋排放含 的废水会影响海洋中 的废水会影响海洋中 的含量 的含量 |
| D.海洋中的反硝化作用一定有氧气的参与 |
 可实现过程④的转化,方程式如下,请标出该反应的电子转移的方向与数目。
可实现过程④的转化,方程式如下,请标出该反应的电子转移的方向与数目。
(9)有人研究了温度对海洋硝化细菌去除氯氮效果的影响.下表为对
 人工海水样本的监测数据.硝化细菌去除氨氮的最佳反应温度是
人工海水样本的监测数据.硝化细菌去除氨氮的最佳反应温度是 内去除氨氮反应的平均速率是
内去除氨氮反应的平均速率是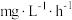 。
。温度/ | 样本氨氮含量/ | 处理 | 处理 |
氨氮含量/ | 氨氮含量/ | ||
20 | 1008 | 838 | 788 |
25 | 1008 | 757 | 468 |
30 | 1008 | 798 | 600 |
40 | 1008 | 977 | 910 |
您最近一年使用:0次
3 . 电解质在水溶液中的行为影响了电解质溶液的性质(以下讨论均在常温时)。
(1)0.1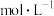
 溶液的pH=3
溶液的pH=3
① 的电离度
的电离度___________ (用百分比表示)。
②该溶液中由水电离出的 浓度是
浓度是___________ 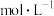 。
。
③计算 的电离平衡常数
的电离平衡常数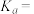
___________ 。
(2)H2CO3和HClO离平衡常数如下:
①向NaClO溶液通入少量 的离子方程式
的离子方程式___________ 。
②向 的溶液中通入少量
的溶液中通入少量 的离子方程式
的离子方程式___________ 。
③NaClO溶液的漂白性与溶液中c(HClO)有关。向NaClO溶液中加入下列物质,能增大c(HClO)的是____ (填字母)。向新制的氯水中滴加2滴石蕊溶液,观察的现象为____ 。
a. b.
b. c.
c.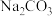 d.NaOH
d.NaOH
(1)0.1
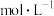
 溶液的pH=3
溶液的pH=3①
 的电离度
的电离度②该溶液中由水电离出的
 浓度是
浓度是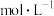 。
。③计算
 的电离平衡常数
的电离平衡常数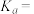
(2)H2CO3和HClO离平衡常数如下:
| 化学式 | 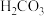 | HClO |
电离平衡常数(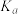 ) ) | 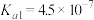  | 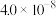 |
①向NaClO溶液通入少量
 的离子方程式
的离子方程式②向
 的溶液中通入少量
的溶液中通入少量 的离子方程式
的离子方程式③NaClO溶液的漂白性与溶液中c(HClO)有关。向NaClO溶液中加入下列物质,能增大c(HClO)的是
a.
 b.
b. c.
c.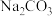 d.NaOH
d.NaOH
您最近一年使用:0次
4 . 某兴趣小组探究氯的单质及其化合物的性质。
Ⅰ.甲同学设计如图所示装置研究氯气能否与水发生反应,气体a是含有少量空气和水蒸气的氯气。
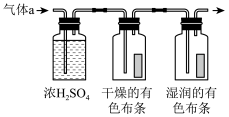
(1)浓硫酸的作用是___________ 。
(2)证明氯气和水反应的实验现象为___________ 。
(3)Cl2溶于水可制得氯水,检验氯水中的Cl-,可选择___________(填字母序号)试剂。
Ⅱ.回答下列问题
(4)NaClO是“84消毒液”的有效成分,在抗击新冠肺炎疫情中发挥了重要作用。向“84消毒液”中滴入盐酸,可能发生反应: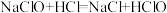 ,其属于
,其属于___________ (填四大基本反应类型)反应。乙同学认为上述过程中还发生了氧化还原反应并生成Cl2,反应的离子方程式为___________ 。
Ⅰ.甲同学设计如图所示装置研究氯气能否与水发生反应,气体a是含有少量空气和水蒸气的氯气。

(1)浓硫酸的作用是
(2)证明氯气和水反应的实验现象为
(3)Cl2溶于水可制得氯水,检验氯水中的Cl-,可选择___________(填字母序号)试剂。
| A.硝酸银溶液 | B.酚酞溶液 | C.碳酸钠溶液 | D.品红溶液 |
Ⅱ.回答下列问题
(4)NaClO是“84消毒液”的有效成分,在抗击新冠肺炎疫情中发挥了重要作用。向“84消毒液”中滴入盐酸,可能发生反应:
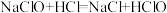 ,其属于
,其属于
您最近一年使用:0次
5 . 在氨水中存在的粒子有___________ ;在氯水中存在的粒子有___________ 。
您最近一年使用:0次
解题方法
6 . SO2和Cl2是中学化学中常见的气体,探究二者的制法和性质是十分重要的内容。
(1)实验室可通过铜与浓硫酸加热制SO2.请写出该反应的化学方程式___________
(2)如图是用KMnO4与浓盐酸反应制取适量Cl2的简易装置。已知: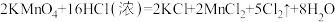

①B、D装置的作用依次是___________ 、___________ 。
②E中反应的离子方程式为___________ 。
(3)某同学用如图装置探究SO2、Cl2的化学性质。通过控制弹簧夹a、b,向X中分别通入不同气体:

①若关闭b,打开a,X溶液为品红溶液,则X中的现象为___________ ,说明二氧化硫具有___________ 性。
②若关闭a,打开b,X溶液为紫色石蕊试液,则X中的现象为___________ 。
③若同时打开a、b,X溶液为紫色石蕊试液,同时通入体积比(同温同压)为1:1的气体,则X中的现象为___________ ,与②中现象不同的原因是___________ (用化学方程式表示)。
(1)实验室可通过铜与浓硫酸加热制SO2.请写出该反应的化学方程式
(2)如图是用KMnO4与浓盐酸反应制取适量Cl2的简易装置。已知:
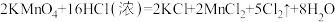

①B、D装置的作用依次是
②E中反应的离子方程式为
(3)某同学用如图装置探究SO2、Cl2的化学性质。通过控制弹簧夹a、b,向X中分别通入不同气体:

①若关闭b,打开a,X溶液为品红溶液,则X中的现象为
②若关闭a,打开b,X溶液为紫色石蕊试液,则X中的现象为
③若同时打开a、b,X溶液为紫色石蕊试液,同时通入体积比(同温同压)为1:1的气体,则X中的现象为
您最近一年使用:0次
2021-02-24更新
|
730次组卷
|
2卷引用:云南建水县第六中学2020-2021学年高二上学期期中考试化学试题
解题方法
7 . 请根据物质在生产中的应用填空:
(1)自来水厂对水消毒,常使用的物质是__________ (填“液氯”或“明矾”)
(2)制造光导纤维的基本原料是__________ (填“硅”或“二氧化硅”)
(3)铁在冷的浓硫酸或浓硝酸中,表面被氧化生成致密氧化物膜而保护内层金属,常温下盛装浓硫酸或浓硝酸可以使用容器是________ (填“铁罐”或“铜罐”)
(1)自来水厂对水消毒,常使用的物质是
(2)制造光导纤维的基本原料是
(3)铁在冷的浓硫酸或浓硝酸中,表面被氧化生成致密氧化物膜而保护内层金属,常温下盛装浓硫酸或浓硝酸可以使用容器是
您最近一年使用:0次
名校
解题方法
8 . 氧化物X、单质Y都能对大气造成污染。已知X是红棕色气体,能与水反应;Y是黄绿色气体,能使湿润的有色布条褪色。请回答下列问题:
(1)X的化学式为_________ ;
(2)X与水反应生成NO和一种酸,该酸的名称为________ ;
(3)Y能使湿润的有色布条褪色,说明Y的水溶液具有____ (填“漂白”或“酸”)性。
(1)X的化学式为
(2)X与水反应生成NO和一种酸,该酸的名称为
(3)Y能使湿润的有色布条褪色,说明Y的水溶液具有
您最近一年使用:0次
2020-03-09更新
|
307次组卷
|
3卷引用:2016年湖南省普通高中学业水平考试化学试题
解题方法
9 . 新制备的氯水显酸性,说明氯水中有______ (填离子符号)存在。向氯水中滴入几滴AgNO3溶液,立即有______ 生成,说明氯水中有Cl-存在。请写出Cl2与水反应的化学方程式为:________ 。
您最近一年使用:0次
2020-01-21更新
|
42次组卷
|
2卷引用:湖南省茶陵县第三中学2019-2020学年高二上学期期末考试化学(学考)试题
10 . 请回答下列问题:
(1) 浓硫酸常用作干燥剂,说明浓硫酸具有__________ ;(填“吸水性”或“脱水性”)
(2) 实验室中少量钠常常保存在______ 中(填“煤油”或“水”);
(3)Al2O3能溶于酸或强碱溶液生成盐和水,则Al2O3是一种_________ (填“酸性”、“碱性”或“两性”)氧化物
(4) 氨气极易溶于水,其水溶液显_________ (填“酸”、“碱”或“中”)性
(5) 检验某补铁剂中的Fe2+是否被氧化成Fe3+,可用_____ (填“KSCN”或“H2SO4”)溶液;
(6)新制氯水中含有Cl2 、H2O、HClO、H+、Cl-等粒子,根据下列性质选择恰当的粒子进行填空(填符号)。
①新制绿水呈现浅黄绿色的物质是___________________ .
②能起杀菌消毒作用,光照易分解的弱酸是______________ .
③能与硝酸银作用生成白色沉淀的离子是_______________ .
(1) 浓硫酸常用作干燥剂,说明浓硫酸具有
(2) 实验室中少量钠常常保存在
(3)Al2O3能溶于酸或强碱溶液生成盐和水,则Al2O3是一种
(4) 氨气极易溶于水,其水溶液显
(5) 检验某补铁剂中的Fe2+是否被氧化成Fe3+,可用
(6)新制氯水中含有Cl2 、H2O、HClO、H+、Cl-等粒子,根据下列性质选择恰当的粒子进行填空(填符号)。
①新制绿水呈现浅黄绿色的物质是
②能起杀菌消毒作用,光照易分解的弱酸是
③能与硝酸银作用生成白色沉淀的离子是
您最近一年使用:0次






