名校
解题方法
1 . 下列反应的离子方程式正确的是
A.铜跟浓HNO3反应:3Cu+8H++2NO =3Cu2++2NO↑+4H2O =3Cu2++2NO↑+4H2O |
B.向氯化铝溶液中加入过量氨水:Al3++4OH﹣=AlO +2H2O +2H2O |
| C.向水中通入Cl2:Cl2+H2O=2H++Cl﹣+ClO- |
D.NaAlO2溶液和NaHCO3溶液混合:AlO +HCO +HCO +H2O=Al(OH)3↓+CO +H2O=Al(OH)3↓+CO |
您最近一年使用:0次
2 . 某实验小组用如图装置制备氯气并探究其性质(夹持装置已省略),下列分析错误的是
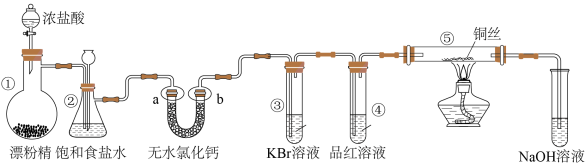

A.装置①中生成氯气反应的化学方程式: |
| B.a、b分别放干燥和湿润的有色布条,可以验证干燥的Cl2不具有漂白性 |
| C.反应开始后可观察到③中溶液变黄,④中溶液褪色,说明氯水具有氧化性和漂白性 |
| D.反应开始后点燃酒精灯,可在⑤号硬质玻璃管中观察到棕黄色烟 |
您最近一年使用:0次
2023-11-01更新
|
1275次组卷
|
2卷引用:2024届广东省湛江市普通高中毕业班调研测试化学试题
名校
解题方法
3 . 下列离子方程式书写正确的是
A. 通入水中制氯水: 通入水中制氯水: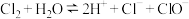 |
B.用 溶液处理锅炉水垢中的 溶液处理锅炉水垢中的 : : |
C.过量铁粉与稀硝酸反应: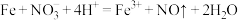 |
D. 溶液与少量 溶液与少量 溶液混合: 溶液混合: |
您最近一年使用:0次
名校
4 . 二氯异氰尿酸钠[(CNO)3Cl2Na]是常用的杀菌消毒剂,常温下为白色固体,难溶于冷水。某同学利用高浓度的NaClO溶液和(CNO)3H3固体在10℃时反应制备二氯异氰尿酸钠,装置如图所示(部分夹持装置略)。
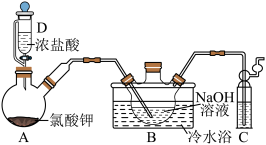
已知:2NaClO+(CNO)3H3=(CNO)3Cl2Na+NaOH+H2O。
回答下列问题:
(1)装置A中用氯酸钾和浓盐酸制备Cl2的化学方程式为___________ 。
(2)装置D的名称是___________ ;它的作用是___________ 。
(3)待装置B___________ (填实验现象)时,再由三颈烧瓶上口加入(CNO)3H3固体;反应过程中仍需不断通入Cl2的理由是___________ 。
(4)通过下列实验测定二氯异氰尿酸钠样品中有效氯的含量。
反应原理:[(CNO)3Cl2]-+H++2H2O=(CNO)3H3+2HClO;
HClO+2I-+H+=I2+Cl-+H2O;
2S2O +I2=S4O
+I2=S4O +2I-。
+2I-。
实验步骤:准确称取mg样品,用容量瓶配成250mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,充分反应后,用c mol/L Na2S2O3标准溶液滴定至溶液呈微黄色。加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液平均为V mL。
①滴定终点现象为___________ 。
②该样品的有效氯含量表达式为___________ 。 (该样品的有效氯=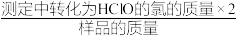 ×100%)
×100%)

已知:2NaClO+(CNO)3H3=(CNO)3Cl2Na+NaOH+H2O。
回答下列问题:
(1)装置A中用氯酸钾和浓盐酸制备Cl2的化学方程式为
(2)装置D的名称是
(3)待装置B
(4)通过下列实验测定二氯异氰尿酸钠样品中有效氯的含量。
反应原理:[(CNO)3Cl2]-+H++2H2O=(CNO)3H3+2HClO;
HClO+2I-+H+=I2+Cl-+H2O;
2S2O
 +I2=S4O
+I2=S4O +2I-。
+2I-。实验步骤:准确称取mg样品,用容量瓶配成250mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,充分反应后,用c mol/L Na2S2O3标准溶液滴定至溶液呈微黄色。加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液平均为V mL。
①滴定终点现象为
②该样品的有效氯含量表达式为
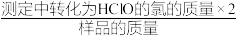 ×100%)
×100%)
您最近一年使用:0次
5 . 84消毒液(有效成分为 )和双氧水是常用的家用消毒剂。
)和双氧水是常用的家用消毒剂。
(1)实验室用 和
和 溶液制备84消毒液,其反应的离子方程式为
溶液制备84消毒液,其反应的离子方程式为___________ 。
(2)在研究物质性质时,研究小组向盛有 84消毒液的试管中逐滴加入10%的双氧水,发现有大量的气泡产生,对此作出以下猜测。
84消毒液的试管中逐滴加入10%的双氧水,发现有大量的气泡产生,对此作出以下猜测。
[猜测1]双氧水与消毒液发生反应产生气体。
[猜测2]……
①请设计实验证明产生的气体为氧气:___________ 。
②猜测2可能为___________ 。
③为了验证猜想,设计用如下装置进行实验,注射器中装有 10%的双氧水,锥形瓶中装有
10%的双氧水,锥形瓶中装有 84消毒液,分5次注入双氧水,产生气体的体积如下表所示。
84消毒液,分5次注入双氧水,产生气体的体积如下表所示。
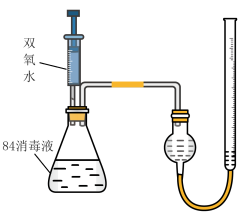
④
___________ ;通过实验得出猜想1正确,其判断依据为___________ ,二者发生反应的化学方程式为___________ 。
 )和双氧水是常用的家用消毒剂。
)和双氧水是常用的家用消毒剂。(1)实验室用
 和
和 溶液制备84消毒液,其反应的离子方程式为
溶液制备84消毒液,其反应的离子方程式为(2)在研究物质性质时,研究小组向盛有
 84消毒液的试管中逐滴加入10%的双氧水,发现有大量的气泡产生,对此作出以下猜测。
84消毒液的试管中逐滴加入10%的双氧水,发现有大量的气泡产生,对此作出以下猜测。[猜测1]双氧水与消毒液发生反应产生气体。
[猜测2]……
①请设计实验证明产生的气体为氧气:
②猜测2可能为
③为了验证猜想,设计用如下装置进行实验,注射器中装有
 10%的双氧水,锥形瓶中装有
10%的双氧水,锥形瓶中装有 84消毒液,分5次注入双氧水,产生气体的体积如下表所示。
84消毒液,分5次注入双氧水,产生气体的体积如下表所示。
| 次数 | 注入双氧水的体积/mL | 产生气体的总体积/mL |
| 第1次 | 4 | 125 |
| 第2次 | 4 | 250 |
| 第3次 | 4 | 325 |
| 第4次 | 4 | V |
| 第5次 | 4 | 333 |

您最近一年使用:0次
2023-10-30更新
|
100次组卷
|
2卷引用:江西省百师联盟2024届高三上学期一轮复习联考化学试题
6 . 在给定条件下,下列选项所示的物质间转化关系均正确的是
A. |
B. |
C. |
D. |
您最近一年使用:0次
解题方法
7 . 某化学小组用“84消毒液” (主要成分有 NaClO)制备氯气并探究其性质,进行如图所示的实验(a~d中均为浸有相应试液的棉花,夹持装置省略)。下列说法正确的是
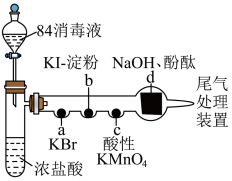

| A.具支试管中反应生成了黄绿色气体,该反应体现了浓盐酸的酸性和还原性 |
| B.a处变为橙色, b处变为蓝色,说明氧化性:Cl2>Br2>I2 |
| C.c处褪色, 说明 Cl2具有还原性 |
| D.d处褪色,说明Cl2具有漂白性 |
您最近一年使用:0次
2023-10-29更新
|
411次组卷
|
2卷引用:广东省深圳市宝安区2023-2024学年高三上学期第一次调研测试化学试题
名校
解题方法
8 . 按要写出下列反应的离子方程式:
(1)向FeBr2溶液中通入等物质的量Cl2___________ 。
(2)向Ba(HCO3)2溶液中滴加少量NaOH溶液___________ 。
(3)SO2通入酸性KMnO4溶液中___________ 。
(4)用过氧化氢从酸化的海带灰浸出液中提取碘___________ 。
(5)Fe3O4与稀硝酸反应___________ 。
(1)向FeBr2溶液中通入等物质的量Cl2
(2)向Ba(HCO3)2溶液中滴加少量NaOH溶液
(3)SO2通入酸性KMnO4溶液中
(4)用过氧化氢从酸化的海带灰浸出液中提取碘
(5)Fe3O4与稀硝酸反应
您最近一年使用:0次
名校
解题方法
9 . 下列操作、现象和结论均正确且有关联性的是
| 选项 | 操作及现象 | 结论 |
| A | 向品红溶液中通入氯气,品红溶液褪色 | 氯气有漂白性 |
| B | 向酸性 溶液中滴加乙醇,溶液褪色 溶液中滴加乙醇,溶液褪色 | 乙醇表现还原性 |
| C | 在酚酞溶液中加入 粉末,溶液先变红后褪色 粉末,溶液先变红后褪色 |  表现碱性 表现碱性 |
| D | 在盛满 的集气瓶中加入烘干的活性炭,气体颜色变浅 的集气瓶中加入烘干的活性炭,气体颜色变浅 | 活性炭表现还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-10-27更新
|
388次组卷
|
5卷引用:陕西省汉中市多校2023-2024学年高三上学期第四次联考化学试题
10 . 某小组设计实验探究氯气性质,装置如图(夹持装置已省略)。下列叙述错误的是
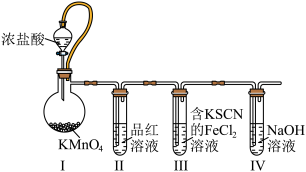

| A.I装置中浓盐酸只表现还原性,可以用Ca(ClO)2替代KMnO4 |
| B.若加热II装置中的无色溶液后,溶液仍为无色,则氯水具有永久漂白性 |
| C.若III装置中溶液变红色,则氯气表现氧化性 |
| D.IV装置用于吸收尾气中氯气 |
您最近一年使用:0次



