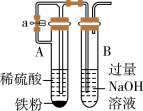
1 . 下列实验装置使用正确的是
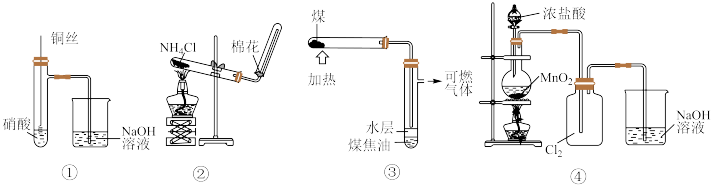
| A.图①装置用于铜和稀硝酸反应的探究实验 | B.图②装置用于实验室制备 |
| C.图③装置用于煤的气化实验 | D.图④装置用于实验室制备 |
您最近一年使用:0次
2024-05-04更新
|
321次组卷
|
3卷引用:浙江绍兴市2023-2024学年高三下学期选考科目适应性考试化学试题
解题方法
2 . 下图为实验室制备氯气并进行一系列相关实验的装置(夹持仪器、加热仪器已略)。

(1)仪器a的名称为___________
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅲ应该放___________ 。(填写“湿润红纸”或“干燥红纸”)
(3)写出氯气的尾气处理原理(用离子方程式表示)___________ 。

(1)仪器a的名称为
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅲ应该放
(3)写出氯气的尾气处理原理(用离子方程式表示)
您最近一年使用:0次
解题方法
3 . 实验室制Cl2的反应为4HCl(浓)十MnO2 MnCl2+C12↑+2H2O,下列说法错误的是
MnCl2+C12↑+2H2O,下列说法错误的是
 MnCl2+C12↑+2H2O,下列说法错误的是
MnCl2+C12↑+2H2O,下列说法错误的是| A.还原剂是HCl,氧化剂是MnO2 |
| B.每生成1.12LCl2,转移电子的物质的量为0.1 mol |
| C.每消耗8.7 gMnO2,被氧化的HCl的物质的量为0.2mol |
| D.生成的Cl2中,除含有一些水蒸气外,还含有HCl杂质 |
您最近一年使用:0次
解题方法
4 . 下列离子方程式正确的是
A.大理石与醋酸反应:CO +2CH3COOH=2CH3COOˉ+H2O+CO2↑ +2CH3COOH=2CH3COOˉ+H2O+CO2↑ |
B.高锰酸钾与浓盐酸制氯气的反应:MnO +4Clˉ+8H+=Mn2++2Cl2↑+4H2O +4Clˉ+8H+=Mn2++2Cl2↑+4H2O |
| C.金属钠和水反应:Na+2H2O=Na++2OHˉ+H2↑ |
D.过量氢氧化钙溶液与碳酸氢钠溶液反应:OHˉ+Ca2++HCO =CaCO3↓+H2O =CaCO3↓+H2O |
您最近一年使用:0次
5 . 下列装置或操作能达到实验目的的是
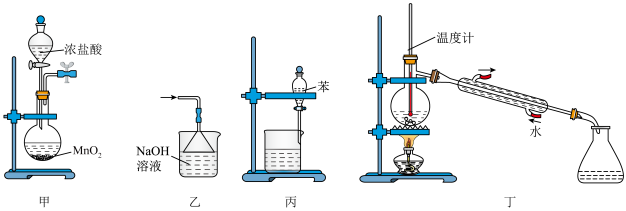

| A.用甲装置制取氯气 | B.用乙装置除去氯气中的HCl气体 |
| C.用丙装置分离苯和水 | D.用丁装置模拟海水淡化 |
您最近一年使用:0次
6 . 请回答:
(1) 的电子式是
的电子式是______ ;漂白粉的有效成分是______ (用化学式表示)。
(2)足量 通入品红溶液,可观察到的现象是
通入品红溶液,可观察到的现象是____________ 。
(3)实验室制备氯气的离子方程式是____________ 。
(1)
 的电子式是
的电子式是(2)足量
 通入品红溶液,可观察到的现象是
通入品红溶液,可观察到的现象是(3)实验室制备氯气的离子方程式是
您最近一年使用:0次
2024-03-01更新
|
128次组卷
|
2卷引用:浙江省绍兴市第一中学2023-2024学年高一下学期回头考试化学试题
名校
解题方法
7 . 高铁酸盐是优良的多功能水处理剂。某实验小组采用如图装置制备高铁酸钾(K2FeO4)并探究其性质用途。
资料:K2FeO4为紫色固体,微溶于KOH溶液,难溶于有机溶剂;具有强氧化性,在酸性或中性溶液中紫色快速褪去并产生O2,在碱性溶液中较稳定。
制备K2FeO4(夹持、加热等装置略)

(1)B中所用试剂为_____
(2)C中反应为放热反应,而反应温度须控制在0~8℃,可使用的控温方法为_____ ,充分反应后得到紫色固体,化学方程式为_____ 。
(3)C中混合物经过滤、洗涤、干燥,得纯净高铁酸钾晶体,洗涤时洗涤剂可选用_____ 。
a.冰水 b.KOH溶液 c.异丙醇
(4)反应中KOH必须过量的原因是_____ 。
资料:K2FeO4为紫色固体,微溶于KOH溶液,难溶于有机溶剂;具有强氧化性,在酸性或中性溶液中紫色快速褪去并产生O2,在碱性溶液中较稳定。
制备K2FeO4(夹持、加热等装置略)

(1)B中所用试剂为
(2)C中反应为放热反应,而反应温度须控制在0~8℃,可使用的控温方法为
(3)C中混合物经过滤、洗涤、干燥,得纯净高铁酸钾晶体,洗涤时洗涤剂可选用
a.冰水 b.KOH溶液 c.异丙醇
(4)反应中KOH必须过量的原因是
您最近一年使用:0次
8 . 人类社会的发展离不开科学家的贡献,下列说法中不正确的是
| A.道尔顿提出原子学说,认为原子是不可再分的实心球体 |
| B.汤姆生提出电子在原子核周围沿着不同的轨道运转,就像行星绕太阳 |
| C.门捷列夫在前人研究的基础上制出了第一张元素周期表 |
| D.戴维确认舍勒制得的黄绿色气体是一种新元素组成的单质——氯气 |
您最近一年使用:0次
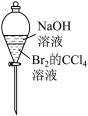
9 . 下列装置能达到实验目的的是
| A | B |
|
|
| 用此方法可较长时间看到Fe(OH)2白色沉淀 | 除CCl4中的Br2 |
| C | D |
|
|
| 实验室制取Cl2 | 氧化碘离子 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 氯气常用于自来水的杀菌消毒,实验室常用 和浓盐酸共热制备氯气。
和浓盐酸共热制备氯气。
(1)若 和
和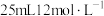 盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量
盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量 溶液,生成AgCl沉淀物质的量为___________(不考虑盐酸的挥发)
溶液,生成AgCl沉淀物质的量为___________(不考虑盐酸的挥发)
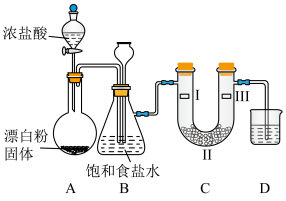
(2)若改用漂白粉与浓盐酸反应制备氯气,反应的化学方程式为 ,装置如图所示,同时验证氯气性质(其中夹持装置已省略)。
,装置如图所示,同时验证氯气性质(其中夹持装置已省略)。
①从反应条件看, 和
和 的氧化能力不同,氧化能力较强的是
的氧化能力不同,氧化能力较强的是___________ 。
②装置B除了用于除去挥发的HCl,也是安全瓶,目的是监测实验进行时装置C中是否发生堵塞,请写出装置C中发生堵塞时装置B中的实验现象:___________ 。
③装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是___________ (填字母)。
④装置D中为NaOH溶液,其作用是___________ (用化学方程式表示)。
(3)用氯气对自来水消毒易产生致癌物质,二氧化氯是一种更为高效安全的消毒剂。工业上制备 的反应为
的反应为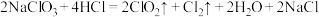 。
。
①其中氧化剂和还原剂的物质的量之比为___________ 。
② 在杀菌消毒的过程中会生成副产物亚氯酸盐(
在杀菌消毒的过程中会生成副产物亚氯酸盐( ),需要将其转化为
),需要将其转化为 除去,下列试剂能实现其转化过程的是
除去,下列试剂能实现其转化过程的是___________ (填序号)。
A. B.
B. C.KI D.
C.KI D.
 和浓盐酸共热制备氯气。
和浓盐酸共热制备氯气。(1)若
 和
和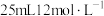 盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量
盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量 溶液,生成AgCl沉淀物质的量为___________(不考虑盐酸的挥发)
溶液,生成AgCl沉淀物质的量为___________(不考虑盐酸的挥发)| A.等于0.15mol | B.小于0.15mol |
| C.大于0.15mol,小于0.3mol | D.以上结论都不正确 |
(2)若改用漂白粉与浓盐酸反应制备氯气,反应的化学方程式为
 ,装置如图所示,同时验证氯气性质(其中夹持装置已省略)。
,装置如图所示,同时验证氯气性质(其中夹持装置已省略)。
①从反应条件看,
 和
和 的氧化能力不同,氧化能力较强的是
的氧化能力不同,氧化能力较强的是②装置B除了用于除去挥发的HCl,也是安全瓶,目的是监测实验进行时装置C中是否发生堵塞,请写出装置C中发生堵塞时装置B中的实验现象:
③装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是
| Ⅰ | Ⅱ | Ⅲ | |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(3)用氯气对自来水消毒易产生致癌物质,二氧化氯是一种更为高效安全的消毒剂。工业上制备
 的反应为
的反应为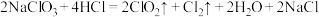 。
。①其中氧化剂和还原剂的物质的量之比为
②
 在杀菌消毒的过程中会生成副产物亚氯酸盐(
在杀菌消毒的过程中会生成副产物亚氯酸盐( ),需要将其转化为
),需要将其转化为 除去,下列试剂能实现其转化过程的是
除去,下列试剂能实现其转化过程的是A.
 B.
B. C.KI D.
C.KI D.
您最近一年使用:0次
2023-12-11更新
|
71次组卷
|
2卷引用:浙江省绍兴市第一中学2023-2024学年高一上学期11月期中考试(平行班)化学试题