1 . 下列实验装置使用正确的是
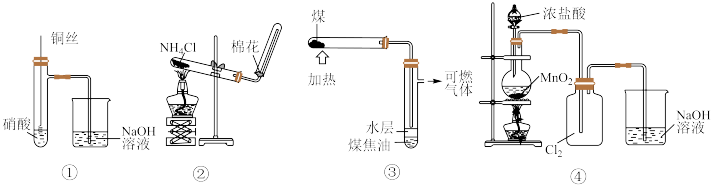
| A.图①装置用于铜和稀硝酸反应的探究实验 | B.图②装置用于实验室制备 |
| C.图③装置用于煤的气化实验 | D.图④装置用于实验室制备 |
您最近半年使用:0次
7日内更新
|
232次组卷
|
2卷引用:浙江绍兴市2023-2024学年高三下学期选考科目适应性考试化学试题
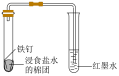
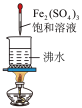
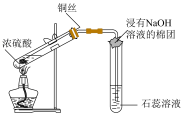
2 . 利用下列装置(夹持装置省略)进行实验,能达到实验目的的是
|
|
| A.证明氯水中有酸 | B.观察铁的的吸氧腐蚀 |
|
|
| C.制备Fe(OH)3胶体 | D.检验二氧化硫的漂白性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
3 . 三氧化二铬 是一种绿色固体,常作颜料。以它为原料实现如下转化:
是一种绿色固体,常作颜料。以它为原料实现如下转化:
②沉淀E溶于浓的强碱。
③在二价锰盐中,除少数 、
、 难溶与水外,其余大部分易溶于水。
难溶与水外,其余大部分易溶于水。
(1)写出溶液B中的所有阳离子__________ 。写出步骤Ⅱ中生成气体C的离子方程式__________ 。沉淀E的化学式为__________ 。
(2)下列说法正确的是__________。
(3)在碱性条件下, 具有强还原剂,可被
具有强还原剂,可被 氧化为最高价,写出两者恰好反应的离子方程式
氧化为最高价,写出两者恰好反应的离子方程式__________ 。根据该反应原理,设计实验检验上述反应后溶液中生成的阴离子__________ 。
 是一种绿色固体,常作颜料。以它为原料实现如下转化:
是一种绿色固体,常作颜料。以它为原料实现如下转化: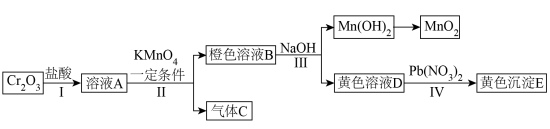
②沉淀E溶于浓的强碱。
③在二价锰盐中,除少数
 、
、 难溶与水外,其余大部分易溶于水。
难溶与水外,其余大部分易溶于水。(1)写出溶液B中的所有阳离子
(2)下列说法正确的是__________。
| A.气体C在工业上可通过电解法制备 |
| B.在溶液B中加入乙醇,溶液变为绿色,再变为蓝色 |
| C.将步骤Ⅰ中的盐酸换成硫酸,仅影响步骤Ⅱ的反应 |
| D.在步骤Ⅲ中,溶液B加入纯碱溶液,也能分离出锰元素 |
(3)在碱性条件下,
 具有强还原剂,可被
具有强还原剂,可被 氧化为最高价,写出两者恰好反应的离子方程式
氧化为最高价,写出两者恰好反应的离子方程式
您最近半年使用:0次
名校
4 . 氯气和亚氯酸钠(NaClO2)都是重要的漂白剂。
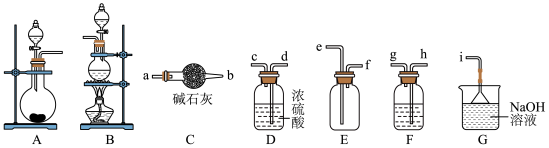
(I)某小组以KMnO4和浓盐酸为原料制备干燥、纯净的氯气___________ 。
(2)制备氯气时,可选用的发生装置为___________ (填序号),选择上述合适的装置,其连接顺序为:发生装置→___________ →i(按气流方向,用小写字母表示)。
(3)F装置所盛溶液是___________ (填溶液名称)。
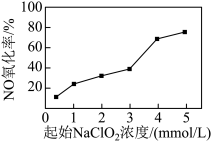
(II)工业上NaClO2可由ClO2、H2O2和NaOH溶液混合制得,实验流程如下:___________ 。
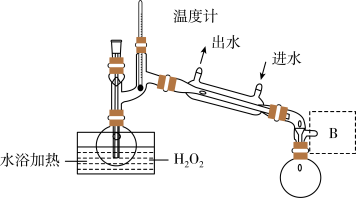
(5)已知H2O2(沸点150℃)浓度对反应速率有影响。通过下图所示装置将少量30% H2O2溶液浓缩至40%,B处应增加一个设备。该设备的作用是___________ 。___________ 。
(I)某小组以KMnO4和浓盐酸为原料制备干燥、纯净的氯气
(2)制备氯气时,可选用的发生装置为
(3)F装置所盛溶液是
(II)工业上NaClO2可由ClO2、H2O2和NaOH溶液混合制得,实验流程如下:

(5)已知H2O2(沸点150℃)浓度对反应速率有影响。通过下图所示装置将少量30% H2O2溶液浓缩至40%,B处应增加一个设备。该设备的作用是
您最近半年使用:0次
解题方法
5 . 氯气常用于自来水的杀菌消毒,实验室常用MnO2和浓盐酸共热制备氯气。
(1)若0.1mol∙L-1 MnO2和25mL12mol∙L-1盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量为___________(不考虑盐酸的挥发)
(2)若改用漂白粉与浓盐酸反应制备氯气,装置如图所示,同时验证氯气性质(其中夹持装置已省略)。___________ 。
②从反应条件看,MnO2和Ca(ClO)2的氧化能力不同,氧化能力较强的是___________ 。
③装置B除了用于除去挥发的HCl,也是安全瓶,目的是监测实验进行时装置C中是否发生堵塞,请写出装置C中发生堵塞时装置B中的实验现象___________ 。
④装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是___________ (填字母)。
(3)用氯气对自来水消毒易产生致癌物质,二氧化氯是一种更为高效安全的消毒剂。工业上制备ClO2的反应为2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①其中氧化剂和还原剂的物质的量之比为___________ 。
②ClO2在杀菌消毒的过程中会生成副产物亚氯酸盐( ),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是
),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是___________ (填序号)。
A.O2 B.FeCl2 C.KI D.KMnO4
③常温常压下,ClO2的消毒能力是等体积Cl2的___________ 倍。(假设ClO2、Cl2全部都被还原为Cl-,没有其它的含氯产物生成)
(1)若0.1mol∙L-1 MnO2和25mL12mol∙L-1盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量为___________(不考虑盐酸的挥发)
| A.等于0.15mol | B.小于0.15mol |
| C.大于0.15mol,小于0.3mol | D.以上结论都不正确 |
(2)若改用漂白粉与浓盐酸反应制备氯气,装置如图所示,同时验证氯气性质(其中夹持装置已省略)。

②从反应条件看,MnO2和Ca(ClO)2的氧化能力不同,氧化能力较强的是
③装置B除了用于除去挥发的HCl,也是安全瓶,目的是监测实验进行时装置C中是否发生堵塞,请写出装置C中发生堵塞时装置B中的实验现象
④装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是
| Ⅰ | Ⅱ | Ⅲ | |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(3)用氯气对自来水消毒易产生致癌物质,二氧化氯是一种更为高效安全的消毒剂。工业上制备ClO2的反应为2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①其中氧化剂和还原剂的物质的量之比为
②ClO2在杀菌消毒的过程中会生成副产物亚氯酸盐(
 ),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是
),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是A.O2 B.FeCl2 C.KI D.KMnO4
③常温常压下,ClO2的消毒能力是等体积Cl2的
您最近半年使用:0次
解题方法
6 . 下列说法不正确的是
| A.侯德榜是我国著名化工专家,发明了侯氏制碱法 |
| B.舍勒发现了一种黄绿色气体,戴维确认该气体为氯气 |
| C.屠呦呦——从青蒿中提取青蒿素 |
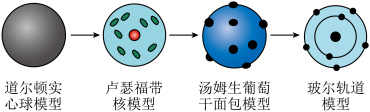
| D.原子结构模型演变历史可以表示为如图 |
您最近半年使用:0次
解题方法
7 . 高锰酸钾( )为紫黑色固体小颗粒,易溶于水,是一种强氧化剂。
)为紫黑色固体小颗粒,易溶于水,是一种强氧化剂。
查阅资料:①锰酸钾( )为墨绿色晶体,其水溶液呈深绿色,这是锰酸根(
)为墨绿色晶体,其水溶液呈深绿色,这是锰酸根( )
)
的特征颜色。其在浓的强碱溶液中可稳定存在,碱性减弱时易发生歧化反应。
②一些物质溶解度随温度变化单位: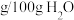
某实验小组设计如下实验步骤用 制备
制备
I.高锰酸钾的制备
III.高锰酸钾的纯度测定
①准确称取 样品
样品 ,用容量瓶配成
,用容量瓶配成 溶液;②称取高纯度
溶液;②称取高纯度 固体
固体 ,全部置于
,全部置于 锥形瓶中,再加入
锥形瓶中,再加入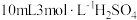 溶液和
溶液和 纯净水后盖上表面皿,于
纯净水后盖上表面皿,于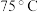 水浴加热振荡全部溶解;③用以上
水浴加热振荡全部溶解;③用以上 溶液趁热滴定。重复②~③,滴定3次。请回答:
溶液趁热滴定。重复②~③,滴定3次。请回答:
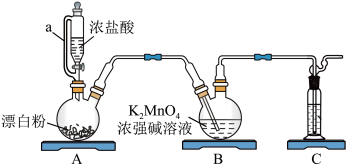
(1)装置a的名称是___________ ,其作用①是平衡气压使液体按一定的速率顺利流下;②是___________ 。
(2)装置A中漂白粉可用___________代替。
(3)上述装置存在一处缺陷导致 产率降低,改进的方法是
产率降低,改进的方法是___________ 。
(4)步骤Ⅱ为了获得杂质较少的 晶体,从下列选项中选出合理的操作并排序:将装置B中的溶液转移至蒸发皿中→
晶体,从下列选项中选出合理的操作并排序:将装置B中的溶液转移至蒸发皿中→___________ →___________ →___________ →___________ →干燥→ 晶体
晶体
a.用少量冰水洗涤 b.先用冰水洗涤,再用乙醇洗涤 c.小火蒸发至析出大量晶体,停止加热
d.小火蒸发至溶液表面出现晶膜,停止加热 e.减压过滤 f.趁热过滤 g.缓慢降温结晶
(5)下列说法正确的是___________。
(6)某次滴定,称取 固体质量
固体质量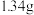 ,消耗
,消耗 溶液体积
溶液体积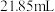 ,计算该次滴定实验测得的高锰酸钾含量是
,计算该次滴定实验测得的高锰酸钾含量是___________  (精确到小数点后两位)。
(精确到小数点后两位)。
 )为紫黑色固体小颗粒,易溶于水,是一种强氧化剂。
)为紫黑色固体小颗粒,易溶于水,是一种强氧化剂。查阅资料:①锰酸钾(
 )为墨绿色晶体,其水溶液呈深绿色,这是锰酸根(
)为墨绿色晶体,其水溶液呈深绿色,这是锰酸根( )
)的特征颜色。其在浓的强碱溶液中可稳定存在,碱性减弱时易发生歧化反应。
②一些物质溶解度随温度变化单位:
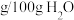
| 物质 | 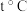 | |||||
| 0 | 20 | 40 | 60 | 70 | 80 | |
 | 28 | 34.2 | 40.1 | 45.8 | 47.2 | 51.3 |
 | 2.8 | 6.4 | 12.6 | 22.2 | —— | —— |
 制备
制备
I.高锰酸钾的制备
III.高锰酸钾的纯度测定
①准确称取
 样品
样品 ,用容量瓶配成
,用容量瓶配成 溶液;②称取高纯度
溶液;②称取高纯度 固体
固体 ,全部置于
,全部置于 锥形瓶中,再加入
锥形瓶中,再加入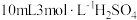 溶液和
溶液和 纯净水后盖上表面皿,于
纯净水后盖上表面皿,于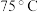 水浴加热振荡全部溶解;③用以上
水浴加热振荡全部溶解;③用以上 溶液趁热滴定。重复②~③,滴定3次。请回答:
溶液趁热滴定。重复②~③,滴定3次。请回答:(1)装置a的名称是
(2)装置A中漂白粉可用___________代替。
A. | B. | C. | D.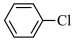 |
(3)上述装置存在一处缺陷导致
 产率降低,改进的方法是
产率降低,改进的方法是(4)步骤Ⅱ为了获得杂质较少的
 晶体,从下列选项中选出合理的操作并排序:将装置B中的溶液转移至蒸发皿中→
晶体,从下列选项中选出合理的操作并排序:将装置B中的溶液转移至蒸发皿中→ 晶体
晶体a.用少量冰水洗涤 b.先用冰水洗涤,再用乙醇洗涤 c.小火蒸发至析出大量晶体,停止加热
d.小火蒸发至溶液表面出现晶膜,停止加热 e.减压过滤 f.趁热过滤 g.缓慢降温结晶
(5)下列说法正确的是___________。
A.步骤I装置C中应盛放浓 |
| B.轻轻摇动装置B,若容器内壁未见暗绿色,说明反应完全 |
C.步骤III中的 可用 可用 或 或 代替 代替 |
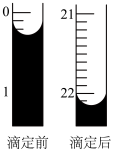
D.一次平行操作滴定前与滴定后(终点)读数如右图,则本次消耗的 溶液体积为 溶液体积为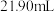 |
(6)某次滴定,称取
 固体质量
固体质量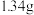 ,消耗
,消耗 溶液体积
溶液体积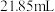 ,计算该次滴定实验测得的高锰酸钾含量是
,计算该次滴定实验测得的高锰酸钾含量是 (精确到小数点后两位)。
(精确到小数点后两位)。
您最近半年使用:0次
8 . 已知:K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O,按要求完成下列空格。
(1)用单线桥标明电子转移方向和数目______ 。
(2)该反应中氧化剂是______ 。
(3)该反应在标况下生成2.24L氯气时,转移电子______ 个。
(1)用单线桥标明电子转移方向和数目
(2)该反应中氧化剂是
(3)该反应在标况下生成2.24L氯气时,转移电子
您最近半年使用:0次
9 . 回答下列问题
(1)①写出小苏打的化学式___________ ;
②写出Fe2+的价电子排布式___________ 。
(2)实验室用软锰矿和浓盐酸制氯气,写出该反应的化学方程式___________ 。
(3)在常温下,0.1mol/LCH3COONa溶液的pH=9,则溶液中由水电离出来的c(OH-)=___________
(4)火箭发射可以用肼(N2H4,液态)作燃料,NO2作氧化剂,两者反应生成N2和水蒸气。
已知:N2(g)+2O2(g)=2NO2(g) ΔH1=+66.4kJ/mol
N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ/mol
请写出N2H4(l)与NO2反应的热化学方程式___________
(5)下表列出了某短周期元素R的各级电离能数据(用I1、I2……表示)。
关于元素R的下列推断中,正确的是___________ (用相应的编号填写)
①R元素基态原子的电子排布式为1s22s2
②R元素位于元素周期表中第ⅡA族
③R元素的最高正化合价为+2价
④R元素的第一电离能高于同周期相邻元素的第一电离能
(1)①写出小苏打的化学式
②写出Fe2+的价电子排布式
(2)实验室用软锰矿和浓盐酸制氯气,写出该反应的化学方程式
(3)在常温下,0.1mol/LCH3COONa溶液的pH=9,则溶液中由水电离出来的c(OH-)=
(4)火箭发射可以用肼(N2H4,液态)作燃料,NO2作氧化剂,两者反应生成N2和水蒸气。
已知:N2(g)+2O2(g)=2NO2(g) ΔH1=+66.4kJ/mol
N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ/mol
请写出N2H4(l)与NO2反应的热化学方程式
(5)下表列出了某短周期元素R的各级电离能数据(用I1、I2……表示)。
| 元素 | 电离能/(kJ·mol-1) | |||||
| I1 | I2 | I3 | I4 | I5 | …… | |
| R | 740 | 1500 | 7700 | 10500 | 13630 | …… |
①R元素基态原子的电子排布式为1s22s2
②R元素位于元素周期表中第ⅡA族
③R元素的最高正化合价为+2价
④R元素的第一电离能高于同周期相邻元素的第一电离能
您最近半年使用:0次
10 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.含0.4molHCl的盐酸与足量MnO2加热反应生成氯气,转移电子数为0.2NA |
| B.标准状况下,2.24LH2O中含有H-O数目为0.2NA |
| C.0.1mol·L-1的Na2CO3溶液中阴离子数目一定小于0.1NA |
| D.常温下1LpH=2的硫酸溶液中H+的数目为0.01NA |
您最近半年使用:0次