1 . 化学实验的微型化可有效地减少污染,实现化学实验绿色化的要求。某学生按下列操作做一个实验:
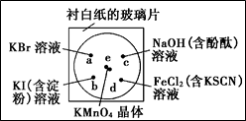
在一块下衬白纸的玻璃片的不同位置分别滴加浓度为0.1 mol/L的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,每种液滴彼此分开,围成半径小于表面皿的圆形(如下图所示),在圆心处放置2粒芝麻粒大小的KMnO4晶体,向KMnO4晶体滴加一滴浓盐酸,KMnO4晶体迅速溶解,然后产生气体,立即将表面皿盖好。
已知:2KMnO4 + 16HCl(浓) == 2KCl + 2MnCl2 + 5Cl2↑+ 8H2O ]。
(1) e处反应的离子方程式为____________ 。
该反应中氧化剂和还原剂的物质的量之比为____________ 。
(2) b处的实验现象为____________ ,d处的实验现象为____________ 。
(3) c处反应的化学方程式为____________ 。标准状况下,当有0.224 L Cl2被NaOH溶液吸收后,转移电子的个数约为____________ 。
(4) 通过该实验能否比较Cl2、FeCl3、KMnO4三种物质氧化性的强弱?
____________ (填“能”或“不能”),若能,其氧化性由强到弱的顺序是____________ 。
在一块下衬白纸的玻璃片的不同位置分别滴加浓度为0.1 mol/L的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,每种液滴彼此分开,围成半径小于表面皿的圆形(如下图所示),在圆心处放置2粒芝麻粒大小的KMnO4晶体,向KMnO4晶体滴加一滴浓盐酸,KMnO4晶体迅速溶解,然后产生气体,立即将表面皿盖好。

已知:2KMnO4 + 16HCl(浓) == 2KCl + 2MnCl2 + 5Cl2↑+ 8H2O ]。
(1) e处反应的离子方程式为
该反应中氧化剂和还原剂的物质的量之比为
(2) b处的实验现象为
(3) c处反应的化学方程式为
(4) 通过该实验能否比较Cl2、FeCl3、KMnO4三种物质氧化性的强弱?
您最近一年使用:0次



