解题方法
1 . 用NA表示阿伏加德罗常数,下列说法错误的是
A.将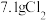 通入足量氢氧化钠溶液中,转移电子数为 通入足量氢氧化钠溶液中,转移电子数为 |
B.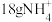 所含的电子数目为 所含的电子数目为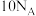 |
C.含0.2mol FeCl3的氯化铁饱和溶液滴入沸水充分反应形成的 胶体粒子数小于0.2NA 胶体粒子数小于0.2NA |
D. 在空气中完全燃烧生成MgO和Mg3N2的混合物,转移的电子数为 在空气中完全燃烧生成MgO和Mg3N2的混合物,转移的电子数为 |
您最近一年使用:0次
名校
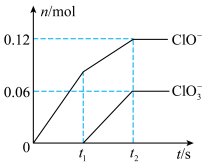
2 . 将一定量的 通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中
通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中 和
和 两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法不正确的是
两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法不正确的是
 通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中
通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中 和
和 两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法不正确的是
两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法不正确的是
A.溶液中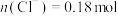 |
B.原KOH溶液中,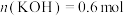 |
| C.反应中转移电子的物质的量是0.42mol |
D.依据图像,总的离子反应方程式为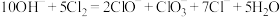 |
您最近一年使用:0次
2023-08-21更新
|
355次组卷
|
3卷引用:四川省眉山市仁寿第一中学校南校区2023-2024学年高一下学期3月月考化学试题
名校
3 . 按下图装置进行实验,探究氯气的性质,下列说法正确的是
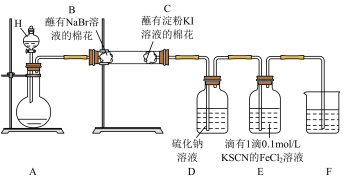

| A.仪器H的名称为分液漏斗,可用长颈漏斗替换 |
| B.C中棉花变蓝,说明氯气置换出碘,则非金属性:Cl>I, |
| C.E中溶液先变红后褪色,说明Cl2有漂白性 |
| D.F中溶液为NaOH溶液,进行尾气处理 |
您最近一年使用:0次
2023-08-08更新
|
307次组卷
|
2卷引用:四川省仁寿第一中学校南校区2023-2024学年高三上学期开学考试化学试题
名校
解题方法
4 . 设 是阿伏加德罗常数的值。下列说法错误的是
是阿伏加德罗常数的值。下列说法错误的是
 是阿伏加德罗常数的值。下列说法错误的是
是阿伏加德罗常数的值。下列说法错误的是A.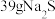 和 和 组成的混合物中,含有阴离子的数目为0.5NA 组成的混合物中,含有阴离子的数目为0.5NA |
| B.密闭容器中,1mol N2(g)与3mol H2(g)充分反应制备氨气,形成N−H键少于6NA |
C.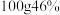 的乙醇溶液中,含 的乙醇溶液中,含 键的数目为 键的数目为 |
D.在标况下将 溶于足量 溶于足量 溶液中,转移电子数目为 溶液中,转移电子数目为 |
您最近一年使用:0次
2023-06-19更新
|
95次组卷
|
2卷引用:四川省仁寿第一中学校南校区2023-2024学年高二上学期10月月考化学试题
名校
5 . 高铁酸钾(K2FeO4)是一种高效多功能的新型非氯绿色消毒剂。其溶于水与水结合放出氧气并有絮状沉淀产生,常用作净水剂。其生产工艺如下:
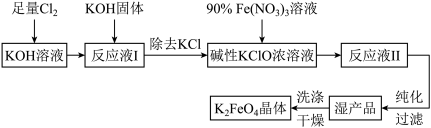
回答下列问题:
(1)写出Cl2与KOH溶液反应的化学方程式___________ 。
(2)在“反应液I”中加入KOH固体的目的是___________ 。
(3)写出Fe(NO3)3溶液与碱性KClO溶液反应的离子方程式___________ 。
(4)K2FeO4可作为新型多功能水处理剂的原因是___________ 。
(5)从“反应液II”中分离出K2FeO4后,副产品有___________ (写化学式)。实验室模拟工业流程中“过滤”操作用到的主要玻璃仪器有___________ 。
(6)该工艺每得到1.98kg K2FeO4,理论上消耗Cl2的物质的量为___________ mol。

回答下列问题:
(1)写出Cl2与KOH溶液反应的化学方程式
(2)在“反应液I”中加入KOH固体的目的是
(3)写出Fe(NO3)3溶液与碱性KClO溶液反应的离子方程式
(4)K2FeO4可作为新型多功能水处理剂的原因是
(5)从“反应液II”中分离出K2FeO4后,副产品有
(6)该工艺每得到1.98kg K2FeO4,理论上消耗Cl2的物质的量为
您最近一年使用:0次
2023-04-06更新
|
229次组卷
|
3卷引用:四川省眉山市2022-2023学年高二上学期期末教学质量检测理综化学试题
6 . 下列反应的离子方程式不正确 的是
A. 通入氢氧化钠溶液: 通入氢氧化钠溶液: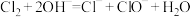 |
B.氧化铝溶于氢氧化钠溶液: |
C.过量 通入饱和碳酸钠溶液: 通入饱和碳酸钠溶液: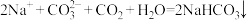 |
D. 溶液中滴入氯化钙溶液: 溶液中滴入氯化钙溶液: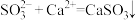 |
您最近一年使用:0次
2023-01-11更新
|
11082次组卷
|
20卷引用:四川省眉山市仁寿第一中学校(北校区)2023-2024学年高三上学期11月期中考试理综化学试题
四川省眉山市仁寿第一中学校(北校区)2023-2024学年高三上学期11月期中考试理综化学试题2023年1月浙江省普通高校招生选考化学试题(已下线)广东省东莞市2022-2023学年高三上学期期末教学质量检查变式汇编(11-16)(已下线)广东省广州市2022届高三一模考试(选择题11-16)(已下线)2023年1月浙江省普通高校招生选考变式题(选择题6-10)浙江省平阳县万全综合高级中学2022-2023学年高二下学期第一次月考化学试题 (已下线)专题卷05 离子方程式正误判断-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)专题04 离子反应(已下线)2023年高考化学真题完全解读(浙江1月)(已下线)专题04 离子反应(已下线)专题04 离子反应(已下线)第04练 离子共存 离子方程式的正误判断 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)第2讲 离子反应和离子方程式(已下线)【知识图鉴】单元讲练测必修第一册第一单元03巩固练(已下线)考点04 离子反应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)浙江省金华第一中学2022-2023学年高一下学期6月期末化学试题(已下线)专题04 离子方程式与离子共存-2023年高考化学真题题源解密(新高考专用)(已下线)广东省东莞市光正实验学校2023-2024学年高三上学期第二次月孝化学试题(已下线)选择题1-5上海市华东师范大学第二附属中学(紫竹校区)2023-2024学年高三下学期三模考试 化学试题
名校
解题方法
7 . 下列反应能达到目的且对应离子方程式正确的是
A.过氧化钠作供氧剂与水反应: |
B.向 溶液中滴入 溶液中滴入 溶液至产生的沉淀质量最大: 溶液至产生的沉淀质量最大:  |
C.将 通入澄清石灰水中制取漂粉精: 通入澄清石灰水中制取漂粉精: |
D.往 溶液中通入少量 溶液中通入少量 : :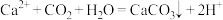 |
您最近一年使用:0次
2022-12-09更新
|
218次组卷
|
2卷引用:四川省眉山市仁寿第一中学校南校区2023-2024学年高一上学期开学化学试题
8 . I.某实验室需要配制500 mL0.10 mol/LNa2CO3溶液。
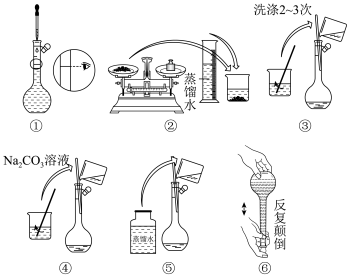
(1)所需玻璃仪器有:玻璃棒、烧杯、量筒、___________ 、 ___________ 。
(2)实验时图中所示操作的先后顺序为___________ (填编号)。
(3)在配制过程中,下列操作对所配溶液浓度如何?(填“偏高”、“偏低”或“无影响”)
①向容量瓶加水定容时俯视液面___________
②摇匀后液面下降,再加水至刻度线___________
(4)所需Na2CO3固体的质量为___________ g;若改用浓溶液稀释。需要量取2mol/LNa2CO3溶液___________ mL。
II.某研究小组制备消毒液(主要成分为NaClO)设计了图示装置
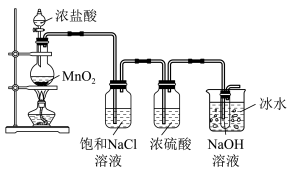
在阅资料得知;在加热情况下卤素单质和碱液发生反应:3X2+6OH- 5X + XO3+3H2O
5X + XO3+3H2O
回答下列问题:
(5)烧瓶中发生反应的化学方程式为___________ 。
(6)装置中饱和NaCl溶液的作用是___________ 。
(7)装置中能不能省去盛冰水的烧杯?___________ (填“ 能”或“不能”)。理由是___________ 。
(8)装置中的试管内发生反应的离子方程式为___________ 。

(1)所需玻璃仪器有:玻璃棒、烧杯、量筒、
(2)实验时图中所示操作的先后顺序为
(3)在配制过程中,下列操作对所配溶液浓度如何?(填“偏高”、“偏低”或“无影响”)
①向容量瓶加水定容时俯视液面
②摇匀后液面下降,再加水至刻度线
(4)所需Na2CO3固体的质量为
II.某研究小组制备消毒液(主要成分为NaClO)设计了图示装置

在阅资料得知;在加热情况下卤素单质和碱液发生反应:3X2+6OH-
 5X + XO3+3H2O
5X + XO3+3H2O回答下列问题:
(5)烧瓶中发生反应的化学方程式为
(6)装置中饱和NaCl溶液的作用是
(7)装置中能不能省去盛冰水的烧杯?
(8)装置中的试管内发生反应的离子方程式为
您最近一年使用:0次
名校
解题方法
9 . KMnO4和MnO2都是重要化学物质,在实验室可以做氧化剂和催化剂,某学习小组对两种物质的制备和性质探究如下:
Ⅰ.MnO2的制备:该学习小组设计了将粗MnO2(含有较多的MnO、MnCO3和Fe2O3)样品转化为纯MnO2实验,其工艺流程如下:

请回答下列问题:
(1)第①步操作中,生成CO2的化学方程式为___________
(2)第②步操作中,NaClO3氧化MnSO4的离子方程式为___________
(3)第③步操作中,最终得到的固体除NaClO3外,还一定含有的是___________
a.NaCl b.NaClO c.NaClO4 d.NaOH
(4)为得到纯净的MnO2,须将过滤后的MnO2合并后进行洗涤。洗涤沉淀所用的玻璃仪器有:___________ ,判断是否洗涤干净可选用的试剂是___________ (填化学式)。
(5)NaClO3和MnO2在一定条件下都可以氧化浓盐酸制取氯气,制取等量的氯气消耗NaClO3与MnO2的物质的量之比为___________
Ⅱ.KMnO4的制备和性质:
(6)该小组同学为了探究KMnO4溶液和Na2C2O4溶液的反应,将酸性KMnO4溶液逐滴滴入一定体积的Na2C2O4溶液中(温度相同,并不断振荡),记录现象如下:
① 请将MnO 氧化C2O
氧化C2O 的离子方程式补充完整:
的离子方程式补充完整:___________
___________MnO +___________C2O
+___________C2O +___________=___________Mn2++___________CO2↑+_________
+___________=___________Mn2++___________CO2↑+_________
② 请分析KMnO4溶液褪色时间变化的最可能原因___________
Ⅰ.MnO2的制备:该学习小组设计了将粗MnO2(含有较多的MnO、MnCO3和Fe2O3)样品转化为纯MnO2实验,其工艺流程如下:

请回答下列问题:
(1)第①步操作中,生成CO2的化学方程式为
(2)第②步操作中,NaClO3氧化MnSO4的离子方程式为
(3)第③步操作中,最终得到的固体除NaClO3外,还一定含有的是
a.NaCl b.NaClO c.NaClO4 d.NaOH
(4)为得到纯净的MnO2,须将过滤后的MnO2合并后进行洗涤。洗涤沉淀所用的玻璃仪器有:
(5)NaClO3和MnO2在一定条件下都可以氧化浓盐酸制取氯气,制取等量的氯气消耗NaClO3与MnO2的物质的量之比为
Ⅱ.KMnO4的制备和性质:
(6)该小组同学为了探究KMnO4溶液和Na2C2O4溶液的反应,将酸性KMnO4溶液逐滴滴入一定体积的Na2C2O4溶液中(温度相同,并不断振荡),记录现象如下:
| 滴入KMnO4溶液的次序 | KMnO4溶液紫色褪去所需的时间 |
| 先滴入第1滴 | 60s |
| 褪色后,再滴入第2滴 | 15s |
| 褪色后,再滴入第3滴 | 3s |
| 褪色后,再滴入第4滴 | 1s |
① 请将MnO
 氧化C2O
氧化C2O 的离子方程式补充完整:
的离子方程式补充完整:___________MnO
 +___________C2O
+___________C2O +___________=___________Mn2++___________CO2↑+_________
+___________=___________Mn2++___________CO2↑+_________② 请分析KMnO4溶液褪色时间变化的最可能原因
您最近一年使用:0次
名校
10 . 下列过程中的化学反应相应的离子方程式正确的是
| A.室温下用稀NaOH溶液吸收Cl2:Cl2+2OH−=ClO−+Cl−+H2O |
B.过量铁粉加入稀硝酸中:Fe+4H++ =Fe3++NO↑+2H2O =Fe3++NO↑+2H2O |
C.硫酸铝溶液中滴加少量氢氧化钾溶液:Al3++4OH-= +2H2O +2H2O |
| D.氯化铜溶液中通入硫化氢:Cu2++S2-=CuS↓ |
您最近一年使用:0次



