解题方法
1 . 按要求,回答下列问题:
(1)实验室用二氧化锰和浓盐酸反应制取氯气,反应的离子方程式是___________ 。
(2)氯气可用湿润的淀粉碘化钾试纸检验,请用化学方程式解释原因:___________ 。
(3)由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,工业上生产漂白粉的主要化学方程式是___________ 。
(4)家庭中使用漂白粉时,为了增强漂白能力,可加入少量的物质是___________。
(5)某同学在探究漂白粉溶液性质时,在漂白粉溶液中加入几滴无色酚酞溶液,发现溶液呈红色,随后溶液迅速褪色,说明漂白粉溶液呈___________ 性,并具有___________ 性。
(6)实验室也可用 固体和浓盐酸反应制氯气,反应方程式如下:
固体和浓盐酸反应制氯气,反应方程式如下: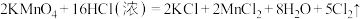 ,若反应中有0.5mol电子转移,被氧化HCl的物质的量为
,若反应中有0.5mol电子转移,被氧化HCl的物质的量为___________ 。
(1)实验室用二氧化锰和浓盐酸反应制取氯气,反应的离子方程式是
(2)氯气可用湿润的淀粉碘化钾试纸检验,请用化学方程式解释原因:
(3)由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,工业上生产漂白粉的主要化学方程式是
(4)家庭中使用漂白粉时,为了增强漂白能力,可加入少量的物质是___________。
| A.食醋 | B.食盐 | C.烧碱 | D.纯碱 |
(6)实验室也可用
 固体和浓盐酸反应制氯气,反应方程式如下:
固体和浓盐酸反应制氯气,反应方程式如下: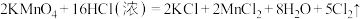 ,若反应中有0.5mol电子转移,被氧化HCl的物质的量为
,若反应中有0.5mol电子转移,被氧化HCl的物质的量为
您最近一年使用:0次
2022高一·全国·专题练习
解题方法
2 . 漂白粉长期露置于空气中,最终得到的物质是什么?写出反应的化学方程式。_______
您最近一年使用:0次
解题方法
3 . 科学的分类能够反映事物的本质特征,运用分类的方法,可以发现物质及其变化的规律。基于物质类别和元素价态,可以设计物质间转化的途径。请根据下列物质回答相关问题:
①小苏打 ②石墨 ③HCl ④酒精 ⑤FeCl3溶液 ⑥氧化钠
(1)上述物质中属于电解质的是_______ (填序号)
(2)Ⅰ.某同学用含钠元素的不同类别 物质制备NaCl。化学反应方程式如下:
a.2Na+Cl2 2NaCl
2NaCl
b.
c.NaOH+HCl=NaCl+H2O
d.
请从上述①~⑥中选择合适反应物补充b、d反应的化学反应方程式b:_______ ;d:_______ 。
Ⅱ.另一位同学从含氯元素的不同价态 考虑,认为Cl2与NaOH溶液反应也可以生成NaCl,请写出此方法的化学反应方程式_______ 。
(3)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,工业上制备Na2FeO4有多种方法,其中一种方法是用NaClO和⑤作为反应物在碱性环境下完成,此方法的化学原理可用离子反应方程式表示为:3ClO-+2Fe3++10OH-=2FeO +3Cl-+5H2O,该反应中氧化剂与还原剂的物质的量之比为
+3Cl-+5H2O,该反应中氧化剂与还原剂的物质的量之比为_______ ;请用单线桥法 在离子反应方程式上标出电子转移的方向和数目_______ 。
①小苏打 ②石墨 ③HCl ④酒精 ⑤FeCl3溶液 ⑥氧化钠
(1)上述物质中属于电解质的是
(2)Ⅰ.某同学用
a.2Na+Cl2
 2NaCl
2NaClb.
c.NaOH+HCl=NaCl+H2O
d.
请从上述①~⑥中选择合适反应物补充b、d反应的化学反应方程式b:
Ⅱ.另一位同学从
(3)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,工业上制备Na2FeO4有多种方法,其中一种方法是用NaClO和⑤作为反应物在碱性环境下完成,此方法的化学原理可用离子反应方程式表示为:3ClO-+2Fe3++10OH-=2FeO
 +3Cl-+5H2O,该反应中氧化剂与还原剂的物质的量之比为
+3Cl-+5H2O,该反应中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
4 . 实验室用二氧化锰和浓盐酸反应制取氯气并探究其性质,实验装置如图所示
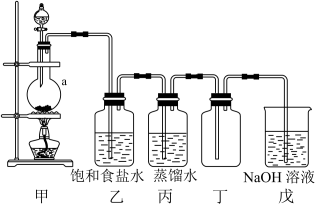
(1)仪器a的名称为___________ 。
(2)装置甲中发生反应的化学方程式为____ 。
(3)装置乙中饱和食盐水的作用是___________ 。
(4)装置丁中收集氯气的方法是___________ ,在装满氯气的集气瓶中放入红色鲜花,观察到鲜花褪色,原因是___________ 。
(5)装置戊中发生反应的离子方程式为___________ 。
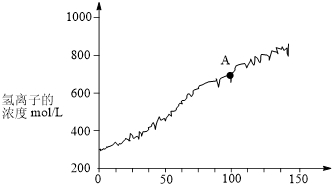
(6)充分反应后,将氯离子传感器插入广口瓶丙的溶液中,与数据采集器,计算机连接,用强光照射瓶中溶液,采集数据所得图象如图所示。
①A点溶液发生分解反应的离子方程式为___________ 。
②A点溶液中氯元素的存在形式有 和
和___________ 。


(1)仪器a的名称为
(2)装置甲中发生反应的化学方程式为
(3)装置乙中饱和食盐水的作用是
(4)装置丁中收集氯气的方法是
(5)装置戊中发生反应的离子方程式为
(6)充分反应后,将氯离子传感器插入广口瓶丙的溶液中,与数据采集器,计算机连接,用强光照射瓶中溶液,采集数据所得图象如图所示。
①A点溶液发生分解反应的离子方程式为
②A点溶液中氯元素的存在形式有
 和
和
您最近一年使用:0次
名校
5 . 请按要求回答下列问题:
(1)Al2O3能溶于强酸或强碱溶液生成盐和水,则Al2O3是一种_______ (填“酸性”、“碱性”或“两性”) 氧化物。
(2)氨气极易溶于水,其水溶液显_______ (填“酸”、“碱”或“中”)性。
(3)在常温下,将Cl2通入NaOH溶液中,可以得到漂白液。请写出该反应的离子方程式_______ 。
(4)高锰酸钾与浓盐酸在常温下能反应生成氯气,请写出反应的化学方程式_______ 。
(5)等质量的下列气体HCl、NH3、CO2、O2四种气体中,在相同温度和相同压强条件下,体积最大的是_______ 。
(6)设NA为阿伏加德罗常数的数值,如果ag某未知气体中含有的分子数为b,则cg该气体在标准状况下的体积约是_______ L (用NA的式子表示)。
(1)Al2O3能溶于强酸或强碱溶液生成盐和水,则Al2O3是一种
(2)氨气极易溶于水,其水溶液显
(3)在常温下,将Cl2通入NaOH溶液中,可以得到漂白液。请写出该反应的离子方程式
(4)高锰酸钾与浓盐酸在常温下能反应生成氯气,请写出反应的化学方程式
(5)等质量的下列气体HCl、NH3、CO2、O2四种气体中,在相同温度和相同压强条件下,体积最大的是
(6)设NA为阿伏加德罗常数的数值,如果ag某未知气体中含有的分子数为b,则cg该气体在标准状况下的体积约是
您最近一年使用:0次
6 . 氯气是一种化学性质活泼的气体。
(1)氯气是一种具有_______ 气味的气体,密度比空气的_______ (填“大”或“小”),若采用如图装置收集氯气,则氯气应由_______ 管(填“A”或“B”)通入。
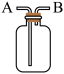
(2)氯气与NaOH溶液反应的化学方程式为_______ ,该反应可用于工业上制取漂白液,其有效成分是_______ 。
(1)氯气是一种具有

(2)氯气与NaOH溶液反应的化学方程式为
您最近一年使用:0次
名校
7 . 新型冠状病毒肺炎爆发以来,各类杀菌消毒剂逐渐被人们所认识和使用。下列是常见的几种消毒剂:①“84”消毒液(有效成分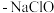 );②
);② (在水中一部分可以电离出正、负离子);③漂白粉;④
(在水中一部分可以电离出正、负离子);③漂白粉;④ ⑤
⑤ ;⑥碘酒;⑦
;⑥碘酒;⑦ 酒精;⑧过氧乙酸
酒精;⑧过氧乙酸 ⑨高铁酸钠
⑨高铁酸钠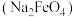 。回答下列问题:
。回答下列问题:
(1)上述杀菌消毒剂___________ (填序号)属于电解质,___________ (填序号)属于非电解质。“84”消毒液中有效成分的电离方程式为___________ 。
(2)巴西奥运会期间,由于工作人员将“84"消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能原因是NaClO与H2O2反应产生O2促进藻类快速生长。该反应说明氧化性:NaClO___________ H2O2(填“>”或“<”)。
(3)若混合使用“洁厕灵”(盐酸是成分之一)与84消毒液会产生氯气。原因是___________ (用离子方程式表示)。
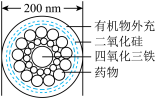
(4)如图是中国科学院上海硅酸盐研究所研发的“纳米药物分子运输车”,可提高肿瘤的治疗效果。以下说法不正确的是___________。
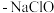 );②
);② (在水中一部分可以电离出正、负离子);③漂白粉;④
(在水中一部分可以电离出正、负离子);③漂白粉;④ ⑤
⑤ ;⑥碘酒;⑦
;⑥碘酒;⑦ 酒精;⑧过氧乙酸
酒精;⑧过氧乙酸 ⑨高铁酸钠
⑨高铁酸钠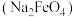 。回答下列问题:
。回答下列问题:(1)上述杀菌消毒剂
(2)巴西奥运会期间,由于工作人员将“84"消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能原因是NaClO与H2O2反应产生O2促进藻类快速生长。该反应说明氧化性:NaClO
(3)若混合使用“洁厕灵”(盐酸是成分之一)与84消毒液会产生氯气。原因是
(4)如图是中国科学院上海硅酸盐研究所研发的“纳米药物分子运输车”,可提高肿瘤的治疗效果。以下说法不正确的是___________。

| A.葡萄糖等大多数含碳化合物属于有机物 |
| B.该“纳米药物分子车"属于混合物 |
| C.该“纳米药物分子车”分散于水后能够透过半透膜 |
| D.该“纳米药物分子车”中的二氧化硅和四氧化三铁属于氧化物 |
您最近一年使用:0次
解题方法
8 . 海水中含有大量的卤族元素,具有十分巨大的开发利用潜力。
I.氯气是非常重要的化工产品
(1)用浓盐酸和二氧化锰制氯气是实验室常用的方法,写出该反应的化学方程式:_____ 。
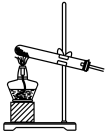
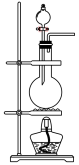
(2)也可用浓盐酸和高锰酸钾制氯气,反应方程式如下:2KMnO4+16HCl(浓)=KCl+2MnCl2+5Cl2↑+8H2O,实验室用该方法制氯气时,可选用的发生装置是___________ (写编号)。
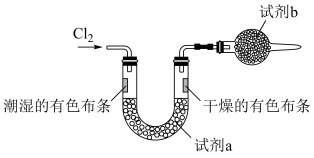
(3)为证明氯气与水反应产物具有漂白性,将Cl2缓缓通过下列装置:___________ ;试剂b的作用是___________ ;___________ 。
(4)通常使用84消毒液时需要把消毒对象在其中浸泡一段时间,以提高消毒效果。请结合反应方程式分析原因___________
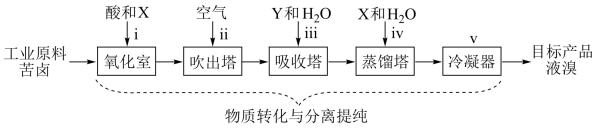
II.地球上99%的溴元素以Br-形式存在于海水中。海水中Br-含量约为65mg/L,而苦卤(海水晒盐后得到的母液)中Br-含量高很多,苦卤常作海水提溴的主要原料。目前最成熟的“空气吹出法”海水提溴工艺流程如图(已知:溴的沸点为59℃):___________ 。
(6)利用“空气吹出法”将“氧化室”产生的低浓度Br2分离出来的方法利用了溴的___________ 这一物理性质。
(7)将低浓度Br2富集为高浓度Br2历经步骤iii反应的离子方程式为:___________ 。
I.氯气是非常重要的化工产品
(1)用浓盐酸和二氧化锰制氯气是实验室常用的方法,写出该反应的化学方程式:
(2)也可用浓盐酸和高锰酸钾制氯气,反应方程式如下:2KMnO4+16HCl(浓)=KCl+2MnCl2+5Cl2↑+8H2O,实验室用该方法制氯气时,可选用的发生装置是
| 编号 | A | B | C |
| 发生装置 |
|
|
|
(4)通常使用84消毒液时需要把消毒对象在其中浸泡一段时间,以提高消毒效果。请结合反应方程式分析原因
II.地球上99%的溴元素以Br-形式存在于海水中。海水中Br-含量约为65mg/L,而苦卤(海水晒盐后得到的母液)中Br-含量高很多,苦卤常作海水提溴的主要原料。目前最成熟的“空气吹出法”海水提溴工艺流程如图(已知:溴的沸点为59℃):
(6)利用“空气吹出法”将“氧化室”产生的低浓度Br2分离出来的方法利用了溴的
(7)将低浓度Br2富集为高浓度Br2历经步骤iii反应的离子方程式为:
您最近一年使用:0次
2021-11-12更新
|
453次组卷
|
3卷引用:天津市五校联考2021-2022学年高三上学期期中考试化学试题
名校
解题方法
9 . 利用如图所示的“价-类”二维图,可以从不同角度认识含氯元素的物质的性质及其转化关系,图中甲~辛均为含氯元素的物质。回答下列问题:
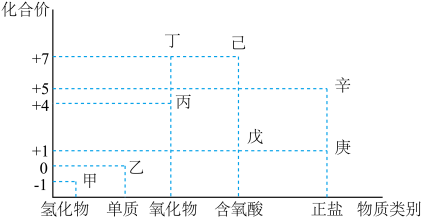
(1)丙的化学式为_____________ ;丁的化学式为_____________ 。
(2)甲、乙、丁、戊中,属于电解质的是__________________________ (填化学式);根据氯元素的化合价判断,乙____________________ (填标号)。
a.只有氧化性 b.既有氧化性又有还原性
c.只有还原性 d.既能作氧化剂又能作还原剂
(3)庚是漂白粉的有效成分,用乙制取漂白粉的化学方程式为____________________________ 。
(4)辛在 催化下受热分解可制备一种常见的气体,这种气体的化学式是
催化下受热分解可制备一种常见的气体,这种气体的化学式是______________ 。

(1)丙的化学式为
(2)甲、乙、丁、戊中,属于电解质的是
a.只有氧化性 b.既有氧化性又有还原性
c.只有还原性 d.既能作氧化剂又能作还原剂
(3)庚是漂白粉的有效成分,用乙制取漂白粉的化学方程式为
(4)辛在
 催化下受热分解可制备一种常见的气体,这种气体的化学式是
催化下受热分解可制备一种常见的气体,这种气体的化学式是
您最近一年使用:0次
2020-10-02更新
|
514次组卷
|
2卷引用:人教版(2019)高一必修第一册 第二章 海水中的重要元素 第二节 氯及其化合物 作业帮
10 . 利用分类法可以更系统、全面的认识物质的性质以及化学反应。
Ⅰ、有下列物质:①盐酸② ③
③ ④KOH溶液⑤
④KOH溶液⑤
(1)属于碱性氧化物的是___________ (填序号)。
(2)③属于___________ (填“共价”或“离子”)化合物。
(3)属于电解质的是___________ (填序号)。
(4)①和④反应的离子方程式是___________ 。
Ⅱ、有以下四个反应:①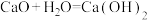 ②
②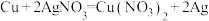
③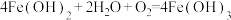 ④
④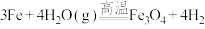
(5)不属于氧化还原反应的是___________ (填序号)。
(6)既是化合反应又是氧化还原反应的是___________ (填序号)。
Ⅲ、单质到盐的转化关系可表示为:A(单质)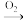 B(氧化物)
B(氧化物)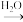 C
C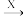 D(盐)。
D(盐)。
(7)若A是碳单质,则C的水溶液呈___________ (填“酸”、“碱”或“中”)性。
(8)若C→D的转化可用于工业制漂白粉,则物质X是___________ 。
(9)若B是一种淡黄色固体,X是 ,则B的用途是
,则B的用途是___________ (举一例),D的化学式可能是___________ 。
Ⅰ、有下列物质:①盐酸②
 ③
③ ④KOH溶液⑤
④KOH溶液⑤
(1)属于碱性氧化物的是
(2)③属于
(3)属于电解质的是
(4)①和④反应的离子方程式是
Ⅱ、有以下四个反应:①
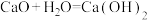 ②
②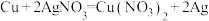
③
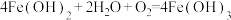 ④
④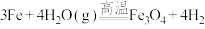
(5)不属于氧化还原反应的是
(6)既是化合反应又是氧化还原反应的是
Ⅲ、单质到盐的转化关系可表示为:A(单质)
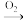 B(氧化物)
B(氧化物)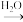 C
C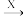 D(盐)。
D(盐)。(7)若A是碳单质,则C的水溶液呈
(8)若C→D的转化可用于工业制漂白粉,则物质X是
(9)若B是一种淡黄色固体,X是
 ,则B的用途是
,则B的用途是
您最近一年使用:0次