1 . 氮化铬(CrN)是一种良好的耐磨材料,实验室可用如下装置进行模拟制备(省略夹持装置):

Ⅰ.完成下列填空:
(1)干燥的NH3可选用以下装置制得,相应的连接顺序可以是_______→_______→_______(选填端口字母编号)。_______
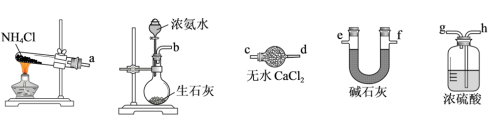
Ⅱ.固体X可用无水氯化铬(CrCl3)固体,主要反应为NH3+CrCl3 CrN+3HCl。
CrN+3HCl。
(2)无水氯化铬具有很强的吸水性,通常形成晶体CrCl3·6H2O。直接加热脱水往往得到Cr2O3,有关反应的化学方程式为_______ 。以氯化铬晶体制备无水氯化铬的方法是_______ 。
(3)实际进行实验时,发现上述装置存在一个缺陷,会导致危险,请简要说明。_______
Ⅲ.固体X也可用Cr2O3固体。通入NH3时先将氧化物还原为金属单质,然后金属单质与另一产物化合得到CrN,这些过程几乎同时进行。
(4)写出NH3与Cr2O3发生氧化还原反应的化学方程式:_______ 。
(5)CrN产品中含有Cr2N杂质,可利用如下方法进行纯度测定:取样品14.380g在空气中充分加热至反应完全,剩余固体全为Cr2O3,质量为16.720g。样品中CrN与Cr2N的物质的量之比为_______ 。
(6)证明样品已反应完全的操作名称是_______ ;若加热时长不足,则最终测定CrN的纯度将_______ (选填“偏大”“偏小”或“不变”)。

Ⅰ.完成下列填空:
(1)干燥的NH3可选用以下装置制得,相应的连接顺序可以是_______→_______→_______(选填端口字母编号)。

Ⅱ.固体X可用无水氯化铬(CrCl3)固体,主要反应为NH3+CrCl3
 CrN+3HCl。
CrN+3HCl。(2)无水氯化铬具有很强的吸水性,通常形成晶体CrCl3·6H2O。直接加热脱水往往得到Cr2O3,有关反应的化学方程式为
(3)实际进行实验时,发现上述装置存在一个缺陷,会导致危险,请简要说明。
Ⅲ.固体X也可用Cr2O3固体。通入NH3时先将氧化物还原为金属单质,然后金属单质与另一产物化合得到CrN,这些过程几乎同时进行。
(4)写出NH3与Cr2O3发生氧化还原反应的化学方程式:
(5)CrN产品中含有Cr2N杂质,可利用如下方法进行纯度测定:取样品14.380g在空气中充分加热至反应完全,剩余固体全为Cr2O3,质量为16.720g。样品中CrN与Cr2N的物质的量之比为
(6)证明样品已反应完全的操作名称是
您最近一年使用:0次
名校
解题方法
2 . 氮循环是自然界中一种重要的物质循环方式:
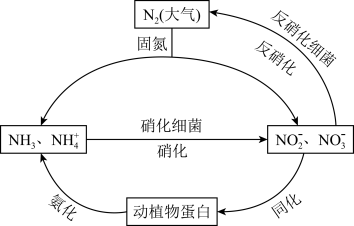
(1)化学与生产、生活和科技都密切相关。下列有关说法不正确的是___________ 。
A.硝化过程无需氧化剂参与
B.含有新冠病毒的飞沫分散在空气中形成的分散系为气溶胶
C.固氮过程中, 只做氧化剂
只做氧化剂
D.“落红不是无情物,化作春泥更护花”蕴含着自然界中的碳、氮循环
E.反硝化过程有助于弥补人工固氮对氮循环造成的影响
F.同化、氨化过程中,实现了氮元素在无机物和有机物之间的转化
(2)写出氮循环中 的电子式
的电子式___________ ,其空间构型是___________ 。写出 的检验方法
的检验方法___________ 。
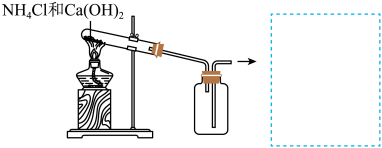
(3)实验室用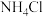 与
与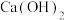 反应来制备
反应来制备 ,原理:
,原理:___________ (化学反应方程式)。在图中补上尾气处理装置(注明所用的化学物质的化学式)。___________
(4)通常我们把大气中游离态的氮转化为氮的化合物的过程称为氮的固定,主要有3种途径。如上① 称为
称为___________ ,②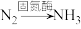 称为生物固氮,还有1种是工业固氮,其反应的化学方程式是
称为生物固氮,还有1种是工业固氮,其反应的化学方程式是___________ 。
(5)反硝化过程中, (C化合价:
(C化合价: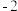 )可作为反应的还原剂。请将该反应的离子方程式补充完整:
)可作为反应的还原剂。请将该反应的离子方程式补充完整:___________ 。
___________ ___________
___________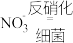 ___________
___________ ___________
___________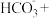 ___________
___________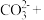 ___________。
___________。

(1)化学与生产、生活和科技都密切相关。下列有关说法不正确的是
A.硝化过程无需氧化剂参与
B.含有新冠病毒的飞沫分散在空气中形成的分散系为气溶胶
C.固氮过程中,
 只做氧化剂
只做氧化剂D.“落红不是无情物,化作春泥更护花”蕴含着自然界中的碳、氮循环
E.反硝化过程有助于弥补人工固氮对氮循环造成的影响
F.同化、氨化过程中,实现了氮元素在无机物和有机物之间的转化
(2)写出氮循环中
 的电子式
的电子式 的检验方法
的检验方法(3)实验室用
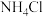 与
与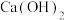 反应来制备
反应来制备 ,原理:
,原理:
(4)通常我们把大气中游离态的氮转化为氮的化合物的过程称为氮的固定,主要有3种途径。如上①
 称为
称为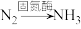 称为生物固氮,还有1种是工业固氮,其反应的化学方程式是
称为生物固氮,还有1种是工业固氮,其反应的化学方程式是(5)反硝化过程中,
 (C化合价:
(C化合价: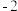 )可作为反应的还原剂。请将该反应的离子方程式补充完整:
)可作为反应的还原剂。请将该反应的离子方程式补充完整:___________
 ___________
___________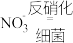 ___________
___________ ___________
___________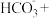 ___________
___________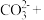 ___________。
___________。
您最近一年使用:0次
名校
解题方法
3 . 氨和硫化氢都是非金属元素的气态氢化物,下列关于两者的实验室制法的说法正确的是
| A.发生装置都可以使用启普发生器 | B.都能用无水氯化钙干燥 |
| C.都能利用复分解反应制取 | D.都能用向下排空气法收集 |
您最近一年使用:0次
4 . 20世纪初,哈伯和博施开发了以 和
和 为原料合成氨工艺,目前该工艺仍在广泛使用。
为原料合成氨工艺,目前该工艺仍在广泛使用。
(1)关于哈伯和博施法工业合成氨的说法正确的是___________。
(2)关于 说法正确的是___________。
说法正确的是___________。
(3)氮的氢化物 与
与 反应
反应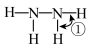

 ,比较键角①
,比较键角①___________ ②(填“>”、“<”或“=”),请说明理由___________ 。
 和
和 为原料合成氨工艺,目前该工艺仍在广泛使用。
为原料合成氨工艺,目前该工艺仍在广泛使用。(1)关于哈伯和博施法工业合成氨的说法正确的是___________。
| A.采用温度为500℃有利于反应正向进行 |
| B.尾气处理利用氨气极易溶于水的性质 |
| C.合成氨工业中利用了热交换器,实现绿色低碳化 |
D.理论上通过该反应 、 、 可以判断该反应常温下不能自发 可以判断该反应常温下不能自发 |
(2)关于
 说法正确的是___________。
说法正确的是___________。A. 遇到HCl产生白雾 遇到HCl产生白雾 | B.利用 受热分解可制得 受热分解可制得 |
C. 可用湿润的红色石蕊试纸检验 可用湿润的红色石蕊试纸检验 | D. 分子间易形成氢键,故 分子间易形成氢键,故 极易溶于水 极易溶于水 |
(3)氮的氢化物
 与
与 反应
反应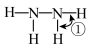

 ,比较键角①
,比较键角①
您最近一年使用:0次
名校
5 . 有关氨气的说法正确的是
| A.氨气可以由所有铵盐受热分解得到 |
| B.氨气通入浓硫酸或浓硝酸中会被氧化 |
| C.氨气与氯气相遇可能冒白烟 |
| D.氨气比PH3易液化是因为N-H键的键能比P-H键能大 |
您最近一年使用:0次
名校
解题方法
6 . 氮是与人类生活密切相关的一种重要元素。请回答下列问题:
(1)N 原子的结构示意图为___________ ;NH3 分子的空间构型是___________ 。
(2)NaNO3 中各元素按照原子半径从大到小排列的顺序是___________ 。
(3)下列氮元素的化合物属于电解质的为_________
(4)用下图装置可以制取氨气并探究其性质,按下列装置进行实验(部分夹持装置已略去)。

①若氨气的发生装置选择 a,则其化学反应方程式为___________ 。
②若氨气的发生装置选择 b,则所用的试剂为___________ 和___________ 。
③B 装置中的干燥剂可选用_________
A. 碱石灰 B.浓硫酸 C.氯化钙固体 D. 氢氧化钠溶液
④实验中观察到 C 中湿润的红色石蕊试纸变蓝色,用方程式说明其原因:___________ 。
⑤当实验进行一段时间后,挤压 D 装置中的胶头滴管,滴入 1~2 滴浓盐酸,可观察到的现象是___________ ,写出相关的化学方程式___________ 。
⑥E 中倒扣漏斗的作用是___________ 。
⑦用 c 装置做氨气喷泉实验时,如果没有胶头滴管,请写出引发喷泉的简单操作是___________ 。
(5)过量的 NH 进入水体可能导致水体富营养化,检测水样中 NH
进入水体可能导致水体富营养化,检测水样中 NH 所需的试剂及主要实验用品,除酒精灯以外,还需要
所需的试剂及主要实验用品,除酒精灯以外,还需要___________ ,反应的离子方程式为___________ 。
(6)氮循环是自然界中一种重要的物质循环方式。

下列说法不正确的是 ______
(1)N 原子的结构示意图为
(2)NaNO3 中各元素按照原子半径从大到小排列的顺序是
(3)下列氮元素的化合物属于电解质的为_________
| A.NH3 | B.NO2 | C.HNO3 | D.NH4Cl |

①若氨气的发生装置选择 a,则其化学反应方程式为
②若氨气的发生装置选择 b,则所用的试剂为
③B 装置中的干燥剂可选用
A. 碱石灰 B.浓硫酸 C.氯化钙固体 D. 氢氧化钠溶液
④实验中观察到 C 中湿润的红色石蕊试纸变蓝色,用方程式说明其原因:
⑤当实验进行一段时间后,挤压 D 装置中的胶头滴管,滴入 1~2 滴浓盐酸,可观察到的现象是
⑥E 中倒扣漏斗的作用是
⑦用 c 装置做氨气喷泉实验时,如果没有胶头滴管,请写出引发喷泉的简单操作是
(5)过量的 NH
 进入水体可能导致水体富营养化,检测水样中 NH
进入水体可能导致水体富营养化,检测水样中 NH 所需的试剂及主要实验用品,除酒精灯以外,还需要
所需的试剂及主要实验用品,除酒精灯以外,还需要(6)氮循环是自然界中一种重要的物质循环方式。

下列说法不正确的是 ______
| A.氮循环过程中氮元素均被氧化 |
| B.含氮无机物和含氮有机物之间可以相互转化 |
| C.NO、NO2等氮氧化合物是光化学烟雾的主要污染物 |
| D.NO2含量的增加会导致温室效应加剧 |
您最近一年使用:0次



