解题方法
1 . N元素的单质及其化合物之间的转化关系如图所示:
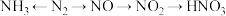
回答下列问题:
(1)N元素在元素周期表中的位置为__________ ,画出N原子结构示意图_________ 。
(2)工业上用氮气和氢气合成氨气,请写出NH3的电子式_____________ 。
(3)实验室可以利用氢氧化钙固体和氯化铵固体制备氨气,请写出该反应的化学方程式___________
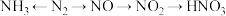
回答下列问题:
(1)N元素在元素周期表中的位置为
(2)工业上用氮气和氢气合成氨气,请写出NH3的电子式
(3)实验室可以利用氢氧化钙固体和氯化铵固体制备氨气,请写出该反应的化学方程式
您最近一年使用:0次
2 . 下图表示由元素周期表中1到20号且不同主族的元素组成的单质及化合物之间的转化关系(产物中的水已略去)。其中A为黄绿色气体单质,D有漂白性;在实验室中常用固体B和固体C加热制取刺激性气味F;F和G的组成元素相同,G与H分子所含电子数相同。

请回答
(1)单质A的组成元素在周期表中的位置是________ ;
(2)B的化学式为________ ,F的电子式为________ ,C中所含化学键类型有_______ ;
(3)写出反应②的化学方程式_____________ ;
(4)反应④中F和气体H在空气中相遇时的实验现象为__________ 写出的F一种具体用途_______________ ;
(5)向具有漂白作用的D溶液中加入H的浓溶液有A生成,其反应的离子方程式为______________ 。
(6)砷元素(As)与上述某元素处于同一主族。砷酸铅可用作杀虫剂。已知:
①在砷酸铅中,砷处于最高价态,铅处于稳定价态。
②砷酸铅是正砷酸对应的盐,1mol正砷酸分子中含有8mol原子.
砷的最高价氧化物的化学式为___________ 砷酸铅的化学式为________

请回答
(1)单质A的组成元素在周期表中的位置是
(2)B的化学式为
(3)写出反应②的化学方程式
(4)反应④中F和气体H在空气中相遇时的实验现象为
(5)向具有漂白作用的D溶液中加入H的浓溶液有A生成,其反应的离子方程式为
(6)砷元素(As)与上述某元素处于同一主族。砷酸铅可用作杀虫剂。已知:
①在砷酸铅中,砷处于最高价态,铅处于稳定价态。
②砷酸铅是正砷酸对应的盐,1mol正砷酸分子中含有8mol原子.
砷的最高价氧化物的化学式为
您最近一年使用:0次
3 . 依据图中氮元素及其化合物的转化关系,回答下列问题:______ 。
(2)回答下列关于 的问题:
的问题:
①利用下列方法制氨气,其中合理的是______ (填字母)。
A.将浓氨水滴入氢氧化钠固体中
B.将氯化铵稀溶液滴入氧化钙固体中
C.将氯化铵固体加热分解
D.加热浓氨水
E.将浓氨水滴入碱石灰固体中
②氨气是重要的化工原料,可以合成多种物质,写出其催化氧化的化学方程式:______ 。
③ 、
、 合成
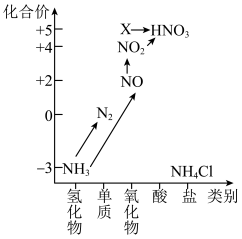
合成 的反应中,当分别用以下各种物质表示反应速率时,则反应速率最快的是
的反应中,当分别用以下各种物质表示反应速率时,则反应速率最快的是______ 。
A. B.
B.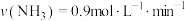
C.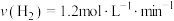 D.
D.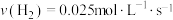
(3)下列关于NO、 的问题:
的问题:
①汽车排气管上装有催化转化器可减少尾气对环境的污染,汽车尾气中的有害气体C0和NO反应可转化为无害气体排放,写出相关反应的化学方程式:______ 。
②NO和 按一定比例混合可以被NaOH溶液完全吸收生成一种正盐,写出相关反应的化学方程式:
按一定比例混合可以被NaOH溶液完全吸收生成一种正盐,写出相关反应的化学方程式:______ 。
(2)回答下列关于
 的问题:
的问题:①利用下列方法制氨气,其中合理的是
A.将浓氨水滴入氢氧化钠固体中
B.将氯化铵稀溶液滴入氧化钙固体中
C.将氯化铵固体加热分解
D.加热浓氨水
E.将浓氨水滴入碱石灰固体中
②氨气是重要的化工原料,可以合成多种物质,写出其催化氧化的化学方程式:
③
 、
、 合成
合成 的反应中,当分别用以下各种物质表示反应速率时,则反应速率最快的是
的反应中,当分别用以下各种物质表示反应速率时,则反应速率最快的是A.
 B.
B.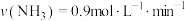
C.
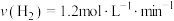 D.
D.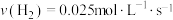
(3)下列关于NO、
 的问题:
的问题:①汽车排气管上装有催化转化器可减少尾气对环境的污染,汽车尾气中的有害气体C0和NO反应可转化为无害气体排放,写出相关反应的化学方程式:
②NO和
 按一定比例混合可以被NaOH溶液完全吸收生成一种正盐,写出相关反应的化学方程式:
按一定比例混合可以被NaOH溶液完全吸收生成一种正盐,写出相关反应的化学方程式:
您最近一年使用:0次
名校
解题方法
4 . 依据图中氮元素及其化合物的转化关系,回答问题:
(1)图1中,X的化学式为________ ,从化合价上看,X具有___________ 性(填“氧化”或“还原”)。
(2)根据图2回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为________ 。
②下列试剂不能用于干燥NH3的是________ (填字母)。
A.浓硫酸 B.碱石灰 C.NaOH固体
③氨气是重要的化工原料,可以合成多种物质,写出氨气催化氧化的化学方程式________ 。
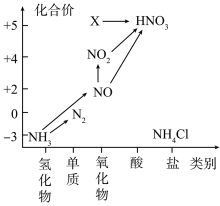
(1)图1中,X的化学式为
(2)根据图2回答下列关于NH3的问题:

①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为
②下列试剂不能用于干燥NH3的是
A.浓硫酸 B.碱石灰 C.NaOH固体
③氨气是重要的化工原料,可以合成多种物质,写出氨气催化氧化的化学方程式
您最近一年使用:0次
名校
解题方法
5 . 依据如图中氮元素及其化合物的转化关系,回答问题:
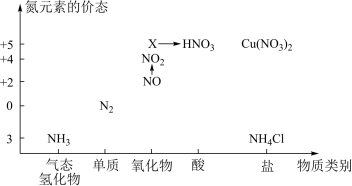
(1)图中,X的化学式为_______ 。
(2)回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为:_______ 。
②下列试剂不能用于干燥NH3的是_______ (填字母)。
A.浓硫酸 B.碱石灰 C.氯化钙固体
③氨气是重要的化工原料,可以合成多种物质,写出催化氧化的化学方程式:_______ 。
(3)回答下列关于NO、NO2的问题:
①汽车排气管上装有催化转化器可减少尾气对环境的污染,发生的反应为:2NO+2CO N2+2CO2该反应中,被氧化的物质是
N2+2CO2该反应中,被氧化的物质是_______ (填化学式),若反应中生成1molN2,则转移电子_______ mol。
②NO→NO2的颜色变化是_______ 。
(4)工业生产中利用氨水吸收SO2和NO2,原理如图所示:
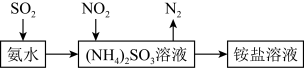
NO2被吸收过程的离子方程式是_______ 。

(1)图中,X的化学式为
(2)回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为:
②下列试剂不能用于干燥NH3的是
A.浓硫酸 B.碱石灰 C.氯化钙固体
③氨气是重要的化工原料,可以合成多种物质,写出催化氧化的化学方程式:
(3)回答下列关于NO、NO2的问题:
①汽车排气管上装有催化转化器可减少尾气对环境的污染,发生的反应为:2NO+2CO
 N2+2CO2该反应中,被氧化的物质是
N2+2CO2该反应中,被氧化的物质是②NO→NO2的颜色变化是
(4)工业生产中利用氨水吸收SO2和NO2,原理如图所示:

NO2被吸收过程的离子方程式是
您最近一年使用:0次
6 . 依据如图氮元素及其化合物的转化关系,回答问题:

(1)图中,氧化物X的化学式为___________ ,从化合价上看,X具有___________ (填“氧化”或“还原”)性。
(2)回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为___________ 。
②下列试剂不能用于干燥NH3的是___________ (填字母)。
A.浓硫酸 B.碱石灰 C.NaOH固体
③若要收集一瓶氨气,请将装置补充完整,在图中虚框内画出连接图___________ 。
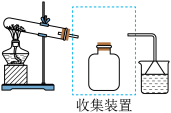
④氨气是重要的化工原料,可以合成多种物质,写出其催化氧化的化学方程式:___________ 。
(3)若要将NH3转变成N2。从氧化还原角度看,下列试剂可行的是:___________

(1)图中,氧化物X的化学式为
(2)回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为
②下列试剂不能用于干燥NH3的是
A.浓硫酸 B.碱石灰 C.NaOH固体
③若要收集一瓶氨气,请将装置补充完整,在图中虚框内画出连接图

④氨气是重要的化工原料,可以合成多种物质,写出其催化氧化的化学方程式:
(3)若要将NH3转变成N2。从氧化还原角度看,下列试剂可行的是:___________
| A.O2 | B.Na | C.NH4Cl | D.NO2 |
您最近一年使用:0次
名校
解题方法
7 . 氮是植物体内蛋白质、叶绿素的重要组成元素,氮肥能促进农作物的生长。氨是生产氮肥的原料。氮及其部分化合物的转化关系如图所示,回答下列问题:
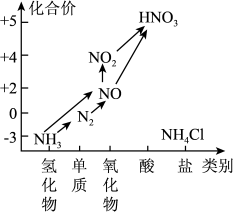
(1)下列反应中,不属于氮的固定的是_______
(2)氨的电子式是_______ 。
(3)在物质转化图中的各气体,可用排水法收集的气体是_______ (填化学式,下同),既可以用浓硫酸干燥,又可以用碱石灰干燥的是气体是_______ 。
(4)实验室常用NH4Cl与Ca(OH)2制取氨气,请写出该反应的化学方程式_______ 。而工业上则由氮气和氢气直接合成氨,该反应的化学方程式为_______ 。
(5)NO、CO都是汽车尾气的主要成分,直接排放会污染空气,人们研究出一种催化剂,可将两种气体通过,反应转化为无污染的空气成分,则反应的化学方程式是_______ 。
(6)氮的一种化合物肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如图所示,已知断裂1mol化学键所需的能量(kJ):N≡N为942、O=O为500、N-N为154,则断裂1molN-H所需的能量是_______ kJ。


(1)下列反应中,不属于氮的固定的是_______
| A.N2和H2在一定条件下合成NH3 |
| B.豆科植物把空气中的氮气转化为化合态的氮 |
| C.雷电时,空气中的N2与O2反应生成NO |
| D.由NH3制碳酸氢铵 |
(3)在物质转化图中的各气体,可用排水法收集的气体是
(4)实验室常用NH4Cl与Ca(OH)2制取氨气,请写出该反应的化学方程式
(5)NO、CO都是汽车尾气的主要成分,直接排放会污染空气,人们研究出一种催化剂,可将两种气体通过,反应转化为无污染的空气成分,则反应的化学方程式是
(6)氮的一种化合物肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如图所示,已知断裂1mol化学键所需的能量(kJ):N≡N为942、O=O为500、N-N为154,则断裂1molN-H所需的能量是

您最近一年使用:0次
解题方法
8 . 依据图中氮元素及其化合物的转化关系,回答问题:
(1)图1中,X的化学式为___ ,从化合价上看,X具有___ 性(“氧化”、“还原”)。
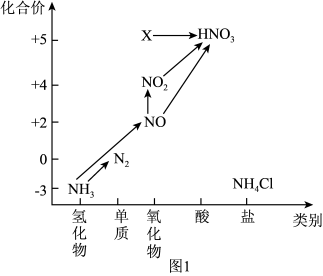
(2)回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为_________ 。
②下列试剂不能用于干燥NH3的是_________ (填字母)。
A.浓硫酸 B.碱石灰 C.NaOH固体
③若要收集一瓶氨气,请将上述装置补充完整,在图2虚框内画出连接图___ 。
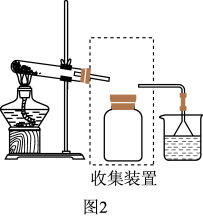
④氨气是重要的化工原料,可以合成多种物质,写出其催化氧化的化学方程式____ 。
(3)回答下列关于NO、NO2的问题:
①汽车排气管上装有催化转化器可减少尾气对环境的污染,汽车尾气中的有害气体CO和NO反应可转化为无害气体排放,写出相关反应的化学方程式:____ 。
②NO和O2按一定比例混合可以被水完全吸收,写出相关化学方程式____ 。工业生产中利用氨水吸收SO2和NO2,原理如图3所示:
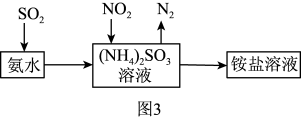
NO2被吸收过程的离子方程式是____ 。
(1)图1中,X的化学式为

(2)回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为
②下列试剂不能用于干燥NH3的是
A.浓硫酸 B.碱石灰 C.NaOH固体
③若要收集一瓶氨气,请将上述装置补充完整,在图2虚框内画出连接图

④氨气是重要的化工原料,可以合成多种物质,写出其催化氧化的化学方程式
(3)回答下列关于NO、NO2的问题:
①汽车排气管上装有催化转化器可减少尾气对环境的污染,汽车尾气中的有害气体CO和NO反应可转化为无害气体排放,写出相关反应的化学方程式:
②NO和O2按一定比例混合可以被水完全吸收,写出相关化学方程式

NO2被吸收过程的离子方程式是
您最近一年使用:0次
2010·宁夏银川·三模
9 . 如图表示由元素周期表中1~20号且不同主族元素组成的单质及化合物之间转化关系(产物中的水已略去)。其中A为单质;在实验室中,常用固体B和固体C加热制取气体F;F与G的组成元素相同,G与I分子所含电子数相同。请回答:

(1)写出B、G的化学式B________ 、G________ 。
(2)写出C的电子式________ ;反应④的实验现象为_________ ;
(3)向具有漂白作用的D溶液加入I的稀溶液,写出反应的离子方程式:________ ;
(4)向D的溶液加入I的浓溶液有A生成,其反应的离子方程式为:_________ 。
(5)写出反应③的化学方程式__________ 。

(1)写出B、G的化学式B
(2)写出C的电子式
(3)向具有漂白作用的D溶液加入I的稀溶液,写出反应的离子方程式:
(4)向D的溶液加入I的浓溶液有A生成,其反应的离子方程式为:
(5)写出反应③的化学方程式
您最近一年使用:0次
解题方法
10 . A、B、C、D、E、X均为中学化学常见物质,相互转化关系如图所示(部分物质略去)。

I.若A为气体单质,气体B能使湿润红色石蕊试纸变蓝,E为红棕色气体。
(1)A中所含元素在周期表中的位置是__________________
(2)实验室制取B的化学方程式为__________________________
(3)D和CO均是汽车尾气的主要成分,通过汽车尾气催化转化装置生成无污染气体,降低污染物排放,写出该反应的化学方程式:_____________________
II.若A是淡黄色固体,B中阴、阳离子均为10电子粒子,常温下X是无色气体。
(4)A与X反应的化学方程式:____________________________
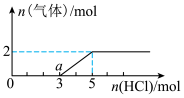
(5)将一定量的气体X通入B的溶液中,在所得溶液中逐滴加入稀盐酸至过量,产生的气体与HCl物质的量的关系如图所示(忽略气体的溶解和HCl的挥发)。a点溶液中所含溶质的化学式为_________________

I.若A为气体单质,气体B能使湿润红色石蕊试纸变蓝,E为红棕色气体。
(1)A中所含元素在周期表中的位置是
(2)实验室制取B的化学方程式为
(3)D和CO均是汽车尾气的主要成分,通过汽车尾气催化转化装置生成无污染气体,降低污染物排放,写出该反应的化学方程式:
II.若A是淡黄色固体,B中阴、阳离子均为10电子粒子,常温下X是无色气体。
(4)A与X反应的化学方程式:
(5)将一定量的气体X通入B的溶液中,在所得溶液中逐滴加入稀盐酸至过量,产生的气体与HCl物质的量的关系如图所示(忽略气体的溶解和HCl的挥发)。a点溶液中所含溶质的化学式为

您最近一年使用:0次
2016-12-09更新
|
345次组卷
|
2卷引用:2016届北京市大兴区高三上学期期末检测化学试卷



