名校
解题方法
1 . 下列有关物质的性质与用途具有对应关系的是
A. 显红棕色,可用于火箭燃料中的氧化剂 显红棕色,可用于火箭燃料中的氧化剂 |
B.氨水具有碱性,可用于去除烟气中的 |
C. 具有强酸性,可用于实验室制取氢气 具有强酸性,可用于实验室制取氢气 |
D. 受热易分解,可用作铵态氮肥 受热易分解,可用作铵态氮肥 |
您最近一年使用:0次
名校
2 . 下列有关物质的性质与用途具有对应关系的是
| A.Zn具有还原性和导电性,可用作锌锰干电池的负极材料 |
| B.Al2O3具有两性,可用于电解冶炼铝 |
| C.NH4Cl受热易分解,可用于实验室制NH3 |
| D.NH3具有还原性,可用作工业制冷剂 |
您最近一年使用:0次
3 . 下列有关物质的性质与用途具有对应关系的是
| A.NH3具有还原性,可用作工业制冷剂 |
| B.Al2O3具有两性,可用于电解冶炼铝 |
| C.NH4Cl受热易分解,可用于实验室制NH3 |
| D.Zn具有还原性和导电性,可用作锌锰干电池的负极材料 |
您最近一年使用:0次
4 . 化学与生产、生活关系密切。下列物质的性质和用途都正确且有对应关系的是
| 选项 | 物质性质 | 用途 |
| A | KMnO4溶液可氧化水果释放的CH2=CH2 | 浸泡过KMnO4溶液的硅藻土可用于水果保鲜 |
| B | 氢氟酸有酸性 | 刻蚀玻璃 |
| C | 氯化钙有较强的吸水性 | 干燥氨气 |
| D | 纤维素能水解 | 制备硝酸纤维和醋酸纤维 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . I.元素的“价—类”二维图体现了化学变化之美。部分含硫、氮物质的类别与硫元素和氮元素化合价的对应关系如下图所示。回答下列问题:

(1)实验室用两种固体制备R的化学方程式________ 。
(2)下列有关图中所示含N、S物质的叙述,正确的是________ (填标号)。
a.在催化剂的作用下,R可将Y、Z还原为X
b.图中所示的物质中,只有W、D、E属于电解质
c.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生
d.Z、C、F均能与NaOH溶液反应,都是酸性氧化物
e.制备焦亚硫酸钠(Na2S2O5),从氧化还原反应的角度分析,可选择B和D反应
II.已知:①联氨(N2H4)性质与NH3相似,溶于水可生成一种二元弱碱。
②N2H4以还原性为主,氧化产物一般是N2,通常总是把联氨用作强还原剂。
(3)用次氯酸钠和氨气常温制备联氨,化学方程式为:________ 。
(4)根据以上信息,推断下列关于N2H4的说法不正确的是______。
(5)在标准状况下将1.92g铜粉投入一定量浓HNO3中,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后共收集到只由NO2和NO组成的混合气体1.12L,则混合气体中NO的体积为_____。

(1)实验室用两种固体制备R的化学方程式
(2)下列有关图中所示含N、S物质的叙述,正确的是
a.在催化剂的作用下,R可将Y、Z还原为X
b.图中所示的物质中,只有W、D、E属于电解质
c.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生
d.Z、C、F均能与NaOH溶液反应,都是酸性氧化物
e.制备焦亚硫酸钠(Na2S2O5),从氧化还原反应的角度分析,可选择B和D反应
II.已知:①联氨(N2H4)性质与NH3相似,溶于水可生成一种二元弱碱。
②N2H4以还原性为主,氧化产物一般是N2,通常总是把联氨用作强还原剂。
(3)用次氯酸钠和氨气常温制备联氨,化学方程式为:
(4)根据以上信息,推断下列关于N2H4的说法不正确的是______。
| A.它与E形成的酸式盐可以表示为N2H5HSO5 |
| B.它溶于水所得的溶液中共有4种离子 |
C.它溶于水发生电离的第一步可表示为: |
| D.若已知联氨和四氧化二氮可以做火箭推进剂,两者反应产物可以是氮气和水 |
(5)在标准状况下将1.92g铜粉投入一定量浓HNO3中,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后共收集到只由NO2和NO组成的混合气体1.12L,则混合气体中NO的体积为_____。
| A.56mL | B.112mL | C.224mL | D.448mL |
您最近一年使用:0次
名校
解题方法
6 . 元素的“价—类”二维图体现了化学变化之美。部分含硫、氮物质的类别与硫元素和氮元素化合价的对应关系如图所示。
(1)写出实验室制备物质R的化学方程式__________________ 。
(2)Z与Y是硝酸厂尾气的主要成分,为保证其充分被吸收往往先鼓入过量的________ ,再将混合气体通入氢氧化钠溶液中,写出用氢氧化钠溶液吸收时的化学方程式:____________ 。
(3)下列有关图中所示含N、S物质的叙述,正确的是______(填标号)。
(4)Na2S2O3是重要的化工原料。从“价一类”角度分析,下列制备Na2S2O3的方案理论上可行的是_________ (填字母)。
a.Na2S+S b. Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
(5)已知中学常见化合物Q是由C与足量氢氧化钠溶液反应所得,能被KMnO4氧化为Na2SO4,则24mL0.05mol/L的Q溶液与20mL0.04mol/L的KMnO4溶液恰好反应时,Mn元素在还原产物中的化合价为_______ ;中学实验室某无色盐溶液可能混入了Q和Na2SO4中的一种或二种,判断是否混入杂质的最合理的可靠的实验操作:取试样于试管中,依次加入下列试剂_________ (填试剂序号)即可确认。
①Ba(NO3)2溶液 ②BaCl2溶液 ③稀盐酸 ④稀硝酸 ⑤品红溶液 ⑥酸性KMnO4溶液

(1)写出实验室制备物质R的化学方程式
(2)Z与Y是硝酸厂尾气的主要成分,为保证其充分被吸收往往先鼓入过量的
(3)下列有关图中所示含N、S物质的叙述,正确的是______(填标号)。
| A.在催化剂的作用下,R可将Y、Z还原为X |
| B.0.4mol/LW与0.2mol/LE的混合溶液100mL最多能溶解铜0.96g |
| C.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生 |
| D.Z、C、F均能与NaOH溶液反应,都是酸性氧化物 |
a.Na2S+S b. Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
(5)已知中学常见化合物Q是由C与足量氢氧化钠溶液反应所得,能被KMnO4氧化为Na2SO4,则24mL0.05mol/L的Q溶液与20mL0.04mol/L的KMnO4溶液恰好反应时,Mn元素在还原产物中的化合价为
①Ba(NO3)2溶液 ②BaCl2溶液 ③稀盐酸 ④稀硝酸 ⑤品红溶液 ⑥酸性KMnO4溶液
您最近一年使用:0次
解题方法
7 . 化学在生产、生活中有着广泛的应用。下列对应关系不正确的是
| 选项 | 化学性质 | 实际应用 |
| A | 乙烯能与 溶液反应 溶液反应 | 用浸泡过 溶液的硅土保存水果 溶液的硅土保存水果 |
| B | HF能与 反应 反应 | 氢氟酸在玻璃器皿上刻蚀标记 |
| C | 铁常温下遇浓硫酸发生钝化 | 用铁桶装浓硫酸 |
| D | 铵盐受热易发生分解反应 | 实验室中利用 分解反应制备氨 分解反应制备氨 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 氨元素是动植物生长不可缺少的元素,图1是自然界中氨元素的循环示意图,图2是氨元素的常见化合价与部分物质类别的对应关系。回答下列问题:
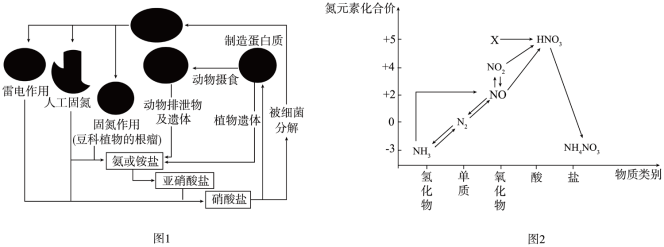
(1)图1中属于固氮过程的是_______ (写两种即可)。
(2) 可以将
可以将 还原为Fe,自身被氧化为
还原为Fe,自身被氧化为 。某学习小组欲制备氨气以还原氧化铁。
。某学习小组欲制备氨气以还原氧化铁。
①下列各装置中常用于实验室制备氨气的是_______ (填字母),利用该装置制备氨气的化学方程式为_______ 。
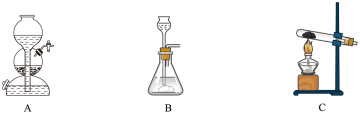
② 还原
还原 并检验有水生成的实验装置如图所示:
并检验有水生成的实验装置如图所示:
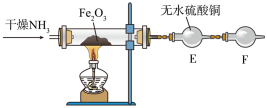
写出氨气与氧化铁反应的化学方程式:_______ 。干燥管F中装有无水氯化钙,其作用是_______ 。
(3)图2中物质X的化学式是_______ ,其与水反应生成 。某硝酸和硫酸的混合溶液200mL,其中硫酸的浓度为
。某硝酸和硫酸的混合溶液200mL,其中硫酸的浓度为 ,硝酸的浓度为
,硝酸的浓度为 ,现向其中加入9.6g铜粉,充分反应生成气体的化学式为
,现向其中加入9.6g铜粉,充分反应生成气体的化学式为_______ (假设只生成一种气体),最多可收集到标准状况下的该气体的体积为_______ L。

(1)图1中属于固氮过程的是
(2)
 可以将
可以将 还原为Fe,自身被氧化为
还原为Fe,自身被氧化为 。某学习小组欲制备氨气以还原氧化铁。
。某学习小组欲制备氨气以还原氧化铁。①下列各装置中常用于实验室制备氨气的是

②
 还原
还原 并检验有水生成的实验装置如图所示:
并检验有水生成的实验装置如图所示:
写出氨气与氧化铁反应的化学方程式:
(3)图2中物质X的化学式是
 。某硝酸和硫酸的混合溶液200mL,其中硫酸的浓度为
。某硝酸和硫酸的混合溶液200mL,其中硫酸的浓度为 ,硝酸的浓度为
,硝酸的浓度为 ,现向其中加入9.6g铜粉,充分反应生成气体的化学式为
,现向其中加入9.6g铜粉,充分反应生成气体的化学式为
您最近一年使用:0次
9 . 硫元素和氨元素在化学实验、化工生产中扮演着重要角色。
I.图1是自然界中硫元素的存在示意图,图2是硫元素的常见化合价与部分物质类别的对应关系。请回答下列问题:
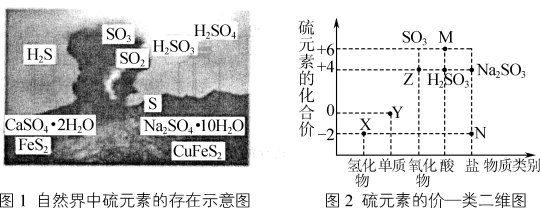
(1)图2中N所对应图1中物质的化学式为_______ ,Y与金属铜反应所得产物的化学式为_______ 。X与Z反应中氧化剂与还原剂的物质的量之比为_______ 。
(2)碳和M的浓溶液反应生成Z的化学方程式为_______ 。
(3)从分类角度分析判断,下列物质不属于酸性氧化物的是_______。
II.氮及其化合物在很多方面有广泛应用。
(4)实验室常用 与
与 制取氨气。证明氨气已集满的操作和现象是
制取氨气。证明氨气已集满的操作和现象是_______ 。
(5)含氮废水会加速藻类和其他浮游生物的大量繁殖,使水质恶化。利用微生物对含氮废水进行处理的流程如下:
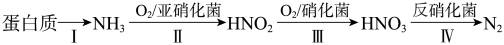
请回答:
①根据下图判断,使用亚硝化菌的最佳条件为_______ 。
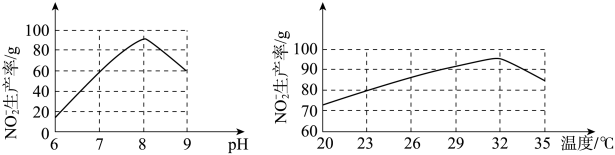
②利用微生物处理含氮废水的优点为_______ 。(答出2点即可)。
(6)汽车排气管上装有催化转化器可减少尾气对环境的污染,汽车尾气中的有害气体CO和NO反应可转化为无害气体排放,写出相关反应的化学方程式_______ 。
I.图1是自然界中硫元素的存在示意图,图2是硫元素的常见化合价与部分物质类别的对应关系。请回答下列问题:

(1)图2中N所对应图1中物质的化学式为
(2)碳和M的浓溶液反应生成Z的化学方程式为
(3)从分类角度分析判断,下列物质不属于酸性氧化物的是_______。
A. | B. | C. | D. |
II.氮及其化合物在很多方面有广泛应用。
(4)实验室常用
 与
与 制取氨气。证明氨气已集满的操作和现象是
制取氨气。证明氨气已集满的操作和现象是(5)含氮废水会加速藻类和其他浮游生物的大量繁殖,使水质恶化。利用微生物对含氮废水进行处理的流程如下:
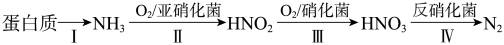
请回答:
①根据下图判断,使用亚硝化菌的最佳条件为

②利用微生物处理含氮废水的优点为
(6)汽车排气管上装有催化转化器可减少尾气对环境的污染,汽车尾气中的有害气体CO和NO反应可转化为无害气体排放,写出相关反应的化学方程式
您最近一年使用:0次
名校
10 . 回答下列问题
(1) 具有广泛的用途,实验室常用下图所示装置制取并收集
具有广泛的用途,实验室常用下图所示装置制取并收集 。
。 和
和 制取
制取 的化学方程式为
的化学方程式为__________ 。
②干燥 应选用的干燥剂是
应选用的干燥剂是__________ 。
③图1中方框内收集 的装置可选用图2中的
的装置可选用图2中的__________ (填序号)。
④尾气处理装置中使用倒置漏斗的作用是__________ 。
⑤将蘸有浓盐酸的棉球放在玻璃片上,再将集满 的集气瓶扣住棉球,可观察到的现象是
的集气瓶扣住棉球,可观察到的现象是__________ 。
(2) 可以转化为其他含氮物质,下图为
可以转化为其他含氮物质,下图为 转化为
转化为 的流程。
的流程。

①工业上 合成氨的化学方程式为
合成氨的化学方程式为__________ 。
②写出 与
与 反应转化为NO的化学方程式
反应转化为NO的化学方程式__________ 。
③ 转化为
转化为 的整个过程中,为提高氮原子的利用率,可采取的措施是
的整个过程中,为提高氮原子的利用率,可采取的措施是__________ 。
(3)某同学用研究浓硫酸和木炭的反应并对其产物进行检验。
①该反应的化学方程式为__________ 。
②设计实验检验该反应气体产物中的各成分,可选用的试剂有:
a.澄清石灰水 b.高锰酸钾酸性溶液 c.无水硫酸铜
将上述试剂按照正确使用顺序排列为______ (填序号);证明产生 的实验现象是:
的实验现象是:__________ 。
(4)某同学用研究 与
与 的水溶液反应并对其产物进行检验。
的水溶液反应并对其产物进行检验。
①用 固体和70%的硫酸溶液反应制备
固体和70%的硫酸溶液反应制备 ,反应的化学方程式是
,反应的化学方程式是__________ 。
②将 通入
通入 的水溶液中,取适量反应后的溶液于试管中,向其中滴加少量X溶液,有白色沉淀生成,得出结论:
的水溶液中,取适量反应后的溶液于试管中,向其中滴加少量X溶液,有白色沉淀生成,得出结论: 可以与
可以与 的水溶液反应。X溶液是
的水溶液反应。X溶液是__________ (填字母)。
a. 溶液 b.
溶液 b. 溶液 c.
溶液 c. 溶液 d.品红溶液
溶液 d.品红溶液
③ 与
与 同时通入水中反应的化学方程式是
同时通入水中反应的化学方程式是__________ 。
(1)
 具有广泛的用途,实验室常用下图所示装置制取并收集
具有广泛的用途,实验室常用下图所示装置制取并收集 。
。
 和
和 制取
制取 的化学方程式为
的化学方程式为②干燥
 应选用的干燥剂是
应选用的干燥剂是③图1中方框内收集
 的装置可选用图2中的
的装置可选用图2中的④尾气处理装置中使用倒置漏斗的作用是
⑤将蘸有浓盐酸的棉球放在玻璃片上,再将集满
 的集气瓶扣住棉球,可观察到的现象是
的集气瓶扣住棉球,可观察到的现象是(2)
 可以转化为其他含氮物质,下图为
可以转化为其他含氮物质,下图为 转化为
转化为 的流程。
的流程。
①工业上
 合成氨的化学方程式为
合成氨的化学方程式为②写出
 与
与 反应转化为NO的化学方程式
反应转化为NO的化学方程式③
 转化为
转化为 的整个过程中,为提高氮原子的利用率,可采取的措施是
的整个过程中,为提高氮原子的利用率,可采取的措施是(3)某同学用研究浓硫酸和木炭的反应并对其产物进行检验。
①该反应的化学方程式为
②设计实验检验该反应气体产物中的各成分,可选用的试剂有:
a.澄清石灰水 b.高锰酸钾酸性溶液 c.无水硫酸铜
将上述试剂按照正确使用顺序排列为
 的实验现象是:
的实验现象是:(4)某同学用研究
 与
与 的水溶液反应并对其产物进行检验。
的水溶液反应并对其产物进行检验。①用
 固体和70%的硫酸溶液反应制备
固体和70%的硫酸溶液反应制备 ,反应的化学方程式是
,反应的化学方程式是②将
 通入
通入 的水溶液中,取适量反应后的溶液于试管中,向其中滴加少量X溶液,有白色沉淀生成,得出结论:
的水溶液中,取适量反应后的溶液于试管中,向其中滴加少量X溶液,有白色沉淀生成,得出结论: 可以与
可以与 的水溶液反应。X溶液是
的水溶液反应。X溶液是a.
 溶液 b.
溶液 b. 溶液 c.
溶液 c. 溶液 d.品红溶液
溶液 d.品红溶液③
 与
与 同时通入水中反应的化学方程式是
同时通入水中反应的化学方程式是
您最近一年使用:0次



