河南省安阳市2021-2022学年高一下学期大联考阶段性测试(五)化学试题
河南
高一
阶段练习
2022-07-03
182次
整体难度:
适中
考查范围:
化学反应原理、常见无机物及其应用、认识化学科学、有机化学基础、化学与STSE、物质结构与性质、化学实验基础
河南省安阳市2021-2022学年高一下学期大联考阶段性测试(五)化学试题
河南
高一
阶段练习
2022-07-03
182次
整体难度:
适中
考查范围:
化学反应原理、常见无机物及其应用、认识化学科学、有机化学基础、化学与STSE、物质结构与性质、化学实验基础
一、单选题 添加题型下试题
单选题
|
适中(0.65)
名校
1. 2022年2月北京冬奥会尽显化学科技,科技助力体现环保理念。下列说法正确的是
| A.火炬“飞扬”外壳由有机高分子材料碳纤维制成 |
| B.火炬“飞扬”采用氢能为燃料,体现“绿色低碳”的发展理念 |
| C.奥运场馆采用硫化镉发电玻璃,实现了电能向化学能的转化 |
| D.奥运“战袍”利用微信小程序调控石墨烯片加热保暖,石墨烯属于烯烃 |
【知识点】 原电池原理理解解读 原电池原理的综合应用解读
您最近一年使用:0次
2022-06-17更新
|
107次组卷
|
2卷引用:河南省安阳市2021-2022学年高一下学期大联考阶段性测试(五)化学试题
单选题
|
适中(0.65)
2. 下列有关 、
、 ,和
,和 的说法正确的是
的说法正确的是
 、
、 ,和
,和 的说法正确的是
的说法正确的是| A.三者都是酸性氧化物 |
| B.三者都能与水反应生成对应的酸 |
| C.三者的熔沸点均较低 |
D.向 溶液中通入足量 溶液中通入足量 ,出现乳白色浑浊, ,出现乳白色浑浊, 体现酸性和氧化性 体现酸性和氧化性 |
您最近一年使用:0次
单选题
|
较易(0.85)
3. 2022年4月16日神舟十三号载人飞船返回着陆,三位宇航员生活用水主要是利用水的循环。科学家研制出利用太阳能产生激光分解水: 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是A.该反应消耗2mol 时,生成16g 时,生成16g |
| B.该反应是放热反应,将太阳能转化为化学能和热能 |
| C.该反应过程中断裂O-H键要吸收能量,形成H-H键要释放能量 |
| D.需要加热才能发生的反应都是吸热反应 |
【知识点】 氧化还原反应有关计算 化学反应中能量变化的原因 能量的相互转化
您最近一年使用:0次
4. 下列物质用途与原理分析均正确的是
| 选项 | 物质用途 | 原理分析 |
| A | 以石油为原料制备聚乙烯、聚丙烯塑料 | 该过程中只涉及蒸馏与分馏、加聚反应 |
| B | 以海水为原料分别提取NaCl,Mg、 | 都只发生氧化还原反应 |
| C | 以 、CO、CH3OH为原料直接合成有机玻璃的单体: 、CO、CH3OH为原料直接合成有机玻璃的单体: | 该工艺是理想的绿色化学工艺 |
| D | 补血制剂(含 )与维生素C配合使用,可提高药物的使用效率 )与维生素C配合使用,可提高药物的使用效率 | 维生素C具有较强的氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
5. 常温下,将6mol 和8mol
和8mol 充入体积为2L的恒容密闭容器中发生反应:
充入体积为2L的恒容密闭容器中发生反应: ,
, 的物质的量与时间的关系如图所示。下列有关叙述正确的是
的物质的量与时间的关系如图所示。下列有关叙述正确的是
 和8mol
和8mol 充入体积为2L的恒容密闭容器中发生反应:
充入体积为2L的恒容密闭容器中发生反应: ,
, 的物质的量与时间的关系如图所示。下列有关叙述正确的是
的物质的量与时间的关系如图所示。下列有关叙述正确的是
A.1~3min内, 的平均反应速率为 的平均反应速率为 |
B.8~10min内, 的物质的量不变,反应已停止 的物质的量不变,反应已停止 |
C.0~8min内,生成 的质量为64g 的质量为64g |
D.c点时反应达到平衡状态,此时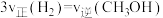 |
【知识点】 化学反应速率计算解读 化学平衡图像分析 化学平衡状态的判断方法解读
您最近一年使用:0次
2022-06-17更新
|
93次组卷
|
2卷引用:河南省安阳市2021-2022学年高一下学期大联考阶段性测试(五)化学试题
单选题
|
较易(0.85)
6. 山梨酸是一种国际公认的安全防腐剂,安全性很高,广泛用于食品、化妆品、农产品等行业。下列有关说法错误的是
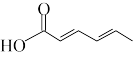

A.山梨酸的分子式为 | B.山梨酸可使溴的四氯化碳溶液褪色 |
| C.山梨酸可与氢氧化钠发生反应 | D.1mol山梨酸可与3mol 发生加成反应 发生加成反应 |
您最近一年使用:0次
2022-06-17更新
|
66次组卷
|
3卷引用:河南省安阳市2021-2022学年高一下学期大联考阶段性测试(五)化学试题
7. 下列关于甲烷和乙烯的叙述错误的是
| A.甲烷分子为正四面体结构,乙烯分子为平面结构 |
| B.甲烷与氯气在光照条件下发生取代反应 |
| C.乙烯与溴的四氯化碳溶液可发生加成反应 |
| D.甲烷中混有的乙烯可通过酸性高锰酸钾溶液除去 |
您最近一年使用:0次
单选题
|
适中(0.65)
8. 目前汽车最常用的启动电源为铅蓄电池,其结构如图所示。铅蓄电池放电时的电池总反应为 。下列叙述错误的是
。下列叙述错误的是
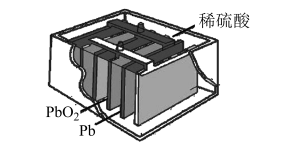
 。下列叙述错误的是
。下列叙述错误的是
A. 是金属氧化物,固态 是金属氧化物,固态 不能导电, 不能导电,  不能作电极 不能作电极 |
B.放电时, 得到电子,被还原生成 得到电子,被还原生成 |
| C.放电时,Pb作负极,失去电子,发生氧化反应 |
D.放电时, 移向正极,溶液的酸性减弱 移向正极,溶液的酸性减弱 |
您最近一年使用:0次
单选题
|
适中(0.65)
9. 下列实验装置不能达到相应实验目的的是
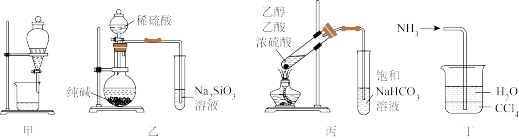

A.装置甲利用 提取碘水中的 提取碘水中的 |
| B.装置乙验证非金属性:S>C>Si |
| C.装置丙利用乙醇和乙酸制备并收集乙酸乙酯 |
| D.装置丁对氨气进行吸收处理 |
您最近一年使用:0次
2022-06-17更新
|
176次组卷
|
2卷引用:河南省安阳市2021-2022学年高一下学期大联考阶段性测试(五)化学试题
10. 铼(Re)具有较高的熔点和沸点,可用于制造火箭引擎等。以过铼酸为原料制备金属铼的流程如下:
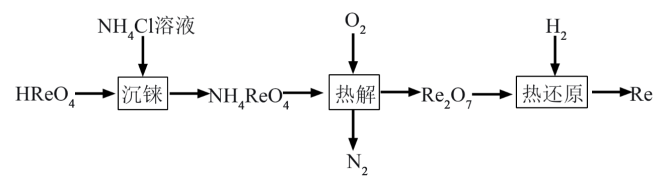
已知:①过铼酸(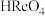 )是易溶于水的一元强酸,但不具有强氧化性。②过铼酸铵(
)是易溶于水的一元强酸,但不具有强氧化性。②过铼酸铵(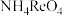 )是白色片状晶体,微溶于冷水,溶于热水。
)是白色片状晶体,微溶于冷水,溶于热水。
下列说法错误的是

已知:①过铼酸(
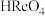 )是易溶于水的一元强酸,但不具有强氧化性。②过铼酸铵(
)是易溶于水的一元强酸,但不具有强氧化性。②过铼酸铵(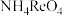 )是白色片状晶体,微溶于冷水,溶于热水。
)是白色片状晶体,微溶于冷水,溶于热水。下列说法错误的是
| A.“沉铼”时适当搅拌能加快反应速率 |
| B.分离过铼酸铵采用过滤、热水洗涤等操作 |
C.“热还原”中可以用CO、Al等还原剂替代 |
D.“热解”反应的化学方程式为 |
您最近一年使用:0次
单选题
|
容易(0.94)
11. 下列各组反应(表中物质均为反应物)刚开始时,放出 速率最快的是
速率最快的是
 速率最快的是
速率最快的是| 选项 | 金属(粉末状) | 酸的浓度及体积 | 反应温度 |
| A | Mg,2.4g | 3.0 硫酸100mL 硫酸100mL | 25℃ |
| B | Zn,6.5g | 6.0 硝酸100mL 硝酸100mL | 30℃ |
| C | Fe,5.6g | 18.4 硫酸100mL 硫酸100mL | 25℃ |
| D | Zn,6.5g | 6.0 盐酸100mL 盐酸100mL | 25℃ |
| A.A | B.B | C.C | D.D |
【知识点】 浓度对化学反应速率的影响解读 温度对化学反应速率的影响解读
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
12. 下列说法正确的是
| A.氮氧化物均为大气污染物,在大气中均可稳定存在 |
B.能使品红溶液褪色的物质一定是 |
C.可用浓盐酸检测输送 的管道是否发生泄漏 的管道是否发生泄漏 |
D. 既能和碱反应,又能和氢氟酸反应,所以是两性氧化物 既能和碱反应,又能和氢氟酸反应,所以是两性氧化物 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
13. 我国科学家首次在实验室实现从 到淀粉的全合成,其合成路线如下:
到淀粉的全合成,其合成路线如下:
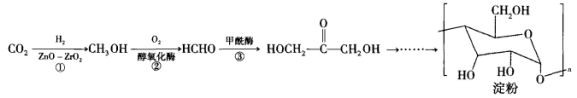
下列说法正确的是
 到淀粉的全合成,其合成路线如下:
到淀粉的全合成,其合成路线如下:
下列说法正确的是
| A.温度越高,反应②③的速率一定越快 |
| B.反应②属于氧化反应 |
C.3.2g 可与金属Na反应生成标准状况下的11.2L 可与金属Na反应生成标准状况下的11.2L |
| D.淀粉属于有机高分子化合物,与纤维素互为同分异构体 |
您最近一年使用:0次
单选题
|
较易(0.85)
14. 科学家首次用X射线激光技术观察到CO与活性O在催化剂表面反应的过程如图所示。下列说法错误的是


| A.状态I→状态II为吸热过程 |
| B.状态I、II、III中最稳定的是状态II |
| C.状态I→状态III过程中有极性共价键形成 |
| D.状态I→状态II表示反应在催化剂表面进行,催化剂能加快反应速率 |
【知识点】 能量的相互转化 影响化学反应速率的因素
您最近一年使用:0次
单选题
|
较易(0.85)
解题方法
15. 甲醇( )又称“木醇”,是基础的有机化工原料和优质燃料,在以KOH溶液为电解质溶液的条件下,与氧气构成清洁燃料电池。下列说法错误的是
)又称“木醇”,是基础的有机化工原料和优质燃料,在以KOH溶液为电解质溶液的条件下,与氧气构成清洁燃料电池。下列说法错误的是
 )又称“木醇”,是基础的有机化工原料和优质燃料,在以KOH溶液为电解质溶液的条件下,与氧气构成清洁燃料电池。下列说法错误的是
)又称“木醇”,是基础的有机化工原料和优质燃料,在以KOH溶液为电解质溶液的条件下,与氧气构成清洁燃料电池。下列说法错误的是A.通入 的电极为燃料电池的负极 的电极为燃料电池的负极 |
| B.该电池的两极均可为石墨电极 |
| C.放电过程中,电子在KOH溶液中由正极向负极移动 |
D.电池总反应式为 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
16. A、X、Y、Z是中学化学常见物质,它们之间在一定条件下可以发生如图所示的转化关系(部分反应中的 没有标注),其中A、X、Y、Z均含有同一种元素。
没有标注),其中A、X、Y、Z均含有同一种元素。
 没有标注),其中A、X、Y、Z均含有同一种元素。
没有标注),其中A、X、Y、Z均含有同一种元素。
| A.若A为碳单质,则Z为碳酸 |
B.若A为 ,Z为硫酸,则X可与A反应生成单质S ,Z为硫酸,则X可与A反应生成单质S |
| C.若A为非金属单质或非金属氢化物,则Z不一定能与金属铜反应生成Y |
| D.若反应①②③都是氧化还原反应,则A、X、Y、Z中含有的同一种元素一定呈现四种化合价 |
您最近一年使用:0次
2022-06-17更新
|
619次组卷
|
7卷引用:河南省安阳市2021-2022学年高一下学期大联考阶段性测试(五)化学试题
二、解答题 添加题型下试题
解答题-原理综合题
|
适中(0.65)
名校
解题方法
17. 推广氢燃料电池汽车有利于实现“碳中和”的宏伟目标,2022年2月北京冬奥会基本实现100%绿电供应。回答下列有关问题:
(1)氢能是一种具有发展前景的理想清洁能源,氢气燃烧时放出大量的热。氢气燃烧时断裂的化学键是_______ (填“离子键”或“共价键”),若断开1mol氢气中的化学键消耗的能量为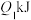 ,断开1mol氧气中的化学键消耗的能量为
,断开1mol氧气中的化学键消耗的能量为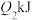 ,形成1mol水中的化学键释放的能量为
,形成1mol水中的化学键释放的能量为 ,则
,则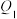 、
、 、
、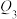 之间的关系为
之间的关系为_______ 。
(2)利用 和
和 在光催化酶作用下可以高效合成甲醇(
在光催化酶作用下可以高效合成甲醇( )。
)。
①甲醇燃烧属于_______ (填“吸热”或“放热”)反应。
②氢气燃料电池在北京冬奥会上得到广泛应用。下图是酸性氢气燃料电池的工作原理示意图:
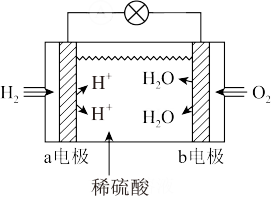
a电极是原电池的_______ (填“正极”或“负极”),该极的电极反应式为_______ ;b电极发生反应_______ (填“氧化”或“还原”);外电路中电子流入的是_______ (填“a”或“b”)电极。
(1)氢能是一种具有发展前景的理想清洁能源,氢气燃烧时放出大量的热。氢气燃烧时断裂的化学键是
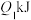 ,断开1mol氧气中的化学键消耗的能量为
,断开1mol氧气中的化学键消耗的能量为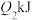 ,形成1mol水中的化学键释放的能量为
,形成1mol水中的化学键释放的能量为 ,则
,则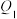 、
、 、
、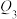 之间的关系为
之间的关系为(2)利用
 和
和 在光催化酶作用下可以高效合成甲醇(
在光催化酶作用下可以高效合成甲醇( )。
)。①甲醇燃烧属于
②氢气燃料电池在北京冬奥会上得到广泛应用。下图是酸性氢气燃料电池的工作原理示意图:

a电极是原电池的
您最近一年使用:0次
2022-07-04更新
|
230次组卷
|
2卷引用:河南省安阳市2021-2022学年高一下学期大联考阶段性测试(五)化学试题
解答题-工业流程题
|
适中(0.65)
18. “玉”为温润而有光泽的美石。《说文解字》记载:“玉,石之美者,有五德,润泽以温,仁之方也。”玉的主要成分是硅酸盐和二氧化硅。由粗 (含少量
(含少量 、
、 杂质)制备纯
杂质)制备纯 的流程如图所示:
的流程如图所示:

回答下列问题:
(1)步骤I中主要反应的化学方程式为_____
(2)步骤II中的过量稀硫酸能否用过量 代替?
代替?_______ (填“能”或“不能”),主要原因是_______ (用离子方程式表示)。
(3)若在实验室中完成步骤III,一般在_______ (填仪器名称)中进行。
(4)制备的纯 可与焦炭在电炉中反应制取粗硅,反应的化学方程式为
可与焦炭在电炉中反应制取粗硅,反应的化学方程式为_______ 。
 (含少量
(含少量 、
、 杂质)制备纯
杂质)制备纯 的流程如图所示:
的流程如图所示:
回答下列问题:
(1)步骤I中主要反应的化学方程式为
(2)步骤II中的过量稀硫酸能否用过量
 代替?
代替?(3)若在实验室中完成步骤III,一般在
(4)制备的纯
 可与焦炭在电炉中反应制取粗硅,反应的化学方程式为
可与焦炭在电炉中反应制取粗硅,反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
较难(0.4)
19. 氨元素是动植物生长不可缺少的元素,图1是自然界中氨元素的循环示意图,图2是氨元素的常见化合价与部分物质类别的对应关系。回答下列问题:
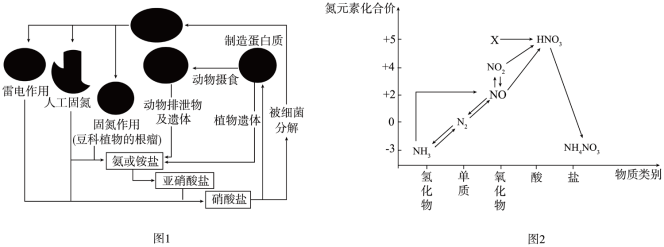
(1)图1中属于固氮过程的是_______ (写两种即可)。
(2) 可以将
可以将 还原为Fe,自身被氧化为
还原为Fe,自身被氧化为 。某学习小组欲制备氨气以还原氧化铁。
。某学习小组欲制备氨气以还原氧化铁。
①下列各装置中常用于实验室制备氨气的是_______ (填字母),利用该装置制备氨气的化学方程式为_______ 。
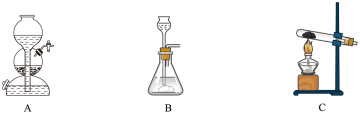
② 还原
还原 并检验有水生成的实验装置如图所示:
并检验有水生成的实验装置如图所示:
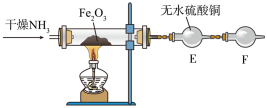
写出氨气与氧化铁反应的化学方程式:_______ 。干燥管F中装有无水氯化钙,其作用是_______ 。
(3)图2中物质X的化学式是_______ ,其与水反应生成 。某硝酸和硫酸的混合溶液200mL,其中硫酸的浓度为
。某硝酸和硫酸的混合溶液200mL,其中硫酸的浓度为 ,硝酸的浓度为
,硝酸的浓度为 ,现向其中加入9.6g铜粉,充分反应生成气体的化学式为
,现向其中加入9.6g铜粉,充分反应生成气体的化学式为_______ (假设只生成一种气体),最多可收集到标准状况下的该气体的体积为_______ L。

(1)图1中属于固氮过程的是
(2)
 可以将
可以将 还原为Fe,自身被氧化为
还原为Fe,自身被氧化为 。某学习小组欲制备氨气以还原氧化铁。
。某学习小组欲制备氨气以还原氧化铁。①下列各装置中常用于实验室制备氨气的是

②
 还原
还原 并检验有水生成的实验装置如图所示:
并检验有水生成的实验装置如图所示:
写出氨气与氧化铁反应的化学方程式:
(3)图2中物质X的化学式是
 。某硝酸和硫酸的混合溶液200mL,其中硫酸的浓度为
。某硝酸和硫酸的混合溶液200mL,其中硫酸的浓度为 ,硝酸的浓度为
,硝酸的浓度为 ,现向其中加入9.6g铜粉,充分反应生成气体的化学式为
,现向其中加入9.6g铜粉,充分反应生成气体的化学式为
您最近一年使用:0次
三、填空题 添加题型下试题
20. 氮的氧化物会对空气造成污染。
(1) 会造成光化学烟雾,一般利用碱液吸收
会造成光化学烟雾,一般利用碱液吸收 防止污染环境,
防止污染环境, 发生歧化反应,氧化产物与还原产物的物质的量比为1:1,则用NaOH溶液吸收
发生歧化反应,氧化产物与还原产物的物质的量比为1:1,则用NaOH溶液吸收 时发生反应的化学方程式为
时发生反应的化学方程式为_______ 。
(2)在 气体中存在
气体中存在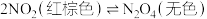 的关系。一定温度下,体积为2L的恒容密闭容器中
的关系。一定温度下,体积为2L的恒容密闭容器中 和
和 的物质的量随时间变化的关系如图所示。回答下列问题:
的物质的量随时间变化的关系如图所示。回答下列问题:
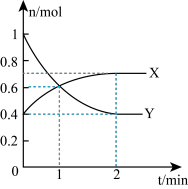
①曲线X表示_______ (填化学式)的物质的量随时间的变化。
②第1min时v(Y)_______ 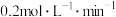 (“>”“<”“=”或“无法确定”)。
(“>”“<”“=”或“无法确定”)。
③反应达到平衡时, 的转化率为
的转化率为_______ 。
④假设上述反应的正反应速率为 、逆反应速率为
、逆反应速率为 ,当温度升高时,
,当温度升高时, 和
和 的变化情况为
的变化情况为_____ 。
⑤下列叙述能表示该反应达到平衡状态的是_______ (填字母)。
a.容器中气体的颜色不再改变
b.容器中 、
、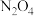 气体的物质的量相等
气体的物质的量相等
c.容器中气体的密度不再改变
d.相同时间内,反应消耗2mol 的同时消耗1mol
的同时消耗1mol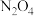
(1)
 会造成光化学烟雾,一般利用碱液吸收
会造成光化学烟雾,一般利用碱液吸收 防止污染环境,
防止污染环境, 发生歧化反应,氧化产物与还原产物的物质的量比为1:1,则用NaOH溶液吸收
发生歧化反应,氧化产物与还原产物的物质的量比为1:1,则用NaOH溶液吸收 时发生反应的化学方程式为
时发生反应的化学方程式为(2)在
 气体中存在
气体中存在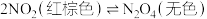 的关系。一定温度下,体积为2L的恒容密闭容器中
的关系。一定温度下,体积为2L的恒容密闭容器中 和
和 的物质的量随时间变化的关系如图所示。回答下列问题:
的物质的量随时间变化的关系如图所示。回答下列问题: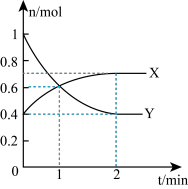
①曲线X表示
②第1min时v(Y)
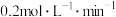 (“>”“<”“=”或“无法确定”)。
(“>”“<”“=”或“无法确定”)。③反应达到平衡时,
 的转化率为
的转化率为④假设上述反应的正反应速率为
 、逆反应速率为
、逆反应速率为 ,当温度升高时,
,当温度升高时, 和
和 的变化情况为
的变化情况为⑤下列叙述能表示该反应达到平衡状态的是
a.容器中气体的颜色不再改变
b.容器中
 、
、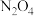 气体的物质的量相等
气体的物质的量相等c.容器中气体的密度不再改变
d.相同时间内,反应消耗2mol
 的同时消耗1mol
的同时消耗1mol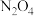
您最近一年使用:0次
四、解答题 添加题型下试题
解答题-无机推断题
|
较难(0.4)
解题方法
21. X是一种重要的化工原料,X的某种同系物的产量可以用来衡量一个国家的石油化工水平。Y是一种具有果香味的合成香料,下图为合成Y的一种流程。
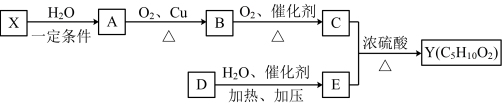
(1)已知有机物E中碳、氢元素的质量分数分别约为52.17%、13.04%,其余为氧元素,E的相对分子质量为46,则E的分子式是_______ 。
(2)X→A的反应类型为_______ 。
(3)A→B反应的化学方程式为_______ ,B中含有官能团的名称是_______ 。
(4)E中含有羟基,则反应C+E→Y的化学方程式为_______ ,该反应中浓硫酸的作用是_______ 。
(5)M是Y的同分异构体,符合下列条件的M有_______ 种(不考虑立体异构)。
①能与银氨溶液反应;②能和钠反应

(1)已知有机物E中碳、氢元素的质量分数分别约为52.17%、13.04%,其余为氧元素,E的相对分子质量为46,则E的分子式是
(2)X→A的反应类型为
(3)A→B反应的化学方程式为
(4)E中含有羟基,则反应C+E→Y的化学方程式为
(5)M是Y的同分异构体,符合下列条件的M有
①能与银氨溶液反应;②能和钠反应
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:化学反应原理、常见无机物及其应用、认识化学科学、有机化学基础、化学与STSE、物质结构与性质、化学实验基础
试卷题型(共 21题)
题型
数量
单选题
16
解答题
4
填空题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 原电池原理理解 原电池原理的综合应用 | |
| 2 | 0.65 | 二氧化硫的弱氧化性 二氧化硅的化学性质 二氧化硅与二氧化碳结构与性质的比较 | |
| 3 | 0.85 | 氧化还原反应有关计算 化学反应中能量变化的原因 能量的相互转化 | |
| 4 | 0.65 | 氧化还原反应基本概念 加聚物的单体、链节及聚合度的确定 绿色化学与可持续发展 海水资源综合利用 | |
| 5 | 0.85 | 化学反应速率计算 化学平衡图像分析 化学平衡状态的判断方法 | |
| 6 | 0.85 | 根据元素种类、原子个数、有机物类别确定分子式 羧酸的酸性 多官能团有机物的结构与性质 | |
| 7 | 0.65 | 有机反应类型 甲烷分子空间构型 乙烯的加成反应 乙烯与强氧化性物质的反应 | |
| 8 | 0.65 | 原电池原理理解 原电池电极反应式书写 铅蓄电池 | |
| 9 | 0.65 | 乙酸乙酯制备实验的装置及操作 元素金属性、非金属性强弱探究实验 实验安全 萃取和分液 | |
| 10 | 0.65 | 常见氧化剂与还原剂 氧化还原反应方程式的配平 影响化学反应速率的因素 化学实验基础操作 | |
| 11 | 0.94 | 浓度对化学反应速率的影响 温度对化学反应速率的影响 | |
| 12 | 0.65 | 酸、碱、盐、氧化物的概念及其相互联系 一氧化氮 二氧化硫的漂白性 二氧化硅的化学性质 | |
| 13 | 0.65 | 影响化学反应速率的因素 有机反应类型 同分异构现象、同分异构体的概念 淀粉和纤维素 | |
| 14 | 0.85 | 能量的相互转化 影响化学反应速率的因素 | |
| 15 | 0.85 | 原电池原理理解 原电池电子流向判断及应用 原电池正负极判断 原电池电极反应式书写 | |
| 16 | 0.65 | 物质的转化 氧化还原反应的规律 无机综合推断 含硫化合物之间的转化 | |
| 二、解答题 | |||
| 17 | 0.65 | 化学反应热的计算 原电池正负极判断 原电池电极反应式书写 化学键概念理解及判断 | 原理综合题 |
| 18 | 0.65 | 二氧化硅 硅的制备 二氧化硅的化学性质 | 工业流程题 |
| 19 | 0.4 | 氧化还原反应有关计算 氨的还原性 氨气的实验室制法 硝酸的强氧化性 | 实验探究题 |
| 21 | 0.4 | 有机反应类型 同分异构体的数目的确定 乙烯的加成反应 有机物的推断 | 无机推断题 |
| 三、填空题 | |||
| 20 | 0.65 | 氧化还原反应方程式的配平 化学反应速率计算 化学平衡的移动及其影响因素 化学平衡状态的判断方法 | |



