名校
解题方法
1 . 氨基甲酸铵是一种白色固体,易水解,是工业上生产尿素的副产物,可以用于药物合成。实验室向四氯化碳中通入干燥的二氧化碳和氨气制取氨基甲酸铵固体,实验装置如下图,反应的化学方程式为 。
。
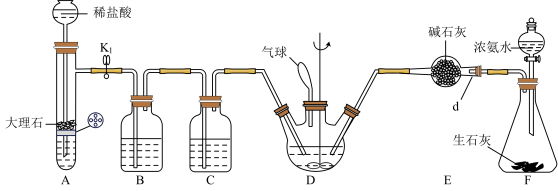
回答下列问题:
(1)仪器d的名称为
___________ ;装置F中发生反应的化学方程式为
___________ 。
(2)装置B中盛放的试剂为
___________ 。
(3)装置D中气球的作用是
___________ 。
(4)反应过程中需要将装置D放入冰水浴中,原因是
___________ 。
(5)氨基甲酸铵易水解,在潮湿的空气中发生水解反应生成碳酸氢铵的化学方程式为
________ 。
(6)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品
 ,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得其质量为
,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得其质量为
 。则样品中氨基甲酸铵的物质的量分数为
。则样品中氨基甲酸铵的物质的量分数为
___________ 。(碳酸氢铵和氨基甲酸铵的相对分子质量分别为79和78)。
 。
。
回答下列问题:
(1)仪器d的名称为
(2)装置B中盛放的试剂为
(3)装置D中气球的作用是
(4)反应过程中需要将装置D放入冰水浴中,原因是
(5)氨基甲酸铵易水解,在潮湿的空气中发生水解反应生成碳酸氢铵的化学方程式为
(6)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品
 ,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得其质量为
,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得其质量为 。则样品中氨基甲酸铵的物质的量分数为
。则样品中氨基甲酸铵的物质的量分数为
您最近一年使用:0次
名校
2 . 氨基甲酸铵( )是一种重要的化工原料,可用作化学肥料、灭火剂洗涤剂等。某化学兴趣小组用以下装置模拟工业原理制备氨基甲酸铵。
)是一种重要的化工原料,可用作化学肥料、灭火剂洗涤剂等。某化学兴趣小组用以下装置模拟工业原理制备氨基甲酸铵。
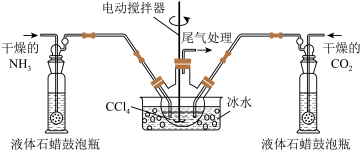
已知:①制取氨基甲酸铵反应为: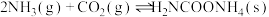
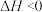 。
。
②氨基甲酸铵易分解、易吸水,溶于水后生成碳酸氢铵和一水合氨。
③四氯化碳与液体石蜡均为惰性介质。
回答下列问题:
(1)若用如图所示装置制取氨气,你所选择的试剂是_______ 。
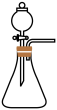
(2)液体石蜡鼓泡瓶的作用是_______ ,尾气处理装置中的试剂是_______ 。
(3)三颈烧瓶需用冰水浴冷却,其目的是_______ 。
(4) 液体中产生较多晶体悬浮物时,即停止反应,从三颈烧瓶中分离出粗产品的操作是
液体中产生较多晶体悬浮物时,即停止反应,从三颈烧瓶中分离出粗产品的操作是_______ 。
(5)将一定量纯净的氨基甲酸铵固体置于密闭真空容器中(容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到平衡: 。可以判断该反应已经达到平衡的是_______。
。可以判断该反应已经达到平衡的是_______。
(6)因部分变质而混有碳酸氢铵的氨基甲酸铵样品1.173g,用足量石灰水充分反应后,使碳元素全部转化为碳酸钙,经过滤、洗涤、干燥后称量,测得质量为1.500g。样品中氨基甲酸铵的质量分数是_______ 。(计算结果保留四位有效数字)[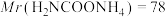 、
、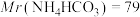 ]
]
 )是一种重要的化工原料,可用作化学肥料、灭火剂洗涤剂等。某化学兴趣小组用以下装置模拟工业原理制备氨基甲酸铵。
)是一种重要的化工原料,可用作化学肥料、灭火剂洗涤剂等。某化学兴趣小组用以下装置模拟工业原理制备氨基甲酸铵。
已知:①制取氨基甲酸铵反应为:
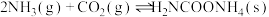
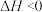 。
。②氨基甲酸铵易分解、易吸水,溶于水后生成碳酸氢铵和一水合氨。
③四氯化碳与液体石蜡均为惰性介质。
回答下列问题:
(1)若用如图所示装置制取氨气,你所选择的试剂是

(2)液体石蜡鼓泡瓶的作用是
(3)三颈烧瓶需用冰水浴冷却,其目的是
(4)
 液体中产生较多晶体悬浮物时,即停止反应,从三颈烧瓶中分离出粗产品的操作是
液体中产生较多晶体悬浮物时,即停止反应,从三颈烧瓶中分离出粗产品的操作是(5)将一定量纯净的氨基甲酸铵固体置于密闭真空容器中(容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到平衡:
 。可以判断该反应已经达到平衡的是_______。
。可以判断该反应已经达到平衡的是_______。A. |
| B.容器中总压强不变 |
| C.容器中混合气体的平均相对分子质量不变 |
| D.容器中氨气的体积分数不变 |
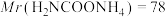 、
、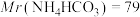 ]
]
您最近一年使用:0次
2022-11-01更新
|
162次组卷
|
2卷引用:湖北省武汉市洪山高级中学2022-2023学年高二上学期开学考试化学试题
名校
3 . 氨基甲酸铵(H2NCOONH4)是一种重要的化工原料,可用作化学肥料、灭火剂洗涤剂等。某化学兴趣小组用以下装置制取氨基甲酸铵。
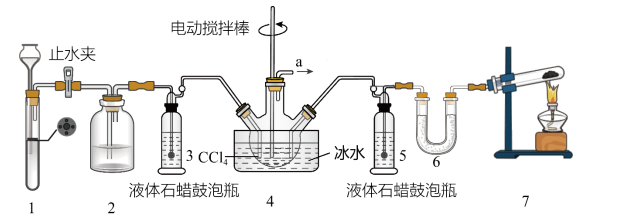
已知:①制取氨基甲酸铵反应为:2NH3(g)+CO2(g) H2NCOONH4(s) △H<0。
H2NCOONH4(s) △H<0。
②氨基甲酸铵易分解、易吸水,溶于水后生成碳酸氢铵和一水合氨。
回答下列问题:
(1)检查装置1气密性的操作是______ 。
(2)装置6中的试剂是_____ ,导管a出口直接与尾气处理装置连接,该尾气处理装置中的试剂是______ 。
(3)装置7中发生反应的化学方程式为_____ 。
(4)三颈烧瓶需用冰水浴冷却,其目的是_____ 。
(5)CCl4液体中产生较多晶体悬浮物时,即停止反应。停止反应的操作是_____ ,从三颈烧瓶中分离出粗产品的操作是_____ 。
(6)因部分变质而混有碳酸氢铵的氨基甲酸铵样品1.173g,用足量石灰水充分反应后,使碳元素全部转化为碳酸钙,经过滤、洗涤、干燥后称量,测得质量为1.500g。写出石灰水与氨基甲酸铵反应转化为碳酸钙的反应方程式____ 。样品中氨基甲酸铵的质量分数是_____ 。(计算结果保留小数点后两位)[Mr(H2NCOONH4)=78、Mr(NH4HCO3)=79]

已知:①制取氨基甲酸铵反应为:2NH3(g)+CO2(g)
 H2NCOONH4(s) △H<0。
H2NCOONH4(s) △H<0。②氨基甲酸铵易分解、易吸水,溶于水后生成碳酸氢铵和一水合氨。
回答下列问题:
(1)检查装置1气密性的操作是
(2)装置6中的试剂是
(3)装置7中发生反应的化学方程式为
(4)三颈烧瓶需用冰水浴冷却,其目的是
(5)CCl4液体中产生较多晶体悬浮物时,即停止反应。停止反应的操作是
(6)因部分变质而混有碳酸氢铵的氨基甲酸铵样品1.173g,用足量石灰水充分反应后,使碳元素全部转化为碳酸钙,经过滤、洗涤、干燥后称量,测得质量为1.500g。写出石灰水与氨基甲酸铵反应转化为碳酸钙的反应方程式
您最近一年使用:0次
4 . 氨基甲酸铵(NH2COONH4)是一种受热易分解、易水解的白色固体,难溶于CCl4。实验室将干燥的二氧化碳和干燥的氨气通入CCl4中进行制备,化学方程式为:2NH3(g)+CO2(g)=NH2COONH4(s) △H<0。某同学从如图装置(不能重复使用)中选用一部分连接后进行实验。
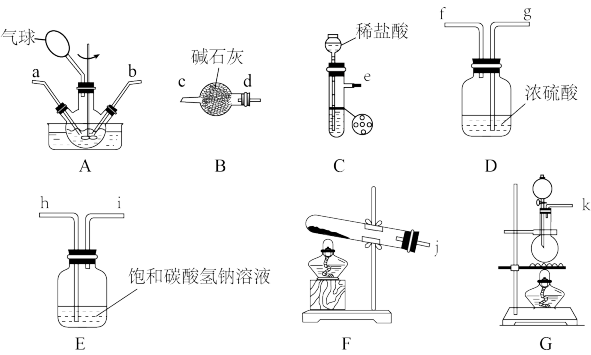
回答下列问题:
(1)氨气的发生装置可以选择图中的___ (填序号,用大写字母表示),反应的化学方程式为___ 。
(2)装置C用来制备二氧化碳气体,块状石灰石放置在试管中的带孔塑料板上。制备时,不能用稀硫酸代替稀盐酸,其原因是___ 。
(3)选择上图中的部分装置制备NH2COONH4,其连接顺序为:氨气的发生装置→__ →ab←___ ←e(按气流方向,用小写字母表示)。
(4)反应时三颈瓶需用冷水浴冷却,其目的是___ 。
(5)从装置A的混合物中分离出产品的方法是___ (填操作名称)。
(6)氨基甲酸铵因吸潮会变质为碳酸氢铵,现取部分变质后的样品11.730g,用足量石灰水充分处理后,碳元素会完全转化为碳酸钙,再过滤、洗涤、干燥、称量,质量为15.000g。则样品中氨基甲酸铵的物质的量分数 为___ %。[已知:M(NH2COONH4)=78g/mol、M(NH4HCO3)=79g/mol、M(CaCO3)=100g/mol]

回答下列问题:
(1)氨气的发生装置可以选择图中的
(2)装置C用来制备二氧化碳气体,块状石灰石放置在试管中的带孔塑料板上。制备时,不能用稀硫酸代替稀盐酸,其原因是
(3)选择上图中的部分装置制备NH2COONH4,其连接顺序为:氨气的发生装置→
(4)反应时三颈瓶需用冷水浴冷却,其目的是
(5)从装置A的混合物中分离出产品的方法是
(6)氨基甲酸铵因吸潮会变质为碳酸氢铵,现取部分变质后的样品11.730g,用足量石灰水充分处理后,碳元素会完全转化为碳酸钙,再过滤、洗涤、干燥、称量,质量为15.000g。则样品中氨基甲酸铵的
您最近一年使用:0次
解题方法
5 . 氨基甲酸铵(H2NCOONH4)是一种重要的化工原料,可用作化学肥料、灭火剂、洗涤剂等。某化学兴趣小组用以下装置制取氨基甲酸铵。
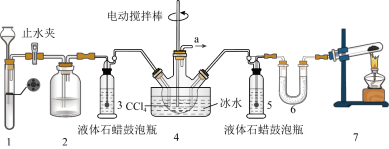
已知:①制取氨基甲酸铵反应为: 2NH3(g)+CO2(g)⇌H2NCOONH4(s) △H<0。
②氨基甲酸铵易分解、易吸水,溶于水后生成碳酸氢铵和一水合氨。
回答下列问题:
(1)检查装置1气密性的操作是_______
(2)装置6中的试剂是_______ ,导管a出口直接与尾气处理装置连接,该尾气处理装置中的试剂是_______ 。
(3)装置7中发生反应的化学方程式为_______
(4)三颈烧瓶需用冰水浴冷却,其目的是_______
(5) CCl4液体中产生较多晶体悬浮物时,即停止反应。停止反应的操作是_______ ,从三颈烧瓶中分离出粗产品的操作是_______
(6)因部分变质而混有碳酸氢铵的氨基甲酸铵样品1.173g,用足量石灰水充分反应后,使碳元素全部转化为碳酸钙,经过滤、洗涤、干燥后称量,测得质量为1.500g。样品中氨基甲酸铵的质量分数是_______ [Mr(H2NCOONH4)=78、Mr(NH4HCO3)=79]

已知:①制取氨基甲酸铵反应为: 2NH3(g)+CO2(g)⇌H2NCOONH4(s) △H<0。
②氨基甲酸铵易分解、易吸水,溶于水后生成碳酸氢铵和一水合氨。
回答下列问题:
(1)检查装置1气密性的操作是
(2)装置6中的试剂是
(3)装置7中发生反应的化学方程式为
(4)三颈烧瓶需用冰水浴冷却,其目的是
(5) CCl4液体中产生较多晶体悬浮物时,即停止反应。停止反应的操作是
(6)因部分变质而混有碳酸氢铵的氨基甲酸铵样品1.173g,用足量石灰水充分反应后,使碳元素全部转化为碳酸钙,经过滤、洗涤、干燥后称量,测得质量为1.500g。样品中氨基甲酸铵的质量分数是
您最近一年使用:0次
解题方法
6 . 氨基甲酸铵(NH2COONH4)是一种易分解、易水解的白色固体、难溶于CCl4。实验室可将干燥二氧化碳和氨气通入CCl4中进行制备,反应原理为2NH3(g)+CO2(g)=NH2COONH4(s) △H<0,回答下列问题:
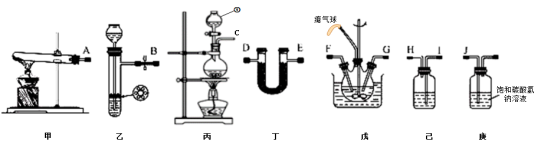
(1)仪器①的名称为_____ ,装置己中盛放的试剂为_____ 。
(2)简述检验装置乙气密性的操作_____ 。
(3)氨气的发生装置可以选择上图中的_____ ,制取氨气的化学方程式为_____ 。
(4)预制备产品,选择上图中必要的装置,其连接顺序为:发生装置→_____ →FG←_____ ←KJ←_____ (按气流方向,用大写字母表示)。
(5)为了提高氨基甲酸铵的产率.对三颈瓶采取的控温方法是_____ ,反应结束后,从反应后的混合物中分离出产品的实验操作是_____ ,戊中气球的作用是_____ 。
(6)氨基甲酸铵容易变质生成碳酸氢铵,现取长期存放的样品19.550g,用足量石灰水处理后,使样品中碳元素完全转化为碳酸钙,通过系列操作得纯净碳酸钙25.000g,则该样品的纯度为_____ %。(计算结果保留三位有效数字;有关物质的相对式量:氨基甲酸铵78、碳酸氢铵79、碳酸钙100) 。

(1)仪器①的名称为
(2)简述检验装置乙气密性的操作
(3)氨气的发生装置可以选择上图中的
(4)预制备产品,选择上图中必要的装置,其连接顺序为:发生装置→
(5)为了提高氨基甲酸铵的产率.对三颈瓶采取的控温方法是
(6)氨基甲酸铵容易变质生成碳酸氢铵,现取长期存放的样品19.550g,用足量石灰水处理后,使样品中碳元素完全转化为碳酸钙,通过系列操作得纯净碳酸钙25.000g,则该样品的纯度为
您最近一年使用:0次
7 . 氨基甲酸铵(NH2COONH4)是一种易分解、易水解的白色固体,难溶于CCl4。实验室可将干燥二氧化碳和干燥氨气通入CCl4中进行制备,化学方程式为:2NH3(g)+CO2(g)=NH2COONH4(s) ΔH<0。
回答下列问题:
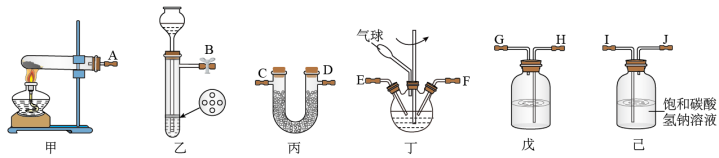
(1)利用装置甲制备氨气的化学方程式为__ 。
(2)简述检查装置乙气密性的操作__ 。
(3)选择图中的装置制备氨基甲酸铵,仪器接口的连接顺序为:B→__ →__ →EF←__ ←A。
(4)反应时为了增加氨基甲酸铵的产量,三颈瓶的加热方式为__ (填“热水浴”或“冷水浴”);丁中气球的作用是__ 。
(5)从装置丁的混合物中分离出产品的方法是__ (填写操作名称)。
(6)取因吸潮变质为碳酸氢铵的氨基甲酸铵样品11.730g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥、称量,质量为15.000g。则样品中氨基甲酸铵的质量分数为__ (已知:Mr(NH2COONH4)=78、Mr(NH4HCO3)=79、Mr(CaCO3)=100。计算结果保留3位有效数字)。
回答下列问题:

(1)利用装置甲制备氨气的化学方程式为
(2)简述检查装置乙气密性的操作
(3)选择图中的装置制备氨基甲酸铵,仪器接口的连接顺序为:B→
(4)反应时为了增加氨基甲酸铵的产量,三颈瓶的加热方式为
(5)从装置丁的混合物中分离出产品的方法是
(6)取因吸潮变质为碳酸氢铵的氨基甲酸铵样品11.730g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥、称量,质量为15.000g。则样品中氨基甲酸铵的质量分数为
您最近一年使用:0次
2020-03-14更新
|
239次组卷
|
2卷引用:武汉市2020届高中毕业生学生质量检测化学试题
名校
解题方法
8 . 氨基甲酸铵(NH2COONH4)是治疗某种疾病的重要成分,也可用作肥料。氨基甲酸铵是一种白色固体,易分解、易水解,难溶于CCl4。实验小组设计在实验室中用氨气和二氧化碳反应制备氨基甲酸铵。
(1)氨气的制备
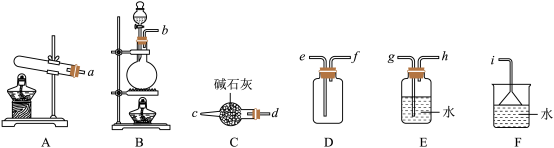
①实验室制取氨气的发生装置可以选择图中的__ ,反应的化学方程式为__ 。
②欲收集一瓶干燥的氨气,选择图中的装置,其连接顺序为:发生装置→__ 。(按气流方向,用小写字母表示)。
(2)氨基甲酸铵(NH2COONH4)的制备把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中。当悬浮物较多时,停止制备。制备氨基甲酸铵的装置和反应的化学方程式如下:2NH3(g)+CO2(g) NH2COONH4(s) △H<0。
NH2COONH4(s) △H<0。
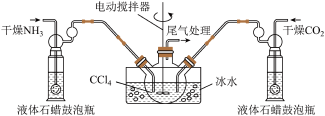
注:四氯化碳与液体石蜡均为惰性介质。
①发生器用冰水冷却的目的是___ 。
②液体石蜡鼓泡瓶的作用是__ 。
③从反应后的混合物中分离出产品的方法是__ (填写操作名称)。
④尾气处理装置如图所示,装置中的浓硫酸的作用除了用于阻止空气中水蒸气进入反应器使氨基甲酸铵水解,还用于__ 。
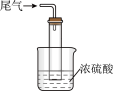
⑤取因部分变质而混有碳酸氢铵的氨基甲酸铵样品0.7820g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.000 g。则样品中氨基甲酸铵的物质的量分数为__ 。(精确到2位小数,碳酸氢铵和氨基甲酸铵的相对分子质量分别为79和78)
(1)氨气的制备

①实验室制取氨气的发生装置可以选择图中的
②欲收集一瓶干燥的氨气,选择图中的装置,其连接顺序为:发生装置→
(2)氨基甲酸铵(NH2COONH4)的制备把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中。当悬浮物较多时,停止制备。制备氨基甲酸铵的装置和反应的化学方程式如下:2NH3(g)+CO2(g)
 NH2COONH4(s) △H<0。
NH2COONH4(s) △H<0。
注:四氯化碳与液体石蜡均为惰性介质。
①发生器用冰水冷却的目的是
②液体石蜡鼓泡瓶的作用是
③从反应后的混合物中分离出产品的方法是
④尾气处理装置如图所示,装置中的浓硫酸的作用除了用于阻止空气中水蒸气进入反应器使氨基甲酸铵水解,还用于

⑤取因部分变质而混有碳酸氢铵的氨基甲酸铵样品0.7820g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.000 g。则样品中氨基甲酸铵的物质的量分数为
您最近一年使用:0次
解题方法
9 . 三颈瓶在化学实验中的应用非常广泛,下面是三颈瓶在部分无机实验或有机实验中的一些应用。
(1)在如图所示装置中,进行氨的催化氧化实验:向三颈瓶内的浓氨水中不断通入空气,将红热的铂丝插入瓶子并接近液面。反应过程中可观察到瓶中有红棕色气体产生,铂丝始终保持红热。实验过程中NH3∙H2O的电离程度____ (填“变大”、“变小”或“不变”)
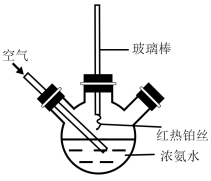
Ⅱ.实验室用下图所示装置制备氨基甲酸铵(NH2COONH4),其反应化学方程式:2NH3(g)+CO2(g) NH2COONH4(s)该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则生成碳酸铵或碳酸氢铵。
NH2COONH4(s)该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则生成碳酸铵或碳酸氢铵。
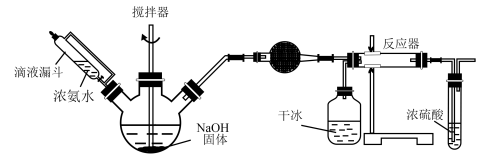
(2)写出加入药品之前实验操作的要点_______ ;反应中若有水存在则生成碳酸氢铵的化学方程式是________________________ 。
(3)干燥管中盛放的药品是______ 。简述左侧三颈瓶装置制取氨气的原理________ 。
(4)对比碳酸盐和酸的反应制取CO2,该实验利用干冰升华产生气体CO2的有优点有_____ .
(5)有同学认为该实验装置存在安全问题,请问可能面临的安全问题是________ 。
(6)氨基甲酸氨可用作肥料,其肥效比尿素[CO(NH2)2]_______ (填“高”或“低”),在潮湿的空气中释放出氨而变成碳酸氢铵。取因部分变质而混有碳酸氢铵的氨基甲酸铵样品0.7830g,用足量石灰水充分处理后,使样品中碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.000g,则样品中氨基甲酸铵的物质的量分数是_____________ 。
(1)在如图所示装置中,进行氨的催化氧化实验:向三颈瓶内的浓氨水中不断通入空气,将红热的铂丝插入瓶子并接近液面。反应过程中可观察到瓶中有红棕色气体产生,铂丝始终保持红热。实验过程中NH3∙H2O的电离程度

Ⅱ.实验室用下图所示装置制备氨基甲酸铵(NH2COONH4),其反应化学方程式:2NH3(g)+CO2(g)
 NH2COONH4(s)该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则生成碳酸铵或碳酸氢铵。
NH2COONH4(s)该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则生成碳酸铵或碳酸氢铵。
(2)写出加入药品之前实验操作的要点
(3)干燥管中盛放的药品是
(4)对比碳酸盐和酸的反应制取CO2,该实验利用干冰升华产生气体CO2的有优点有
(5)有同学认为该实验装置存在安全问题,请问可能面临的安全问题是
(6)氨基甲酸氨可用作肥料,其肥效比尿素[CO(NH2)2]
您最近一年使用:0次
名校
解题方法
10 . 氨基甲酸铵(H2NCOONH4)是一种易分解、易水解的白色固体,可用于化肥、灭火剂、洗涤剂等。某化学兴趣小组模拟工业原理制备氨基甲酸铵:
反应式:2NH3(g)+CO2(g) H2NCOONH4△H <0
H2NCOONH4△H <0
(1)如果使用如图所示的装置制取NH3,你所选择的试剂是_____________ 。

(2)备氨基甲酸铵的装置如下图。把氨和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中,当悬浮物较多时,停止制备:(注:四氯化碳与液体石蜡均为惰性介质。)
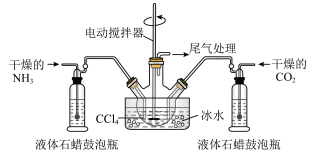
①发生器用冰水冷却的原因是_______ ,液体石蜡鼓泡瓶的作用是__________ ,发生反应的仪器名称是_______________ 。
②从反应后的混合物中过滤分离出产品。为了得到干燥产品,应采取的方法是_____ (选填序号)
a.常压加热烘干 b.高压加热烘干 c.真空40℃以下烘干
(3)尾气有污染,可用________ 溶液吸收处理。
(4)取因部分变质而混有碳酸氢铵的氨基甲酸铵钱样品1.1730g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.500g。样品中氨基甲酸铵的物质的量分数为__________ 。[已知Mr(H2NCOONH4)=78, Mr(NH4HCO3)=79, Mr(CaCO3)=100]
反应式:2NH3(g)+CO2(g)
 H2NCOONH4△H <0
H2NCOONH4△H <0(1)如果使用如图所示的装置制取NH3,你所选择的试剂是

(2)备氨基甲酸铵的装置如下图。把氨和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中,当悬浮物较多时,停止制备:(注:四氯化碳与液体石蜡均为惰性介质。)

①发生器用冰水冷却的原因是
②从反应后的混合物中过滤分离出产品。为了得到干燥产品,应采取的方法是
a.常压加热烘干 b.高压加热烘干 c.真空40℃以下烘干
(3)尾气有污染,可用
(4)取因部分变质而混有碳酸氢铵的氨基甲酸铵钱样品1.1730g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.500g。样品中氨基甲酸铵的物质的量分数为
您最近一年使用:0次
2017-03-15更新
|
810次组卷
|
3卷引用:2017届四川省成都市第七中学高三二诊模拟考试理综化学试卷



