名校
解题方法
1 . 氨和硝酸是重要的化工产品,工业合成氨及制备硝酸的流程如图:

下列说法错误的是

下列说法错误的是
| A.“氨分离器”中主要应用了氨气易液化的性质 |
| B.工业上可用铁槽车储运浓硝酸 |
| C.流程中的转化涉及复分解反应 |
| D.为提高氮的利用率,尾气可循环进入“合成塔” |
您最近一年使用:0次
2023-03-23更新
|
607次组卷
|
8卷引用:福建省泉州市2022届高中毕业班质量检测(三)化学试题
福建省泉州市2022届高中毕业班质量检测(三)化学试题福建省泉州市2022届高三下学期3月质量监测(三)化学试题(已下线)第18讲 硝酸的性质-【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)福建省福州第一中学2022-2023学年高一下学期4月期中考试化学试题江苏省邳州市宿羊山高级中学2022-2023学年高一下学期第一次学情检测化学试题广东省深圳市观澜中学2022-2023学年高一下学期3月月考化学试题(已下线)四川省遂宁中学2022-2023学年高一下学期期中考试化学试题(已下线)化学-2023年高考押题预测卷02(云南,安徽,黑龙江,山西,吉林五省通用)(含考试版、全解全析、参考答案、答题卡)
名校
2 . 用石灰乳吸收硝酸工业的尾气(含NO、NO2)可获得Ca(NO2)2,其部分工艺流程如下:
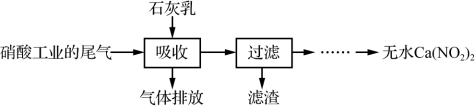
下列说法不正确的是

下列说法不正确的是
| A.用石灰乳比用澄清石灰水吸收效果更好 |
| B.采用气液逆流接触有利于尾气中NO、NO2的充分吸收 |
C.吸收时主要反应的离子方程式为NO+NO2+2OH-=2NO +H2O +H2O |
| D.若尾气中n(NO2):n(NO)<1∶1,吸收后排放的气体中NO含量升高 |
您最近一年使用:0次
3 . 已知A、B、C为化合物,X为单质。其中,A是一种能使湿润的红色石蕊试纸变蓝的气体;X为双原子分子,其原子的最外层电子数为内层的3倍。A、B、C、X之间存在如下转化关系:

请回答:
(1)X的化学式为_______ 。
(2)B转化为C的化学方程式为_______ 。C是一种_______ 色气体。
(3)工业上以NH3、空气、水为原料生产硝酸:
①NH3→NO的化学方程式为_______ ;
②NO→NO2的实验现象是_______ 。
(4)若要实现NH3→N2,从原理上看,下列试剂可行的是_______。

请回答:
(1)X的化学式为
(2)B转化为C的化学方程式为
(3)工业上以NH3、空气、水为原料生产硝酸:
①NH3→NO的化学方程式为
②NO→NO2的实验现象是
(4)若要实现NH3→N2,从原理上看,下列试剂可行的是_______。
| A.O2 | B.Na | C.NH4Cl | D.NO2 |
您最近一年使用:0次
名校
4 . 简要回答下列问题。
(1)NO暴露在空气中,出现红棕色的原因是________ 。
(2)将食品置于低温条件下,常常可以保存更长时间的原因是________ 。
(3)盛有浓硫酸的容器敞口放置一段时间后,硫酸浓度变小的原因是________ 。
(4)推广使用新能源汽车的目的是________ 。
(1)NO暴露在空气中,出现红棕色的原因是
(2)将食品置于低温条件下,常常可以保存更长时间的原因是
(3)盛有浓硫酸的容器敞口放置一段时间后,硫酸浓度变小的原因是
(4)推广使用新能源汽车的目的是
您最近一年使用:0次
名校
5 . 下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
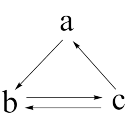
| a | b | c | |
| A |  |  |  |
| B |  |  |  |
| C |  | S |  |
| D |  |  |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-09-02更新
|
410次组卷
|
8卷引用:福建省龙岩市2021-2022学年高一上学期期末考试化学试题
名校
解题方法
6 . 如图是某元素的价一类二维图,其中A为正盐,X是一种强碱,通常条件下Z是无色液体,E的相对分子质量比D大16,各物质的转化关系如图所示。下列说法错误的是


| A.物质A作肥料时不适合与草木灰混合施用 | B.物质B是弱电解质,其水溶液呈弱碱性 |
| C.物质C一般用排水法收集 | D.D→E的反应可用于检验D |
您最近一年使用:0次
2022-08-29更新
|
375次组卷
|
3卷引用:福建省宁德第一中学2023届高三上学期一模考试化学试题
名校
7 . 工业或机动车尾气中的NOx会造成环境问题,可用多种方法脱除。
(1)碱液吸收:NaOH溶液可吸收硝酸工业尾气(含 ),获得副产品
),获得副产品 。
。
①等物质的量NO与NO2被NaOH溶液吸收,反应的离子方程式为_______ 。
②若吸收时NO与NO2比例控制不当,则吸收液经浓缩结晶、过滤得到 晶体中最有可能混有的杂质是
晶体中最有可能混有的杂质是_______ (填化学式)。排放的尾气中含量较高的氮氧化物是_______ (填化学式)。
(2)还原法:尿素水溶液热解产生的NH3可去除尾气中的NOx,流程如下:
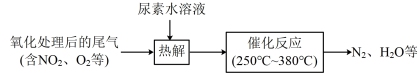
①尿素 中氮元素的化合价为
中氮元素的化合价为_______ 。
②写出“催化反应”过程中NH3还原NO2的化学方程式_______ 。
③若氧化处理后的尾气中混有SO2,此时催化剂表面会因为覆盖部分硫酸盐而导致催化剂中毒,降低NOx的去除率。试分析硫酸盐的产生过程_______ 。
④“催化反应”过程中需控制温度在 之间。温度过高,NOx的去除率下降,其原因可能是温度过高催化剂的活性降低和
之间。温度过高,NOx的去除率下降,其原因可能是温度过高催化剂的活性降低和_______ 。
(1)碱液吸收:NaOH溶液可吸收硝酸工业尾气(含
 ),获得副产品
),获得副产品 。
。①等物质的量NO与NO2被NaOH溶液吸收,反应的离子方程式为
②若吸收时NO与NO2比例控制不当,则吸收液经浓缩结晶、过滤得到
 晶体中最有可能混有的杂质是
晶体中最有可能混有的杂质是(2)还原法:尿素水溶液热解产生的NH3可去除尾气中的NOx,流程如下:

①尿素
 中氮元素的化合价为
中氮元素的化合价为②写出“催化反应”过程中NH3还原NO2的化学方程式
③若氧化处理后的尾气中混有SO2,此时催化剂表面会因为覆盖部分硫酸盐而导致催化剂中毒,降低NOx的去除率。试分析硫酸盐的产生过程
④“催化反应”过程中需控制温度在
 之间。温度过高,NOx的去除率下降,其原因可能是温度过高催化剂的活性降低和
之间。温度过高,NOx的去除率下降,其原因可能是温度过高催化剂的活性降低和
您最近一年使用:0次
2022-08-29更新
|
1034次组卷
|
3卷引用:福建省莆田第二十五中学2022-2023学年高三上学期期中考试化学试题
8 . 工业上用NH3做原料,制取硝酸,要经过三步主要反应,请写出第二步和第三步反应的化学方程式。
第一步反应:4NH3+5O2 4NO+6H2O
4NO+6H2O
第二步反应:_____________________ ;
第三步反应:____________________ 。
第一步反应:4NH3+5O2
 4NO+6H2O
4NO+6H2O第二步反应:
第三步反应:
您最近一年使用:0次
9 . 除去相关物质中的杂质,所选试剂正确的是
| 选项 | 待提纯物质 | 杂质 | 除杂试剂 |
| A |  |  | 盐酸 |
| B |  |  |  |
| C |  | NO |  |
| D |  |  | 铁粉 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 亚硝酸钠是一种工业盐,在生产、生活中应用广泛。现用如图所示装置 夹持装置已省略
夹持装置已省略 及药品,探究亚硝酸钠与硫酸反应及气体产物成分。
及药品,探究亚硝酸钠与硫酸反应及气体产物成分。
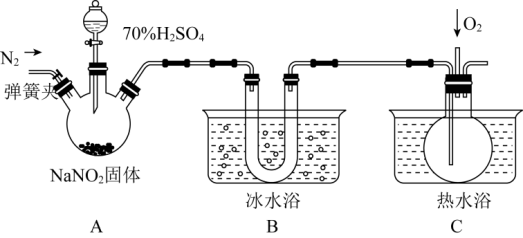
已知:①NO+NO2+2OH-=2NO +H2O;②气体液化的温度:NO221℃、NO-152℃;③HNO2易分解生成NO、NO2和H2O。
+H2O;②气体液化的温度:NO221℃、NO-152℃;③HNO2易分解生成NO、NO2和H2O。
(1)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是____ 。
(2)在关闭弹簧夹,打开分液漏斗活塞,滴入70%硫酸后,A中产生红棕色气体。
①确认A中产生的气体含有NO,依据的现象是____ 。
②装置B的作用是____ 。
(3)通过上述实验探究过程,可得出装置A中反应的化学方程式是____ 。
(4)该实验装置明显缺陷是_____ 。
(5)设计实验证明酸性条件下NaNO2具有氧化性,供选用的试剂:NaNO2溶液、KMnO4溶液、FeSO4溶液、稀硫酸、KSCN溶液。
实验方案具体为:_____ 。
 夹持装置已省略
夹持装置已省略 及药品,探究亚硝酸钠与硫酸反应及气体产物成分。
及药品,探究亚硝酸钠与硫酸反应及气体产物成分。
已知:①NO+NO2+2OH-=2NO
 +H2O;②气体液化的温度:NO221℃、NO-152℃;③HNO2易分解生成NO、NO2和H2O。
+H2O;②气体液化的温度:NO221℃、NO-152℃;③HNO2易分解生成NO、NO2和H2O。(1)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是
(2)在关闭弹簧夹,打开分液漏斗活塞,滴入70%硫酸后,A中产生红棕色气体。
①确认A中产生的气体含有NO,依据的现象是
②装置B的作用是
(3)通过上述实验探究过程,可得出装置A中反应的化学方程式是
(4)该实验装置明显缺陷是
(5)设计实验证明酸性条件下NaNO2具有氧化性,供选用的试剂:NaNO2溶液、KMnO4溶液、FeSO4溶液、稀硫酸、KSCN溶液。
实验方案具体为:
您最近一年使用:0次



