名校
1 . 将4g铁粉与2.5g硫粉在研钵中充分混合后装入试管中,在试管口塞上带长导管的橡皮塞,并在导管末端放入一小团蘸有NaOH溶液的棉花,加热试管。


(1)写出铁与硫反应的化学方程式___________ 。
(2)已知硫的熔点为106.8℃、沸点为444.7℃,解释试管口为什么向上倾斜___________ 。
(3)棉花中的NaOH用于吸收反应过程中产生的二氧化硫,写出该反应的离子方程式___________ 。
(4)工业上通常用接触法制硫酸。在制硫酸的生产中,若有32吨硫黄最终全部转化为硫酸,则可以制得质量分数为98%的浓硫酸为___________ 吨。已知98%的硫酸密度为1.84g/cm3,计算此溶液的物质的量浓度为___________ mol/L。


(1)写出铁与硫反应的化学方程式
(2)已知硫的熔点为106.8℃、沸点为444.7℃,解释试管口为什么向上倾斜
(3)棉花中的NaOH用于吸收反应过程中产生的二氧化硫,写出该反应的离子方程式
(4)工业上通常用接触法制硫酸。在制硫酸的生产中,若有32吨硫黄最终全部转化为硫酸,则可以制得质量分数为98%的浓硫酸为
您最近一年使用:0次
2 . 游离态的硫存在于火山口附近或地壳的岩层中,火山喷发会释放 、
、 、
、 等气体。回答下列问题:
等气体。回答下列问题:
(1)上述气体中___________ (填化学式)是形成酸雨的主要物质。
(2) 的结构与
的结构与 类似,其电子式为
类似,其电子式为___________ 。
(3)S与Cu反应的化学方程式为___________ 。
(4) 能与
能与 反应,产物中氧化产物与还原产物的物质的量之比为
反应,产物中氧化产物与还原产物的物质的量之比为___________ 。
 、
、 、
、 等气体。回答下列问题:
等气体。回答下列问题:(1)上述气体中
(2)
 的结构与
的结构与 类似,其电子式为
类似,其电子式为(3)S与Cu反应的化学方程式为
(4)
 能与
能与 反应,产物中氧化产物与还原产物的物质的量之比为
反应,产物中氧化产物与还原产物的物质的量之比为
您最近一年使用:0次
解题方法
3 .  为阿伏加德罗常数的值。请判断下列说法的正误(正确的打“√”,错误的打“×”),简述判断依据。
为阿伏加德罗常数的值。请判断下列说法的正误(正确的打“√”,错误的打“×”),简述判断依据。
(1)标准状况下,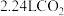 与足量的
与足量的 充分反应,转移的电子总数为
充分反应,转移的电子总数为 ,判断依据:
,判断依据:_______ 。
(2)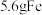 和
和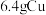 分别与
分别与 充分反应,转移的电子数均为
充分反应,转移的电子数均为 ,判断依据:
,判断依据:_______ 。
(3)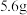 铁粉与硝酸反应失去的电子数一定为
铁粉与硝酸反应失去的电子数一定为 ,判断依据:
,判断依据:_______ 。
(4)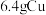 与S完全反应,转移的电子数为
与S完全反应,转移的电子数为 ,判断依据:
,判断依据:_______ 。
(5)向 溶液中通入适量
溶液中通入适量 ,当有
,当有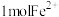 被氧化时,转移的电子总数一定等于
被氧化时,转移的电子总数一定等于 ,判断依据:
,判断依据:_______ 。
 为阿伏加德罗常数的值。请判断下列说法的正误(正确的打“√”,错误的打“×”),简述判断依据。
为阿伏加德罗常数的值。请判断下列说法的正误(正确的打“√”,错误的打“×”),简述判断依据。(1)标准状况下,
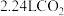 与足量的
与足量的 充分反应,转移的电子总数为
充分反应,转移的电子总数为 ,判断依据:
,判断依据:(2)
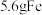 和
和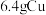 分别与
分别与 充分反应,转移的电子数均为
充分反应,转移的电子数均为 ,判断依据:
,判断依据:(3)
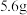 铁粉与硝酸反应失去的电子数一定为
铁粉与硝酸反应失去的电子数一定为 ,判断依据:
,判断依据:(4)
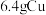 与S完全反应,转移的电子数为
与S完全反应,转移的电子数为 ,判断依据:
,判断依据:(5)向
 溶液中通入适量
溶液中通入适量 ,当有
,当有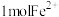 被氧化时,转移的电子总数一定等于
被氧化时,转移的电子总数一定等于 ,判断依据:
,判断依据:
您最近一年使用:0次
名校
4 . 含硫的物质与人们的生活密切相关。已知硫元素常见的化合价有-2价、0价、+4价、+6价四种,其不同价态的物质间可相互转化,完成下列填空:
(1)写出硫与铁反应的化学方程式___ 。
(2)将硫化氢气体与二氧化硫气体在集气瓶中混合发生反应,其中硫化氢呈现___ (选填“氧化性”、“还原性”)
(3)二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是___ 。
(4)将二氧化硫通入含酚酞的NaOH溶液,红色褪去,体现二氧化硫___ (性质)。
(5)硫酸盐的种类很多且应用广泛,医疗上采用___ 作X射线透视肠胃的内服药剂。
(1)写出硫与铁反应的化学方程式
(2)将硫化氢气体与二氧化硫气体在集气瓶中混合发生反应,其中硫化氢呈现
(3)二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是
(4)将二氧化硫通入含酚酞的NaOH溶液,红色褪去,体现二氧化硫
(5)硫酸盐的种类很多且应用广泛,医疗上采用
您最近一年使用:0次
5 . 含硫的物质与人们的生活密切相关。完成下列填空:
(1)硫原子的结构示意图_______ ,硫元素在周期表中的位置:第_______ 周期第_______ 族。
(2)硫化钠 Na2S 的电子式为_______ ,硫化钠中存在的化学键是_______ 键,硫化钠的水溶液呈_______ 性。(选填“酸”“中”或“碱”)
(3)硫与铁在加热条件下发生反应,生成物的化学式为_________
(4)二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是________ ;你认为减少酸雨产生的途径可采用的措施是_______
①少用煤作燃料 ②把工厂烟囱造高 ③燃料脱硫 ④在已酸化的土壤中加石灰 ⑤开发新能源
A.①②③ B.②③④⑤ C.①③⑤ D.①③④⑤
(5)工业上可用铁槽车运输浓硫酸,是由于常温下浓硫酸能使铁发生_______ 现象。
(1)硫原子的结构示意图
(2)硫化钠 Na2S 的电子式为
(3)硫与铁在加热条件下发生反应,生成物的化学式为
(4)二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是
①少用煤作燃料 ②把工厂烟囱造高 ③燃料脱硫 ④在已酸化的土壤中加石灰 ⑤开发新能源
A.①②③ B.②③④⑤ C.①③⑤ D.①③④⑤
(5)工业上可用铁槽车运输浓硫酸,是由于常温下浓硫酸能使铁发生
您最近一年使用:0次
名校
解题方法
6 . 物质的类别和核心元素的化合价是研究物质性质的两个基本视角。请根据如图所示,回答下列问题:

(1)Y是形成酸雨的主要物质之一,它溶于水反应的化学方程式为_____ ;另一类硝酸型酸雨主要由人类活动产生的NOx造成的,写出NO2与水反应的化学方程式为______ ;酸雨的pH______ (填范围)。
(2)Y能使品红溶液褪色,它与一种黄绿色气体等体积通入水中得到的溶液却几乎没有漂白性,反应的离子方程式为_______ ;Y也能使酸性高锰酸钾溶液褪色,写出该反应的离子方程式,并用单线桥法标明电子转移的方向和数目_____ ,体现了Y的_____ 性。
(3)W的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为_____ 。
(4)现用98%的浓硫酸(ρ=1.84g/cm3)配制成浓度为0.5mol/L的稀硫酸500mL,回答下列问题:
①所需浓硫酸的体积为______ mL。
②将浓硫酸沿烧杯内壁缓缓注入盛水的烧杯中,不断搅拌的目的是_____ ,若搅拌过程中有液体溅出,会导致最终所配溶液浓度_____ (填“偏大”、“偏小”或“无影响”,下同)。
③在转入容量瓶前,烧杯中的液体应先_____ ,否则会使浓度_____ 。
(5)已知S的氧化性较弱,则硫粉与铜加热反应的化学方程式为_____ 。
(6)欲制备Na2S2O3(硫代硫酸钠),从氧化还原反应角度分析,合理的是_____ (填序号)。
A.Na2S+S B.Na2SO3+S C.Na2SO3+Na2SO4 D.SO2+Na2SO4

(1)Y是形成酸雨的主要物质之一,它溶于水反应的化学方程式为
(2)Y能使品红溶液褪色,它与一种黄绿色气体等体积通入水中得到的溶液却几乎没有漂白性,反应的离子方程式为
(3)W的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为
(4)现用98%的浓硫酸(ρ=1.84g/cm3)配制成浓度为0.5mol/L的稀硫酸500mL,回答下列问题:
①所需浓硫酸的体积为
②将浓硫酸沿烧杯内壁缓缓注入盛水的烧杯中,不断搅拌的目的是
③在转入容量瓶前,烧杯中的液体应先
(5)已知S的氧化性较弱,则硫粉与铜加热反应的化学方程式为
(6)欲制备Na2S2O3(硫代硫酸钠),从氧化还原反应角度分析,合理的是
A.Na2S+S B.Na2SO3+S C.Na2SO3+Na2SO4 D.SO2+Na2SO4
您最近一年使用:0次
2020-03-23更新
|
277次组卷
|
2卷引用:重庆市育才中学2019-2020学年高一下学期3月月考化学试题
7 . 含硫的物质与人们的生活密切相关。已知硫元素常见的化合价有-2、0、+4、+6四种,其不同价态的物质间可相互转化,完成下列填空:
(1)写出硫与铁反应的化学方程式_____________________ ,所得产物的颜色为_________ 。
(2)将硫化氢气体与二氧化硫气体在集气瓶中混合发生反应,现象是___________ ,硫化氢呈现______ (选填“氧化性”、“还原性”)。
(3)二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是_________ 。
(4)硫酸盐的种类很多,且应用广泛,医疗上采用____ 作X射线透视肠胃的内服药剂。
(1)写出硫与铁反应的化学方程式
(2)将硫化氢气体与二氧化硫气体在集气瓶中混合发生反应,现象是
(3)二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是
(4)硫酸盐的种类很多,且应用广泛,医疗上采用
您最近一年使用:0次
8 . 列举一个可以说明氯和硫的非金属性强弱的事实。______________ 。
您最近一年使用:0次



