名校
1 . 利用 废气制取单质硫的常见途径有:①用
废气制取单质硫的常见途径有:①用 将部分
将部分 氧化为
氧化为 ,
, 与剩余
与剩余 反应得到硫单质,总反应为
反应得到硫单质,总反应为 ;②用
;②用 与
与 反应生成
反应生成 ,再用
,再用 溶液浸取
溶液浸取 得
得 溶液和单质硫。下列关于
溶液和单质硫。下列关于 的说法正确的是。
的说法正确的是。
 废气制取单质硫的常见途径有:①用
废气制取单质硫的常见途径有:①用 将部分
将部分 氧化为
氧化为 ,
, 与剩余
与剩余 反应得到硫单质,总反应为
反应得到硫单质,总反应为 ;②用
;②用 与
与 反应生成
反应生成 ,再用
,再用 溶液浸取
溶液浸取 得
得 溶液和单质硫。下列关于
溶液和单质硫。下列关于 的说法正确的是。
的说法正确的是。A. 与 与 反应体现了 反应体现了 的还原性 的还原性 |
B. 的稳定性比 的稳定性比 的强 的强 |
C.途径①中,每回收 硫,转移电子数为 硫,转移电子数为 |
D.途径②中每回收 硫,理论消耗 硫,理论消耗 |
您最近一年使用:0次
名校
解题方法
2 . 利用 氧化尿素制备
氧化尿素制备 (水合肼),同时可得到
(水合肼),同时可得到 的流程如下所示。
的流程如下所示。

已知: 能将
能将 氧化生成
氧化生成 ;
; 亚硫酸钠溶液的
亚硫酸钠溶液的 约为9.5。下列说法
约为9.5。下列说法不 正确的是
 氧化尿素制备
氧化尿素制备 (水合肼),同时可得到
(水合肼),同时可得到 的流程如下所示。
的流程如下所示。
已知:
 能将
能将 氧化生成
氧化生成 ;
; 亚硫酸钠溶液的
亚硫酸钠溶液的 约为9.5。下列说法
约为9.5。下列说法A.步骤Ⅰ反应时,若产物中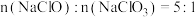 ,则 ,则 |
B.步骤Ⅱ反应的离子方程式为 |
C.步骤Ⅱ的加料方式为在搅拌下将尿素缓慢加入 碱性溶液中 碱性溶液中 |
D.步骤Ⅳ中反应过程中控制溶液为碱性,有利于吸收 |
您最近一年使用:0次
名校
解题方法
3 . 室温下,下列实验探究方案能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 向盛有淀粉-KI溶液的试管中滴加几滴溴水,振荡,观察溶液颜色变化 |  的氧化性比 的氧化性比 强 强 |
| B | 向盛有 水溶液的试管中滴加几滴酸性 水溶液的试管中滴加几滴酸性 溶液,振荡,观察溶液颜色变化 溶液,振荡,观察溶液颜色变化 |  具有漂白性 具有漂白性 |
| C | 向盛有 溶液的试管中滴加几滴新制氯水,再滴入几滴KSCN溶液,振荡,观察溶液颜色变化 溶液的试管中滴加几滴新制氯水,再滴入几滴KSCN溶液,振荡,观察溶液颜色变化 |  溶液是否变质 溶液是否变质 |
| D | 向装有溶液X的试管中滴入稀NaOH溶液,在试管口放湿润的红色石蕊试纸 | 检验溶液X中是否含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-04-25更新
|
312次组卷
|
4卷引用:江苏省常州市金坛区2022-2023学年高二下学期期中质量调研化学试题
4 . 在一定条件下,下列选项所示的物质间转化能实现的是
A.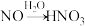 | B. |
C.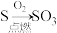 | D. |
您最近一年使用:0次
5 . 二氧化硫是一种重要的含硫化合物,在生产、生活中应用广泛。下列说法正确的是:
| A.常温下,SO2是一种无色、有刺激性气味的气体 |
| B.SO2可以使酸性高锰钾溶液红色褪去,表现出漂白性 |
| C.SO2能使品红溶液红色褪去,表现出氧化性 |
| D.SO2在红酒中添加,是利用其强氧化性 |
您最近一年使用:0次
6 . 下列说法正确的是
| A.由氨气制造碳酸氢铵属于氮的固定 |
B. 通入酸性 通入酸性 溶液,溶液紫红色褪去,说明 溶液,溶液紫红色褪去,说明 有漂白性 有漂白性 |
C.向久置的 溶液中加入足量 溶液中加入足量 溶液,出现白色沉淀;再加入足量稀盐酸,部分沉淀溶解,说明部分 溶液,出现白色沉淀;再加入足量稀盐酸,部分沉淀溶解,说明部分 被氧化 被氧化 |
D.将少量铁粉加入稀硝酸中,充分反应后滴加KSCN溶液,有气体生成且有血红色沉淀,说明稀硝酸将Fe氧化为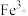 |
您最近一年使用:0次
7 . 下列实验操作和现象正确,且所得到的结论也正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 将甲烷与Cl2混合光照充分反应,向混合气体中滴入紫色石蕊试液,振荡 | 紫色石蕊试液变红后褪色 | 甲烷与Cl2反应产物中有HCl生成 |
B | 向可能含少量苯酚的苯中加入过量的浓溴水 | 未出现白色沉淀 | 苯中不含苯酚 |
C | 将溴乙烷和 NaOH的乙醇溶液混合加热,产生气体通入酸性 KMnO4溶液 | 酸性KMnO4溶液褪色 | 产生了乙烯 |
D | 向苯酚浊液中滴加Na2CO3溶液 | 溶液澄清且未生成气体 | Ka1(H2CO3)>K(C6H6O)> Ka2(H2CO3) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-04-22更新
|
335次组卷
|
3卷引用:江苏省扬州市邗江区2022-2023学年高二下学期期中调研测试化学试题
8 . 下列说法正确的是
| A.SO2具有还原性可用于漂白纸浆 |
| B.工业废气中的SO2和CO2均可采用石灰法进行脱除 |
| C.酯化反应中,浓硫酸的作用是加快反应速率同时提高反应的转化率 |
| D.浓硫酸与金属铜反应时仅表现其氧化性 |
您最近一年使用:0次
9 . 下列有关物质的性质与用途具有对应关系的是
A. 具有氧化性,可用于漂白纸浆 具有氧化性,可用于漂白纸浆 | B.CaO能与水反应,可用作食品干燥剂 |
| C.氨气易溶于水,可用作制冷剂 | D.浓硝酸具有酸性,可用于洗涤附有银镜的试管 |
您最近一年使用:0次
名校
10 . 认识含硫物质的性质及转化规律,能帮助我们更好地认识自然和保护环境。
(1)模拟酸雨的形成原因。将 气体通入蒸馏水中,取出部分溶液并用PH计测定其PH,每隔10min读数一次,所得数据如下:
气体通入蒸馏水中,取出部分溶液并用PH计测定其PH,每隔10min读数一次,所得数据如下:
随着时间的推移,pH逐渐变小的原因是___________ (用化学方程式表示)。
(2)防治 对环境的污染。
对环境的污染。
①从物质分类角度看, 属于酸性氧化物。工业上常用
属于酸性氧化物。工业上常用 将
将 转化为亚硫酸盐,写出所得亚硫酸盐的化学式:
转化为亚硫酸盐,写出所得亚硫酸盐的化学式:___________ 。
②从元素价态看, 中S元素为
中S元素为 价,既具有氧化性,又具有还原性。用生物质热解气(主要成分为CO、
价,既具有氧化性,又具有还原性。用生物质热解气(主要成分为CO、 、
、 )可将
)可将 在高温下还原成单质硫。写出CO还原
在高温下还原成单质硫。写出CO还原 反应的化学方程式:
反应的化学方程式:___________ 。
(3) 的性质:
的性质:
① 能使品红溶液褪色,该现象说明
能使品红溶液褪色,该现象说明 具有
具有___________ 性(填“氧化”、“还原”或“漂白”)。
②酸性条件下, 与
与 在发生如下反应:
在发生如下反应: ,使溶液褪色。反应中
,使溶液褪色。反应中 有
有___________ 性(填“氧化”“还原”或“漂白”)。
(4)获取空气质量信息。某化学小组为了测定空气中 的体积分数,做了如下实验:取标准状况下的空气20.00L(含
的体积分数,做了如下实验:取标准状况下的空气20.00L(含 、
、 、
、 、
、 ),缓慢通过足量氯水中,在所得溶液中加入稍过量的
),缓慢通过足量氯水中,在所得溶液中加入稍过量的 溶液,产生白色沉淀,过滤后将沉淀洗涤、干燥,称得其质量为2.33g。
溶液,产生白色沉淀,过滤后将沉淀洗涤、干燥,称得其质量为2.33g。
①将上述空气缓慢通过足量氯水,写出反应的离子方程式:___________ 。
②检验沉淀是否洗涤干净的方法是___________ 。
③求空气样品中 的体积分数
的体积分数___________ 。(写出计算过程)
(1)模拟酸雨的形成原因。将
 气体通入蒸馏水中,取出部分溶液并用PH计测定其PH,每隔10min读数一次,所得数据如下:
气体通入蒸馏水中,取出部分溶液并用PH计测定其PH,每隔10min读数一次,所得数据如下:| 时间(min) | 0 | 10 | 20 | 30 | 40 |
| PH | 4.95 | 4.94 | 4.86 | 4.85 | 4.85 |
(2)防治
 对环境的污染。
对环境的污染。①从物质分类角度看,
 属于酸性氧化物。工业上常用
属于酸性氧化物。工业上常用 将
将 转化为亚硫酸盐,写出所得亚硫酸盐的化学式:
转化为亚硫酸盐,写出所得亚硫酸盐的化学式:②从元素价态看,
 中S元素为
中S元素为 价,既具有氧化性,又具有还原性。用生物质热解气(主要成分为CO、
价,既具有氧化性,又具有还原性。用生物质热解气(主要成分为CO、 、
、 )可将
)可将 在高温下还原成单质硫。写出CO还原
在高温下还原成单质硫。写出CO还原 反应的化学方程式:
反应的化学方程式:(3)
 的性质:
的性质:①
 能使品红溶液褪色,该现象说明
能使品红溶液褪色,该现象说明 具有
具有②酸性条件下,
 与
与 在发生如下反应:
在发生如下反应: ,使溶液褪色。反应中
,使溶液褪色。反应中 有
有(4)获取空气质量信息。某化学小组为了测定空气中
 的体积分数,做了如下实验:取标准状况下的空气20.00L(含
的体积分数,做了如下实验:取标准状况下的空气20.00L(含 、
、 、
、 、
、 ),缓慢通过足量氯水中,在所得溶液中加入稍过量的
),缓慢通过足量氯水中,在所得溶液中加入稍过量的 溶液,产生白色沉淀,过滤后将沉淀洗涤、干燥,称得其质量为2.33g。
溶液,产生白色沉淀,过滤后将沉淀洗涤、干燥,称得其质量为2.33g。①将上述空气缓慢通过足量氯水,写出反应的离子方程式:
②检验沉淀是否洗涤干净的方法是
③求空气样品中
 的体积分数
的体积分数
您最近一年使用:0次
2023-04-19更新
|
331次组卷
|
2卷引用:江苏省无锡市太湖高级中学2022-2023学年高一下学期期中考试化学试题



