名校
解题方法
1 . SO2溶于水后,与水反应生成H2SO3,下列对于H2SO3的性质预测正确的是( )
| A.有氧化性,无还原性,无酸性 |
| B.有氧化性,有还原性,有酸性 |
| C.有还原性,无氧化性,无酸性 |
| D.有还原性,无氧化性,有酸性 |
您最近一年使用:0次
2020-03-12更新
|
191次组卷
|
3卷引用:广西壮族自治区崇左市扶绥县第二中学2019-2020学年高一上学期期末考试化学试题
名校
2 . 某城市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5 μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1)PM2.5分散在空气中形成的分散系________ (填“属于”或“不属于”)胶体。
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断待测试样为________ (填“酸”或“碱”)性,表示该试样酸碱性的c(H+)或c(OH-)=________ mol·L-1。
(3)煤燃烧排放的烟气含有SO2和NOx,形成酸雨,污染大气,采用NaClO2溶液在碱性条件下可对烟气进行脱硫,脱硝,效果非常好。完成下列对烟气脱硝过程的离子方程式。______  +
+______ NO+______ =______ Cl-+______  +
+______
(4)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。写出焦炭与水蒸气反应的化学方程式:__________________ 。
②洗涤含SO2的烟气。以下物质可作洗涤剂的是______ (填字母)。
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(5)汽车尾气中NOx和CO的生成及转化。
①汽车启动后,汽缸温度越高,单位时间内NO排放量越大,写出汽缸中生成NO的化学方程式:_________________________________________________________________ 。
②汽车燃油不完全燃烧时产生CO,目前,在汽车尾气系统中装置催化转化器可减少CO和NO的污染,其化学反应方程式为__________________________________________________ 。
(1)PM2.5分散在空气中形成的分散系
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ |  |  |  | Cl- |
| 浓度/mol·L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
根据表中数据判断待测试样为
(3)煤燃烧排放的烟气含有SO2和NOx,形成酸雨,污染大气,采用NaClO2溶液在碱性条件下可对烟气进行脱硫,脱硝,效果非常好。完成下列对烟气脱硝过程的离子方程式。
 +
+ +
+(4)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。写出焦炭与水蒸气反应的化学方程式:
②洗涤含SO2的烟气。以下物质可作洗涤剂的是
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(5)汽车尾气中NOx和CO的生成及转化。
①汽车启动后,汽缸温度越高,单位时间内NO排放量越大,写出汽缸中生成NO的化学方程式:
②汽车燃油不完全燃烧时产生CO,目前,在汽车尾气系统中装置催化转化器可减少CO和NO的污染,其化学反应方程式为
您最近一年使用:0次
2020-08-14更新
|
129次组卷
|
10卷引用:广西壮族自治区崇左市大新县大新中学2019-2020学年高一上学期期末考试化学试题
广西壮族自治区崇左市大新县大新中学2019-2020学年高一上学期期末考试化学试题广西来宾市忻城县高级中学2019-2020学年高一上学期期末考试化学试题天津市耀华中学2017-2018学年高一上学期期末考试化学试题鲁科版必修一2019—2020学年高一上学期期末考试模拟试题贵州省施秉县一中2019-2020学年高一上学期期末考试化学试题(已下线)4.3 防治二氧化硫对环境的污染练习(1)——《高中新教材同步备课》(苏教版 必修第一册)鲁科版(2019)高一必修第一册第3章 物质的性质与转化 总结检测黑龙江省齐齐哈尔三立高级中学2022届高三上学期开学考试化学试题山东省威海乳山市第一中学2022-2023学年高一上学期12月月考化学试题微项目 论证重污染天气“汽车限行”的合理性
解题方法
3 . 工业上制取硫酸,回收尾气中的废气常选用的试剂是
| A.氨水 | B.NaOH | C.H2SO3 | D.H2SO4 |
您最近一年使用:0次
名校
4 . 物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据图1和图2所示,回答下列问题:
(1)Y的化学式为__________________
(2)欲制备Na2S2O3,从氧化还原角度分析,合理的是______________ (填序号)。
a.Na2S +S b.Na2SO3+S c.Na2SO3+Na2SO4 d.SO2+Na2SO4
(3)将X与O2混合,可生成淡黄色固体。该反应的氧化剂与还原剂物质的量之比为_____________ 。
(4)图2为铜丝与W的浓溶液反应并验证其产物性质的实验装置。
Ⅰ.①中反应的化学方程式是_____________ 。想要立即终止①的反应,最恰当的方法是__________ 。
a.上移铜丝,使其脱离溶液 b.撤去酒精灯 c.拔去橡胶塞倒出溶液
Ⅱ.④中棉花团的作用是_________________ 。
Ⅲ.反应停止后,待装置冷却,把③取下后向其中加入氯水,观察到白色沉淀生成,写出相关反应的离子方程式_________________

图1
(1)Y的化学式为
(2)欲制备Na2S2O3,从氧化还原角度分析,合理的是
a.Na2S +S b.Na2SO3+S c.Na2SO3+Na2SO4 d.SO2+Na2SO4
(3)将X与O2混合,可生成淡黄色固体。该反应的氧化剂与还原剂物质的量之比为
(4)图2为铜丝与W的浓溶液反应并验证其产物性质的实验装置。

图2
Ⅰ.①中反应的化学方程式是
a.上移铜丝,使其脱离溶液 b.撤去酒精灯 c.拔去橡胶塞倒出溶液
Ⅱ.④中棉花团的作用是
Ⅲ.反应停止后,待装置冷却,把③取下后向其中加入氯水,观察到白色沉淀生成,写出相关反应的离子方程式
您最近一年使用:0次
2017-03-30更新
|
485次组卷
|
4卷引用:2016-2017学年广西南宁市第三中学高一下学期第一次月考化学试卷
2016-2017学年广西南宁市第三中学高一下学期第一次月考化学试卷(已下线)广西南宁市第三中学2016-2017学年高一下学期第一次月考化学试题高一必修第一册(鲁科2019)第3章 第2节 硫的转化高一必修第一册(苏教2019)专题4 第二单元 硫及其化合物的相互转化2
解题方法
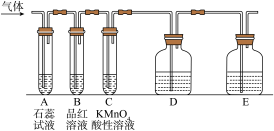
5 . 某课外小组设计了下图所示的实验装置(图中固定装置已略去),进行SO2性质的研究。
(1)从物质分类的角度,SO2属于____ (填“酸性”或“碱性”)氧化物。
①图中D装置可用来验证SO2具有该性质,其中所加入的试剂是________________ 。
②当向该装置通入SO2时,A中实验现象为_________ ,用化学用语解释其原因___________ 。
(2)从元素化合价的角度分析,SO2具有___ 性。
①当向该装置通入SO2一段时间后,可观察C中实验现象为___ ,说明SO2具有_____ 性。
②如验证SO2还具有另一方面的性质,可选择的药品是___ ,实验现象__________ 。
A.过氧化氢 B.浓硫酸C.氯水 D.硫化钠溶液
(3)B中的品红溶液现象是___________ ,证明SO2具有_________ 性。
(4)多余的SO2一般用氢氧化钠溶液吸收,反应的离子方程式_________________ 。
(1)从物质分类的角度,SO2属于
①图中D装置可用来验证SO2具有该性质,其中所加入的试剂是
②当向该装置通入SO2时,A中实验现象为
(2)从元素化合价的角度分析,SO2具有
①当向该装置通入SO2一段时间后,可观察C中实验现象为
②如验证SO2还具有另一方面的性质,可选择的药品是
A.过氧化氢 B.浓硫酸C.氯水 D.硫化钠溶液
(3)B中的品红溶液现象是
(4)多余的SO2一般用氢氧化钠溶液吸收,反应的离子方程式
您最近一年使用:0次
2020-01-17更新
|
134次组卷
|
3卷引用:广西壮族自治区崇左市大新县大新中学2019-2020学年高一上学期期末考试化学试题
14-15高一上·北京西城·期末
名校
6 . 下列关于SO2性质的说法中,不正确的是
| A.能与NaOH溶液反应 | B.能使品红溶液褪色 |
| C.能与水反应直接生成硫酸 | D.能使酸性KMnO4溶液褪色 |
您最近一年使用:0次
2016-12-09更新
|
302次组卷
|
8卷引用:广西南宁市普通高中联盟2021-2022学年高二上学期期末联考化学试题
名校
7 . 下列实验操作所对应的现象、结论均正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 向石蕊溶液中通入SO2 | 溶液褪色 | SO2具有漂白性 |
| B | 向KMnO4酸性溶液中通入乙烯 | 溶液褪色 | 乙烯能发生加成反应 |
| C | 铝片先用砂纸打磨,再加入到浓硝酸中 | 无明显现象 | 浓硝酸具有强氧化性,常温下,铝被浓硝酸钝化 |
| D | 向AgCl悬浊液中滴入NaI溶液 | 出现黄色沉淀 | Ksp(AgCl)<Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . 烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点。
(1)烟气脱硫、脱硝的环境意义是______________________ ;
(2)一种选择性催化脱硝(NO2)的原理为:6NO2+8NH3 7N2+12H2O
7N2+12H2O
① 上述反应中被还原的元素是_________ (填元素符号),反应中每转移3mol电子,生成标准状况下N2的体积为____________ ;
② 超音速飞机排放的尾气是平流层中NOx的主要来源.它们破坏臭氧层的主要机理为:
Ⅰ 、O3 O+O2 Ⅱ 、NO+O3→NO2+O2 Ⅲ 、 NO2+O→ NO+O2
O+O2 Ⅱ 、NO+O3→NO2+O2 Ⅲ 、 NO2+O→ NO+O2
上述反应中NOx所起的作用是_____________ ;
(3)下表列出了2种燃煤烟气脱硫方法的原理。
①方法Ⅰ中用氨水吸收燃煤烟气中的SO2转化为NH4HSO3,是利用了SO2的___________ 性质(选填字母编号)。
A.漂白性 B.氧化性 C.还原性 D.酸性氧化物
C.还原性 D.酸性氧化物
②方法Ⅰ中氨水吸收燃煤烟气中SO2的化学反应为:2NH3+SO2+H2O=(NH4)2SO3
(NH4)2SO3+SO2+H2O=2NH4HSO3,能提高燃煤烟气中SO2去除率的措施有______ (填字母).
A.增大氨水浓度 B.升高反应温度
C.使燃煤烟气与氨水充分接触 D.通入空气使HSO3-转化为SO42-
③采用方法Ⅰ脱硫,并不需要预先除去燃煤烟气中大量的CO2,原因是_________________ (用离子方程式表示)。
(1)烟气脱硫、脱硝的环境意义是
(2)一种选择性催化脱硝(NO2)的原理为:6NO2+8NH3
 7N2+12H2O
7N2+12H2O① 上述反应中被还原的元素是
② 超音速飞机排放的尾气是平流层中NOx的主要来源.它们破坏臭氧层的主要机理为:
Ⅰ 、O3
 O+O2 Ⅱ 、NO+O3→NO2+O2 Ⅲ 、 NO2+O→ NO+O2
O+O2 Ⅱ 、NO+O3→NO2+O2 Ⅲ 、 NO2+O→ NO+O2上述反应中NOx所起的作用是
(3)下表列出了2种燃煤烟气脱硫方法的原理。
方法Ⅰ | 用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4 |
方法Ⅱ | 用生物质热解气(主要成分CO、CH4、H2)将SO2在高温下还原成单质硫 |
①方法Ⅰ中用氨水吸收燃煤烟气中的SO2转化为NH4HSO3,是利用了SO2的
A.漂白性 B.氧化性
 C.还原性 D.酸性氧化物
C.还原性 D.酸性氧化物②方法Ⅰ中氨水吸收燃煤烟气中SO2的化学反应为:2NH3+SO2+H2O=(NH4)2SO3
(NH4)2SO3+SO2+H2O=2NH4HSO3,能提高燃煤烟气中SO2去除率的措施有
A.增大氨水浓度 B.升高反应温度
C.使燃煤烟气与氨水充分接触 D.通入空气使HSO3-转化为SO42-
③采用方法Ⅰ脱硫,并不需要预先除去燃煤烟气中大量的CO2,原因是
您最近一年使用:0次
9 . 下列组合中不可能形成喷泉的是
| A.HCl和H2O | B.O2和H2O |
| C.SO2和NaOH溶液 | D.CO2和NaOH溶液 |
您最近一年使用:0次
2017-04-15更新
|
168次组卷
|
3卷引用:广西壮族自治区上林县中学2019-2020学年高一下学期期末考试化学(理)试题
10 . 下列说法中,正确的是( )
| A.在BaC12溶液中通入SO2气体,溶液仍澄清,滴入3%过氧化氢溶液有白色沉淀 |
| B.可以用澄清石灰水来鉴别SO2与CO2 |
| C.硫在空气中的燃烧产物是二氧化硫,在纯氧中的燃烧产物是三氧化硫 |
| D.SO2能使溴水褪色,体现SO2的漂白性 |
您最近一年使用:0次
2018-01-13更新
|
228次组卷
|
2卷引用:广西陆川中学2017-2018学年高三化学上学期期末考试题



