名校
1 . 设NA为阿伏伽德罗常数的值,下列说法正确的是
| A.硅晶体中,有NA个Si就有2 NA个Si—Si键 |
| B.常温常压下,等物质的量浓度的Na2CO3与Na2S溶液中Na+数目相等 |
| C.惰性电极电解食盐水,若线路中通过2 NA个电子的电量时,则阳极产生气体22.4 L |
| D.标准状况下,2 mol Na2O2与44.8 L SO2完全反应,转移的电子数目为2 NA |
您最近一年使用:0次
2018-01-25更新
|
2425次组卷
|
5卷引用:2020届高三化学大二轮增分强化练——阿伏加德罗常数
2 . 下列哪一个实验,不仅产生气体,而且最终一定能产生白色沉淀
| A.将少量的Na投入到Ca(HCO3)2溶液中 |
| B.将过量的Na2O2投入到FeSO4溶液中 |
| C.将过量的Na投入到KAl(SO4)2溶液中 |
| D.将少量的Mg投入到NaOH溶液中 |
您最近一年使用:0次
2018-01-01更新
|
147次组卷
|
4卷引用:黄金30题系列 高一化学 小题好拿分【提升版】
(已下线)黄金30题系列 高一化学 小题好拿分【提升版】河南省中原名校(即豫南九校)2017-2018学年高一上学期第二次联考化学试题河北省定州中学2017-2018学年高二(承智班)上学期第二次月考化学试题河北省定州中学2017-2018学年高一上学期第二次月考化学试题
3 . 亚硝酸钠(NaNO3)是工业盐的主要成分,在漂白、电镀等方面应用广泛。已知: 室温下,2NO+Na2O2= =2NaNO2,以木炭、浓硝酸、Na2O2为主要原料制备亚硝酸钠的装置如图所示。(部分夹持装置已略去)下列说法正确的是
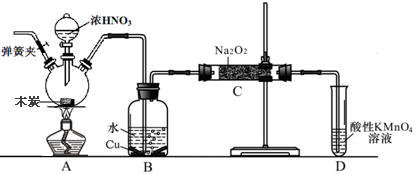

| A.实验开始前先向装置中通入N2,实验结束时先停止通入N2再熄灭酒精灯 |
| B.可以将B中药品换成NaOH 溶液 |
| C.应在B、C之间加一个盛放碱石灰的干燥管 |
| D.D装置用于尾气处理,标况下,每吸收11.2L的尾气消耗0.2mol 的高锰酸钾 |
您最近一年使用:0次
2017-12-31更新
|
362次组卷
|
3卷引用:黄金30题系列 高一化学 小题好拿分【提升版】
4 . 某溶液中含有CH3COO-、SO42-、SO32-、HCO3-、CO32-等五种离子。将过量的Na2O2固体加入其中后,仍能大量存在的离子是
| A.CH3COO-、SO42-、HCO3- | B.SO42-、SO32-、CO32- |
| C.SO32-、HCO3-、SO42- | D.CH3COO-、SO42-、CO32- |
您最近一年使用:0次
2017-12-27更新
|
130次组卷
|
3卷引用:黄金30题系列 高一化学 小题好拿分【基础版】
名校
5 . 下列叙述正确的是( )
| A.有单质参加的化合反应一定是氧化还原反应 |
| B.胶体和溶液的本质区别是丁达尔效应 |
| C.过氧化钠只具有氧化性而不具有还原性 |
| D.钝化现象是一种物理现象 |
您最近一年使用:0次
名校
6 . Na2O2具有强氧化性,H2具有还原性,某同学根据氧化还原反应的知识推测Na2O2与H2能发生反应。为了验证此推测结果,该同学设计并进行如下实验。
I.实验探究
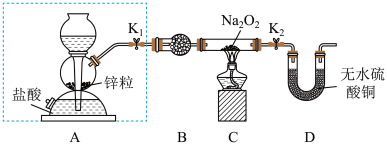
步骤1:按如图所示的装置组装仪器(图中夹持仪器已省略)并检查装置的气密性,然后装入药品。
步骤2:打开K1、K2,在产生的氢气流经装有Na2O2的硬质玻璃管的过程中,未观察到明显现象。
步骤3:进行必要的实验操作,淡黄色的粉末慢慢变成白色固体,无水硫酸铜未变蓝色。
(1)组装好仪器后,要检查装置的气密性。简述检查虚线框内装置气密性的方法:________ 。
(2)B装置中所盛放的试剂是_____ ,其作用是_______ 。
(3)步骤3中的必要操作为打开K1、K2,_______ (请按正确的顺序填入下列步骤的字母)。
A.加热至Na2O2逐渐熔化,反应一段时间
B.用小试管收集气体并检验其纯度
C.关闭K1
D.停止加热,充分冷却
(4)由上述实验可推出Na2O2与H2反应的化学方程式为__________ 。
II.数据处理
(5)实验结束后,该同学欲测定C装置硬质玻璃管内白色固体中未反应完的Na2O2含量。
其操作流程如下:

①测定过程中需要的仪器除固定、夹持仪器外,还有电子天平、烧杯、酒精灯、蒸发皿和____ 。
②在转移溶液时,若溶液转移不完全,则测得的Na2O2质量分数_____ (填“偏大”“偏小”或“不变”)
I.实验探究

步骤1:按如图所示的装置组装仪器(图中夹持仪器已省略)并检查装置的气密性,然后装入药品。
步骤2:打开K1、K2,在产生的氢气流经装有Na2O2的硬质玻璃管的过程中,未观察到明显现象。
步骤3:进行必要的实验操作,淡黄色的粉末慢慢变成白色固体,无水硫酸铜未变蓝色。
(1)组装好仪器后,要检查装置的气密性。简述检查虚线框内装置气密性的方法:
(2)B装置中所盛放的试剂是
(3)步骤3中的必要操作为打开K1、K2,
A.加热至Na2O2逐渐熔化,反应一段时间
B.用小试管收集气体并检验其纯度
C.关闭K1
D.停止加热,充分冷却
(4)由上述实验可推出Na2O2与H2反应的化学方程式为
II.数据处理
(5)实验结束后,该同学欲测定C装置硬质玻璃管内白色固体中未反应完的Na2O2含量。
其操作流程如下:

①测定过程中需要的仪器除固定、夹持仪器外,还有电子天平、烧杯、酒精灯、蒸发皿和
②在转移溶液时,若溶液转移不完全,则测得的Na2O2质量分数
您最近一年使用:0次
2017-10-30更新
|
1137次组卷
|
9卷引用:第三章 能力提升检测卷(测)——2021年高考化学一轮复习讲练测
(已下线)第三章 能力提升检测卷(测)——2021年高考化学一轮复习讲练测(已下线)第06讲 钠及其化合物(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第1讲 钠及其重要化合物江西省百所名校2018届高三第一次联合考试化学试题湖南省衡阳市第八中学2017-2018学年高一(理科实验班)上学期第一次月考理综化学试题河北省承德市各县第一中学2018届高三上学期期末考试化学试题山西省大同市2020届高三第一次联合考试(县区)化学试题河北省廊坊市2018-2019学年高二下学期期末考试化学试题甘肃省天水市第一中学2021届高三上学期第一学段考试化学试题
7 . 甲同学将Na2O2分别与H2O和浓盐酸反应,有如下现象:
请完成下列问题:
实验I中:
⑴该反应是_________ 反应(填“放热”或“吸热”)。
⑵反应的化学方程式是:_____________________________ 。
⑶证明无色无味气体是氧气的方法是:_________________________ 。
实验Ⅱ中:
⑷根据现象②、③,推测生成的气体中可能含有Cl2,产生Cl2的化学方程式是:________________ 。
⑸若往“浅黄绿色溶液”中加入FeCl3溶液,立即产生与实验I相同的气体,原因是:______________________ 。
| 实验序号 | 使用药品 | 现象 |
| Ⅰ | Na2O2、H2O | ①试管壁发热;②有无色无味气体产生 |
| Ⅱ | Na2O2、浓盐酸 | ①试管壁发热;②刺激性气味的气体产生;③反应后所得溶液呈浅黄绿色 |
请完成下列问题:
实验I中:
⑴该反应是
⑵反应的化学方程式是:
⑶证明无色无味气体是氧气的方法是:
实验Ⅱ中:
⑷根据现象②、③,推测生成的气体中可能含有Cl2,产生Cl2的化学方程式是:
⑸若往“浅黄绿色溶液”中加入FeCl3溶液,立即产生与实验I相同的气体,原因是:
您最近一年使用:0次
2017-02-17更新
|
432次组卷
|
4卷引用:2023年北京卷高考真题变式题(实验探究题)
(已下线)2023年北京卷高考真题变式题(实验探究题)2016届北京市朝阳区高三上学期期中统考化学试卷2017届广东省深圳市三校高三上学期第一次联考化学卷山西省运城市景胜中学2020-2021学年高一9月月考化学试题
8 . 甲、乙、丙为常见单质。A、B、C、D、E、F、G、H均为中学化学中常见的化合物,其中B、G的焰色反应均为黄色,C能使品红溶液褪色。在一定条件下,各物质相互转化关系如图所示。
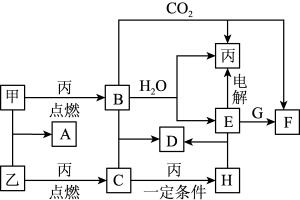
请回答下列问题:
(1)用化学式表示:丙为__________ ,H为__________ 。
(2)A的电子式为___________________________________________________ 。
(3)电解E的水溶液时,E起到的作用是_______________________________ 。
(4)写出B+C—→D的化学方程式:__________________________________ ;
写出E+G—→F的离子方程式:____________________________________ 。

请回答下列问题:
(1)用化学式表示:丙为
(2)A的电子式为
(3)电解E的水溶液时,E起到的作用是
(4)写出B+C—→D的化学方程式:
写出E+G—→F的离子方程式:
您最近一年使用:0次
2016-12-09更新
|
229次组卷
|
6卷引用:2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第5讲 无机框图题的解答策略【押题专练】
(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第5讲 无机框图题的解答策略【押题专练】(已下线)2015届福建省福州文博中学高三上学期期中考试化学试卷2016-2017学年河北省唐山一中高二上9月调研化学试卷2016-2017学年河北省唐山一中高二上学期9月调研化学试卷2016-2017学年广西钦州市钦州港区高一12月月考化学卷人教版2017-2018学年高一化学必修1:3.2 几种重要的金属化合物 同步测试2
14-15高三上·浙江绍兴·阶段练习
解题方法
9 . 比较法是化学中研究物质性质的基本方法之一,请运用比较法解答下题。Na2O2几乎可与所有的常见气态非金属氧化物反应。如
2Na2O2+2CO2=2Na2CO3+O2, Na2O2+CO = Na2CO3。
(1)试分别写出Na2O2与SO2、SO3反应的化学方程式:_________________ ;___________________ 。
(2)通过比较可知,当非金属元素处于____________ 价时,其氧化物与Na2O2反应有O2生成。
(3)依上述规律,写出Na2O2与N2O5反应的化学方程式________________________________ 。
2Na2O2+2CO2=2Na2CO3+O2, Na2O2+CO = Na2CO3。
(1)试分别写出Na2O2与SO2、SO3反应的化学方程式:
(2)通过比较可知,当非金属元素处于
(3)依上述规律,写出Na2O2与N2O5反应的化学方程式
您最近一年使用:0次
10 . 下列各组物质相互混合反应后,最终有白色沉淀生成的是
①过量Na2O2投入到FeCl2溶液中 ②过量Ba(OH)2溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中 ④Na2SiO3溶液中通入过量CO2
⑤CaCl2与NaOH的混合溶液中通入过量CO2
①过量Na2O2投入到FeCl2溶液中 ②过量Ba(OH)2溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中 ④Na2SiO3溶液中通入过量CO2
⑤CaCl2与NaOH的混合溶液中通入过量CO2
| A.全部 | B.①⑤ | C.②③④ | D.②③④⑤ |
您最近一年使用:0次
2016-12-09更新
|
378次组卷
|
3卷引用:专题3.1 钠及其重要化合物(练)——2020年高考化学一轮复习讲练测
(已下线)专题3.1 钠及其重要化合物(练)——2020年高考化学一轮复习讲练测河南省安阳市第三十五中学2016-2017学年高二下学期期末考试化学试题河南省周口市周口恒大中学2023-2024学年高一上学期1月期末化学试题



