名校
解题方法
1 . NaHCO3溶液不仅在受热时能分解放出CO2,而且在室温时亦能分解。
(1)25℃时,1.0 mol·L-1NaHCO3溶液pH随NaHCO3分解率的变化曲线如图所示。

① NaHCO3溶液分解反应的离子方程式为_______ 。
② 等物质的量浓度的Na2CO3和NaHCO3溶液相比,前者碱性_______ (填“强”或“弱”)。
③ 0.5 mol·L-1 Na2CO3溶液的pH=_______ 。
(2)利用如图所示实验装置探究NaHCO3溶液作为植物光合作用的碳源。

① 装置A、D共同的作用是_______ 。
② 一种求NaHCO3的分解率方法如下:将充分反应后C瓶中的沉淀过滤掉,滤液转入锥形瓶中,再滴入2.0 mol·L-1盐酸30 mL,恰好完全反应。则NaHCO3的分解率为_______ 。
③ 实验结果偏低的原因是_______ 。
④ 重新设计另外一种求NaHCO3分解率的方法,写出必要的实验步骤:_______ 。
(1)25℃时,1.0 mol·L-1NaHCO3溶液pH随NaHCO3分解率的变化曲线如图所示。

① NaHCO3溶液分解反应的离子方程式为
② 等物质的量浓度的Na2CO3和NaHCO3溶液相比,前者碱性
③ 0.5 mol·L-1 Na2CO3溶液的pH=
(2)利用如图所示实验装置探究NaHCO3溶液作为植物光合作用的碳源。

① 装置A、D共同的作用是
② 一种求NaHCO3的分解率方法如下:将充分反应后C瓶中的沉淀过滤掉,滤液转入锥形瓶中,再滴入2.0 mol·L-1盐酸30 mL,恰好完全反应。则NaHCO3的分解率为
③ 实验结果偏低的原因是
④ 重新设计另外一种求NaHCO3分解率的方法,写出必要的实验步骤:
您最近一年使用:0次
名校
2 . 实验是解决化学问题的基本途径,下列有关实验的叙述正确的是
| A.常温下,准确称取14.8 g Ca(OH)2,配制100 mL 2 mol·L-1的Ca(OH)2溶液 |
| B.配制750 mL 0.1 mol·L-1的Na2CO3溶液,应选用250 mL和500 mL两种容量瓶 |
| C.向滴有酚酞的水中投入金属钠,发现溶液变红,说明钠与水的反应有碱性物质生成 |
| D.某溶液中加入Na2CO3溶液产生白色沉淀,若改为加入NaHCO3溶液则一定不会有沉淀生成 |
您最近一年使用:0次
名校
3 . 下列实验方案不能达到目的是
A.用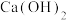 溶液鉴别 溶液鉴别 溶液和 溶液和 溶液 溶液 |
B.用丁达尔效应鉴别 胶体和 胶体和 溶液 溶液 |
C.用饱和 溶液除去 溶液除去 中混有的HCl 中混有的HCl |
D.用焰色反应鉴别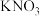 固体和NaCl固体 固体和NaCl固体 |
您最近一年使用:0次
2022-10-12更新
|
348次组卷
|
2卷引用:江苏省海安实验、句容三中、心湖高中2022-2023学年高一10月联考化学试题
解题方法
4 . 在给定条件下,下列选项所示的物质间转化均能实现的是
A.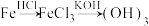 |
B. 溶液 溶液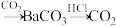 |
C.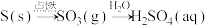 |
D.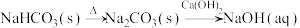 |
您最近一年使用:0次
名校
5 . 实验室有一包白色固体,可能含有 、
、 和NaCl中的一种或多种。下列根据实验事实得出的结论正确的是
和NaCl中的一种或多种。下列根据实验事实得出的结论正确的是
 、
、 和NaCl中的一种或多种。下列根据实验事实得出的结论正确的是
和NaCl中的一种或多种。下列根据实验事实得出的结论正确的是A.取一定量固体,溶解,向溶液中通入足量的CO2,观察到有晶体析出,说明原固体中一定含有 |
B.取一定量固体,溶解,向溶液中加入适量CaO粉末,充分反应后观察到有白色沉淀生成,说明原固体中一定含有 |
| C.取一定量固体,溶解,向溶液中滴加适量AgNO3溶液,观察到有白色沉淀生成,说明原固体中一定含有NaCl |
| D.称取3.80g固体,加热至恒重,质量减少了0.620g。用足量稀盐酸溶解残留固体,充分反应后,收集到0.880g气体,则原固体中还含有NaCl |
您最近一年使用:0次
名校
解题方法
6 . 侯氏制碱法以氯化钠、二氧化碳、氨和水为原料,发生反应NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。将析出的固体灼烧获取纯碱,向析出固体后的母液中加入食盐可获得副产品氯化铵。下列说法正确的是
A.CO 中C原子的轨道杂化类型为sp3 中C原子的轨道杂化类型为sp3 |
| B.相同温度下,NH4Cl在水中的溶解度大于在NaCl溶液中的溶解度 |
| C.用澄清石灰水可以鉴别Na2CO3与NaHCO3 |
| D.NaHCO3的热稳定性比Na2CO3强 |
您最近一年使用:0次
2022-09-01更新
|
616次组卷
|
6卷引用:江苏苏州市2021届高三下学期期初学业质量阳光指标调研化学试题
解题方法
7 . 分别加热Na2CO3和NaHCO3固体,观察到试管内壁均有水珠,结论:两种物质均受热分解。(_______)
您最近一年使用:0次
解题方法
8 . 溶解度:小苏打<苏打。(_______)
您最近一年使用:0次
解题方法
9 . 热稳定性Na2CO3>NaHCO3。(_______)
您最近一年使用:0次
名校
10 . Ⅰ.钠及其化合物有非常重要的用途。
(1)钠的化学性质非常活泼。画出钠原子结构示意图:_______ 。
(2)某课外活动小组为了检验钠与水反应的产物,设计如图装置(夹持装置省略)。首先在U形管内加入少量煤油和几粒钠块,再从U形管高端加入水(含有酚酞),赶出空气,过一会儿点燃酒精灯加热铜丝。

根据反应中观察到的现象,回答下列问题:
①反应过程中金属钠逐渐变小,请写出该反应的化学方程式:_______ 。
②铜丝的变化现象为_______ ,反应的化学方程式是 :_______ 。
Ⅱ.现用金属钠和空气制备纯度较高的Na2O2,可利用的装置如图。
提示:Na2O2可以与H2O、CO2反应。

(3)上述装置④中盛放的试剂是_______ ,为完成实验应将装置④接在_______ (填字母)。
A.①之前 B.①和②之间 C.②和③之间 D.③之后
(4)点燃酒精灯后,装置②中Na生成Na2O2的化学方程式为_______ 。
(5)若缺少装置④,则产生的Na2O2会和水反应,反应的化学方程式为_______ 。
III.为探究Na2CO3和NaHCO3的热稳定性,某同学设计了如图实验:

(6)加热一段时间后,_______ (填“A”或“B”)中澄清石灰水变浑浊,写出试管中发生反应的化学方程式:_______ 。
(1)钠的化学性质非常活泼。画出钠原子结构示意图:
(2)某课外活动小组为了检验钠与水反应的产物,设计如图装置(夹持装置省略)。首先在U形管内加入少量煤油和几粒钠块,再从U形管高端加入水(含有酚酞),赶出空气,过一会儿点燃酒精灯加热铜丝。

根据反应中观察到的现象,回答下列问题:
①反应过程中金属钠逐渐变小,请写出该反应的化学方程式:
②铜丝的变化现象为
Ⅱ.现用金属钠和空气制备纯度较高的Na2O2,可利用的装置如图。
提示:Na2O2可以与H2O、CO2反应。

(3)上述装置④中盛放的试剂是
A.①之前 B.①和②之间 C.②和③之间 D.③之后
(4)点燃酒精灯后,装置②中Na生成Na2O2的化学方程式为
(5)若缺少装置④,则产生的Na2O2会和水反应,反应的化学方程式为
III.为探究Na2CO3和NaHCO3的热稳定性,某同学设计了如图实验:

(6)加热一段时间后,
您最近一年使用:0次



