解题方法
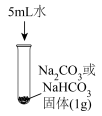
1 . Ⅰ.某小组同学探究Na2CO3的性质。
(1)用Na2CO3固体配制100 mL 0.200 mol·L-1Na2CO3溶液。
①用到的仪器有:天平、药匙、量筒、烧杯、玻璃棒、胶头滴管和___________ 。
②计算需要Na2CO3固体的质量是___________ g。
③下列情况中,会使所配溶液浓度偏高的是___________ (填字母)。
a.转移时,没有洗涤烧杯和玻璃棒
b.定容时,眼睛俯视刻度线
c.摇匀后,发现液面低于刻度线,继续加水至液面与刻度线相切
(2)探究Na2CO3与盐酸的反应。向0.200 mol·L-1Na2CO3溶液中滴加稀盐酸,开始无气泡,继续滴加,产生气泡,反应的离子方程式为: +H+=
+H+= 、
、___________ 。
Ⅱ.某化学兴趣小组设计如下实验探究KMnO4固体与草酸(H2C2O4,具有还原性)反应的产物,以其产物为原料制备氯气:
室温下,取KMnO4固体于锥形瓶中,加入适量的草酸(H2C2O4)溶液,振荡,充分反应,可以观察到有黑色沉淀产生,溶液变为无色,同时生成无色无味的气体M,将燃着的木条靠近锥形瓶瓶口时木条熄灭。
分析实验并回答相应问题。
(3)M的化学式是___________ 。
(4)将充分反应后的混合物过滤,检验滤液中金属阳离子的方法及现象为___________ 、___________ 。向滤液中加入盐酸时又产生无色无味气体。
(5)将滤渣加入浓盐酸中加热,产生黄绿色气体,该反应的离子方程式为___________ 。
(1)用Na2CO3固体配制100 mL 0.200 mol·L-1Na2CO3溶液。
①用到的仪器有:天平、药匙、量筒、烧杯、玻璃棒、胶头滴管和
②计算需要Na2CO3固体的质量是
③下列情况中,会使所配溶液浓度偏高的是
a.转移时,没有洗涤烧杯和玻璃棒
b.定容时,眼睛俯视刻度线
c.摇匀后,发现液面低于刻度线,继续加水至液面与刻度线相切
(2)探究Na2CO3与盐酸的反应。向0.200 mol·L-1Na2CO3溶液中滴加稀盐酸,开始无气泡,继续滴加,产生气泡,反应的离子方程式为:
 +H+=
+H+= 、
、Ⅱ.某化学兴趣小组设计如下实验探究KMnO4固体与草酸(H2C2O4,具有还原性)反应的产物,以其产物为原料制备氯气:
室温下,取KMnO4固体于锥形瓶中,加入适量的草酸(H2C2O4)溶液,振荡,充分反应,可以观察到有黑色沉淀产生,溶液变为无色,同时生成无色无味的气体M,将燃着的木条靠近锥形瓶瓶口时木条熄灭。
分析实验并回答相应问题。
(3)M的化学式是
(4)将充分反应后的混合物过滤,检验滤液中金属阳离子的方法及现象为
(5)将滤渣加入浓盐酸中加热,产生黄绿色气体,该反应的离子方程式为
您最近一年使用:0次
解题方法
2 . 探究 和
和 的性质,进行如下实验。
的性质,进行如下实验。
(1)实验Ⅰ, 固体完全溶解,
固体完全溶解, 固体有剩余。相同条件下,在水中的溶解能力:
固体有剩余。相同条件下,在水中的溶解能力:
_______  (填“>”或“<”)。
(填“>”或“<”)。
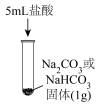
(2)实验Ⅱ,观察到均有气体产生,该气体是_______ 。
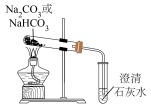
(3)实验Ⅲ,加热 固体,澄清石灰水中无明显变化;加热
固体,澄清石灰水中无明显变化;加热 固体,澄清石灰水变浑浊,写出
固体,澄清石灰水变浑浊,写出 受热分解的化学方程式:
受热分解的化学方程式:_______ 。
(4)下列说法中,正确的是_______ (填字母)。
a.可用盐酸除去 固体中少量的
固体中少量的
b.可用加热的方法鉴别 和
和 两种固体
两种固体
 和
和 的性质,进行如下实验。
的性质,进行如下实验。实验序号 | Ⅰ | Ⅱ | Ⅲ |
实验装置 |
|
|
|
(1)实验Ⅰ,
 固体完全溶解,
固体完全溶解, 固体有剩余。相同条件下,在水中的溶解能力:
固体有剩余。相同条件下,在水中的溶解能力:
 (填“>”或“<”)。
(填“>”或“<”)。(2)实验Ⅱ,观察到均有气体产生,该气体是
(3)实验Ⅲ,加热
 固体,澄清石灰水中无明显变化;加热
固体,澄清石灰水中无明显变化;加热 固体,澄清石灰水变浑浊,写出
固体,澄清石灰水变浑浊,写出 受热分解的化学方程式:
受热分解的化学方程式:(4)下列说法中,正确的是
a.可用盐酸除去
 固体中少量的
固体中少量的
b.可用加热的方法鉴别
 和
和 两种固体
两种固体
您最近一年使用:0次
3 . 某化学兴趣小组模拟侯氏制碱法制取Na2CO3产品并回收NH4Cl,设计如下实验方案。
Ⅰ.NaHCO3的制备,实验装置如图甲:
②向反应器中通入CO2气体,待溶液变为无色后,再加入10mL浓氨水,继续通入CO2.
③再加入10mL浓氨水,充分振荡,使NaCl完全溶解,继续通入过量CO2至生成大量NaHCO3晶体。
④将反应器冷却,然后抽滤,回收母液。用无水乙醇洗涤沉淀,收集NaHCO3晶体。
Ⅱ.Na2CO3的制备
将制得的NaHCO3晶体转移到已称量的蒸发皿中,加热至质量不再改变,停止加热,冷却到室温并称量。
Ⅲ.NH4Cl的回收
加热母液使NH4HCO3分解,滴加氨水至溶液呈碱性,操作b,抽滤,洗涤,置于干燥器中干燥,称重。
(1)仪器a的名称是_____ 。
(2)步骤③中通入过量CO2生成NaHCO3晶体的离子方程式为_____ 。
(3)已知0℃时NaHCO3的溶解度是0.8mol·L-1,不考虑溶液混合时体积的变化及对NaHCO3溶解度的影响,若10.0gNaCl全部转化成NaHCO3,则在0℃时从溶液中能析出NaHCO3固体_____ g(保留1位小数)。
(4)已知碳酸氢钠分解反应的ΔH=+135.6kJ·mol-1·K-1、ΔS=+333.3J·mol-1·K-1。在下列哪些温度下该反应能自发进行_____(填标号)。
(5)①回收NH4Cl时加入氨水的目的是_____ 。
②结合图乙,简单说明操作b的过程_____ 。
(6)若制得的NaHCO3中含有未反应的NaCl,则分解后所得固体的质量_____ (填“大于”、“小于”或“等于”)理论上生成Na2CO3的质量。
Ⅰ.NaHCO3的制备,实验装置如图甲:

②向反应器中通入CO2气体,待溶液变为无色后,再加入10mL浓氨水,继续通入CO2.
③再加入10mL浓氨水,充分振荡,使NaCl完全溶解,继续通入过量CO2至生成大量NaHCO3晶体。
④将反应器冷却,然后抽滤,回收母液。用无水乙醇洗涤沉淀,收集NaHCO3晶体。
Ⅱ.Na2CO3的制备
将制得的NaHCO3晶体转移到已称量的蒸发皿中,加热至质量不再改变,停止加热,冷却到室温并称量。
Ⅲ.NH4Cl的回收
加热母液使NH4HCO3分解,滴加氨水至溶液呈碱性,操作b,抽滤,洗涤,置于干燥器中干燥,称重。
(1)仪器a的名称是
(2)步骤③中通入过量CO2生成NaHCO3晶体的离子方程式为
(3)已知0℃时NaHCO3的溶解度是0.8mol·L-1,不考虑溶液混合时体积的变化及对NaHCO3溶解度的影响,若10.0gNaCl全部转化成NaHCO3,则在0℃时从溶液中能析出NaHCO3固体
(4)已知碳酸氢钠分解反应的ΔH=+135.6kJ·mol-1·K-1、ΔS=+333.3J·mol-1·K-1。在下列哪些温度下该反应能自发进行_____(填标号)。
| A.308K | B.373K | C.421K | D.573K |
(5)①回收NH4Cl时加入氨水的目的是
②结合图乙,简单说明操作b的过程
(6)若制得的NaHCO3中含有未反应的NaCl,则分解后所得固体的质量
您最近一年使用:0次
名校
解题方法
4 . 碳酸钠和碳酸氢钠在日常生产生活中有着广泛应用。用如图装置探究二者的稳定性。 和
和 位置互换?
位置互换?_______ (填“能”或“不能”)。能证明 的热稳定性强于
的热稳定性强于 的实验现象是:
的实验现象是:_______
(2)除了热稳定性外,请你再设计一个实验用于鉴别 和
和 :
:_______ 。

 和
和 位置互换?
位置互换? 的热稳定性强于
的热稳定性强于 的实验现象是:
的实验现象是:(2)除了热稳定性外,请你再设计一个实验用于鉴别
 和
和 :
:
您最近一年使用:0次
5 . 某小组同学利用pH传感器对碳酸氢钠、碳酸钠的某些性质进行以下探究。
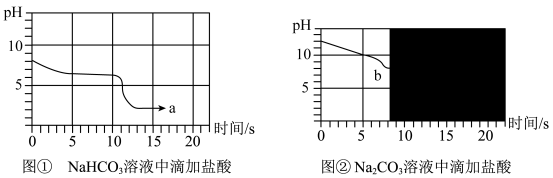
25℃时,向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入相同浓度的盐酸,用pH传感器测得pH变化与时间的关系如图①、图②所示。将图①与图②的阴影部分进行叠加,发现两者基本重合。
回答下列问题:
(1)含等碳原子数的碳酸氢钠和碳酸钠溶液均呈碱性,两种溶液碱性较强的是___________ 。
(2)a点的溶质为___________ ,b点前发生反应的化学方程式为___________ 。
(3)依据实验获取的信息,请将鉴别 和
和 固体的实验方案补充完整:分别取两种固体加入适量水溶解,逐滴缓缓加入稀盐酸,
固体的实验方案补充完整:分别取两种固体加入适量水溶解,逐滴缓缓加入稀盐酸,___________ 。

25℃时,向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入相同浓度的盐酸,用pH传感器测得pH变化与时间的关系如图①、图②所示。将图①与图②的阴影部分进行叠加,发现两者基本重合。
回答下列问题:
(1)含等碳原子数的碳酸氢钠和碳酸钠溶液均呈碱性,两种溶液碱性较强的是
(2)a点的溶质为
(3)依据实验获取的信息,请将鉴别
 和
和 固体的实验方案补充完整:分别取两种固体加入适量水溶解,逐滴缓缓加入稀盐酸,
固体的实验方案补充完整:分别取两种固体加入适量水溶解,逐滴缓缓加入稀盐酸,
您最近一年使用:0次
6 . 碳酸钠和碳酸氢钠在日常生产生活中有着广泛应用。用下图装置探究二者的稳定性。
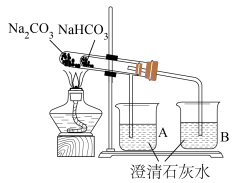
(1)该实验装置中,能否将 和
和 的位置互换?
的位置互换?_______ (填“能”或“不能”)。能证明 的热稳定性强于
的热稳定性强于 的实验现象是
的实验现象是_______ 。
(2)写出 ,受热分解的化学反应方程式
,受热分解的化学反应方程式_______ 。
(3)除了热稳定性外,请你再设计一个实验用于鉴别 和
和
_______ 。

(1)该实验装置中,能否将
 和
和 的位置互换?
的位置互换? 的热稳定性强于
的热稳定性强于 的实验现象是
的实验现象是(2)写出
 ,受热分解的化学反应方程式
,受热分解的化学反应方程式(3)除了热稳定性外,请你再设计一个实验用于鉴别
 和
和
您最近一年使用:0次
名校
7 . 某小组探究Na2CO3和NaHCO3的性质。
(1)探究溶解性。在两支试管中,分别加入约1gNa2CO3和NaHCO3固体,分别加入5mL水,充分振荡后,一支试管中固体有剩余,剩余的固体是
(2)探究稳定性。按照如图所示装置进行实验(部分夹持装置已略去)。
①能够证明Na2CO3的热稳定性强于NaHCO3的证据是
②NaHCO3受热分解的化学方程式是
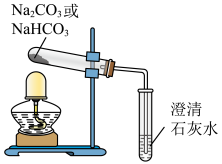
(3)探究与酸的反应。
实验步骤 | 实现现象 | 用离子方程式解释现象 |
向盛有Na2CO3溶液的试管中滴加稀盐酸 | 开始无气泡产生,一段时间后产生气泡 | ① |
向盛有NaHCO3溶液的试管中滴加稀盐酸 | 立即产生气泡 | ② |
您最近一年使用:0次
名校
8 . 钠的一系列化合物在生活与生产中有非常重要的作用,某学习小组开展了相关研究活动:
(1)甲同学欲配制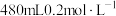 的
的 溶液,需要使用的玻璃仪器有
溶液,需要使用的玻璃仪器有____________ 、烧杯和胶头滴管;下列操作会使所配溶液浓度偏小的是______ 。
a.用托盘天平称量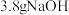 固体进行配制溶液
固体进行配制溶液
b.定容时俯视刻度线
c.未待溶解的 浓溶液冷却即转移至相应容器进行后继操作
浓溶液冷却即转移至相应容器进行后继操作
d.定容摇匀后发现液面低于刻度线,再次加入蒸馏水至刻度线
(2)乙同学欲比较 固体和
固体和 固体的热稳定性,设计实验装置如下图:
固体的热稳定性,设计实验装置如下图:
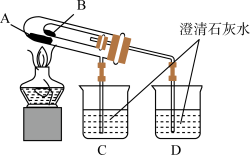
① 烧杯中的现象是
烧杯中的现象是____________
② 处应放置的药品是
处应放置的药品是____________
③热稳定性:
______  (大于、小于)
(大于、小于)
(3)丙同学为探究 的强氧化性,某设计了下图实验装置。
的强氧化性,某设计了下图实验装置。
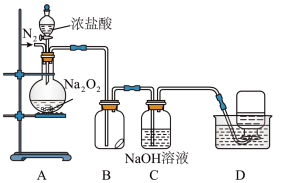
实验步骤及现象如下:
Ⅰ.检查装置气密性后,装入药品并连接仪器。
Ⅱ.缓慢通入一定量的 后,封闭
后,封闭 气体通路,将装置
气体通路,将装置 连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,
连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸, 中剧烈反应,有黄绿色气体产生。
中剧烈反应,有黄绿色气体产生。
Ⅱ.待产生连续气泡后,将装置 中的导管末端伸入集气瓶中,收集到无色气体。
中的导管末端伸入集气瓶中,收集到无色气体。
①. 中气体能使带火星的木条复燃,丙同学分析该气体不可能由
中气体能使带火星的木条复燃,丙同学分析该气体不可能由 还原
还原 所得,从氧化还原角度说明理由:
所得,从氧化还原角度说明理由:______ 。
②.资料显示, 也能与干燥
也能与干燥 反应产生
反应产生 ,写出反应的化学方程式
,写出反应的化学方程式______
(1)甲同学欲配制
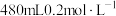 的
的 溶液,需要使用的玻璃仪器有
溶液,需要使用的玻璃仪器有a.用托盘天平称量
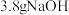 固体进行配制溶液
固体进行配制溶液b.定容时俯视刻度线
c.未待溶解的
 浓溶液冷却即转移至相应容器进行后继操作
浓溶液冷却即转移至相应容器进行后继操作d.定容摇匀后发现液面低于刻度线,再次加入蒸馏水至刻度线
(2)乙同学欲比较
 固体和
固体和 固体的热稳定性,设计实验装置如下图:
固体的热稳定性,设计实验装置如下图:
①
 烧杯中的现象是
烧杯中的现象是②
 处应放置的药品是
处应放置的药品是③热稳定性:

 (大于、小于)
(大于、小于)(3)丙同学为探究
 的强氧化性,某设计了下图实验装置。
的强氧化性,某设计了下图实验装置。
实验步骤及现象如下:
Ⅰ.检查装置气密性后,装入药品并连接仪器。
Ⅱ.缓慢通入一定量的
 后,封闭
后,封闭 气体通路,将装置
气体通路,将装置 连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,
连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸, 中剧烈反应,有黄绿色气体产生。
中剧烈反应,有黄绿色气体产生。Ⅱ.待产生连续气泡后,将装置
 中的导管末端伸入集气瓶中,收集到无色气体。
中的导管末端伸入集气瓶中,收集到无色气体。①.
 中气体能使带火星的木条复燃,丙同学分析该气体不可能由
中气体能使带火星的木条复燃,丙同学分析该气体不可能由 还原
还原 所得,从氧化还原角度说明理由:
所得,从氧化还原角度说明理由:②.资料显示,
 也能与干燥
也能与干燥 反应产生
反应产生 ,写出反应的化学方程式
,写出反应的化学方程式
您最近一年使用:0次
名校
解题方法
9 . Na2CO3和NaHCO3是两种重要的化工原料,二者的性质存在差异,为进一步探究其性质,请根据某实验小组的实验探究回答有关问题。
(1)分别将1.0g Na2CO3和NaHCO3的固体加入50mL盛有10mL蒸馏水的烧杯中,测定烧杯中溶液的温度变化如图所示。则曲线②代表的物质是(填化学式)______ 。
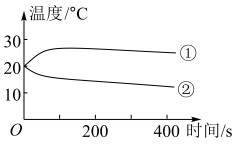
(2)如下图所示,分别向盛有10mL澄清石灰水的烧杯中加入蒸馏水和等浓度的Na2CO3、NaHCO3溶液,利用传感器测得溶液pH与加入试剂体积的变化曲线如下图所示。滴加Na2CO3溶液的烧杯中OH-未参与该反应的实验证据是___________ ;滴加NaHCO3溶液的烧杯中开始时发生反应的离子方程式为:___________ 。(提示:溶液pH越小,OH-的浓度越小,溶液碱性越弱。)

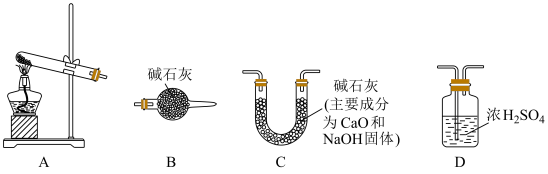
(3)某NaHCO3固体样品中含有Na2CO3杂质,某小组拟通过下列装置(气密性良好)测定CO2的质量来计算样品中NaHCO3的含量,装置的连接顺序为___→___→___→ B (每个装置仅使用一次),_____ 。经分析,上述方案存在缺陷(假定固体充分反应),会导致测定结果偏小,原因可能为:________ 。利用改进装置进行实验,ag样品加热至恒重后,称量所得固体质量为bg,则样品中NaHCO3质量分数为____ %(用含a、b的代数式表示)。
(1)分别将1.0g Na2CO3和NaHCO3的固体加入50mL盛有10mL蒸馏水的烧杯中,测定烧杯中溶液的温度变化如图所示。则曲线②代表的物质是(填化学式)

(2)如下图所示,分别向盛有10mL澄清石灰水的烧杯中加入蒸馏水和等浓度的Na2CO3、NaHCO3溶液,利用传感器测得溶液pH与加入试剂体积的变化曲线如下图所示。滴加Na2CO3溶液的烧杯中OH-未参与该反应的实验证据是

(3)某NaHCO3固体样品中含有Na2CO3杂质,某小组拟通过下列装置(气密性良好)测定CO2的质量来计算样品中NaHCO3的含量,装置的连接顺序为___→___→___→ B (每个装置仅使用一次),

您最近一年使用:0次
解题方法
10 . 课外兴趣小组的同学探究Na2CO3和NaHCO3的性质,并测定混合物中NaHCO3的含量。
实验一:Na2CO3和NaHCO3溶解性与碱性的比较
(1)室温下,Na2CO3的溶解度大于NaHCO3的实验证据是_____________ 。
(2)该实验_____________ (填“能”或“不能”)说明Na2CO3溶液的碱性强于NaHCO3溶液,理由是_____________ 。
实验二:Na2CO3和NaHCO3与澄清石灰水反应的比较
查阅资料:可以用pH表示溶液酸碱性的强弱。常温下,pH<7,溶液为酸性;pH=7,溶液为中性;pH>7,溶液为碱性。pH越小,c(OH-)越小,溶液碱性越弱。
(3)上述实验中,向澄清石灰水中滴加Na2CO3溶液,OH-未参与该反应的实验证据是_____________ 。
(4)滴加NaHCO3溶液的pH变化与滴加Na2CO3溶液的有明显差异,结合离子方程式说明原因:_____________ 。
实验三:Na2CO3和NaHCO3混合物(不考虑其他杂质)中NaHCO3质量分数的测定
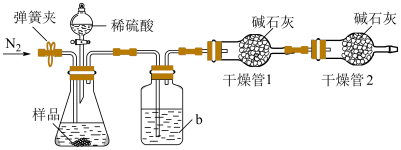
实验装置如图所示。称取19.0g待测样品于锥形瓶中,反应前先打开弹簧夹,通入一段时间的N2,然后关闭弹簧夹,接上总质量为200.0g的干燥管1,再接上干燥管2,打开分液漏斗的活塞,滴加稀硫酸进行反应。待锥形瓶中不再有气泡产生,关闭分液漏斗的活塞,打开弹簧夹,再通入一段时间的N2,最后取下干燥管1,称得其质量为208.8g。
(5)①洗气瓶中盛放的液体是_________________ (填名称)。
②第一次通入N2的目的是_________________ 。第二次通入N2的目的是_________________ 。如果没有进行第一次通N2的操作,测量的结果将会_________________ (填“偏大”“偏小”或“不变”)。
③计算出混合物中NaHCO3的质量分数为_________________ %(保留1位小数)。
实验一:Na2CO3和NaHCO3溶解性与碱性的比较
| 序号 | 实验操作 | 实验现象 | |
| ① | 在两支试管中分别加入1gNa2CO3、NaHCO3,再加入5mL水,充分振荡;用温度计测量两试管中溶液温度的变化 | Na2CO3 | NaHCO3 |
| 温度由17.6℃变为23.2℃;放置到室温时,试管内无固体 | 温度由17.6℃变为17.2℃;放置到室温时,试管内有少量固体残留 | ||
| ② | 室温时,分别向①所得溶液中滴入2滴酚酞溶液 | 溶液变红 | 溶液变微红 |
(1)室温下,Na2CO3的溶解度大于NaHCO3的实验证据是
(2)该实验
实验二:Na2CO3和NaHCO3与澄清石灰水反应的比较
查阅资料:可以用pH表示溶液酸碱性的强弱。常温下,pH<7,溶液为酸性;pH=7,溶液为中性;pH>7,溶液为碱性。pH越小,c(OH-)越小,溶液碱性越弱。
| 实验操作 | 实验数据 |
测量如下实验过程的pH变化 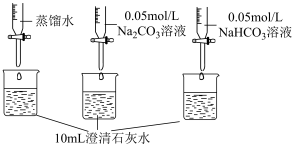 | 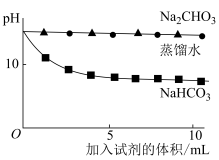 |
(3)上述实验中,向澄清石灰水中滴加Na2CO3溶液,OH-未参与该反应的实验证据是
(4)滴加NaHCO3溶液的pH变化与滴加Na2CO3溶液的有明显差异,结合离子方程式说明原因:
实验三:Na2CO3和NaHCO3混合物(不考虑其他杂质)中NaHCO3质量分数的测定

实验装置如图所示。称取19.0g待测样品于锥形瓶中,反应前先打开弹簧夹,通入一段时间的N2,然后关闭弹簧夹,接上总质量为200.0g的干燥管1,再接上干燥管2,打开分液漏斗的活塞,滴加稀硫酸进行反应。待锥形瓶中不再有气泡产生,关闭分液漏斗的活塞,打开弹簧夹,再通入一段时间的N2,最后取下干燥管1,称得其质量为208.8g。
(5)①洗气瓶中盛放的液体是
②第一次通入N2的目的是
③计算出混合物中NaHCO3的质量分数为
您最近一年使用:0次