解题方法
1 . 钠及其化合物在认识物质转化规律以及生产生活中均有重要应用。
Ⅰ.钠与水的反应
(1)写出钠与水反应的化学方程式________ 。
(2)若反应中生成H2的体积为1.12L(标准状况下),则参与反应的金属Na的质量是__________ 。
(3)同物质类别的金属Mg也能与水发生反应,试着调用反应规律分析Na和Mg分别与水反应的剧烈程度:Na________ Mg(填“>”“<"或“=”)。
Ⅱ.钠与氧气的反应
(4)钠与氧气反应的产物有多种可能,造成产物多样的原因是__________ 。
(5)其中产物_______ (填化学式)可用作潜水艇和呼吸面具中的供氧剂,写出其与CO2反应的化学方程式__________ 。
Ⅲ.碳酸钠、碳酸氢钠在食品加工方面有着广泛的用途。
(6)下列关于Na2CO3的认识正确的是_________ 。
a.受热易分解 b.俗称纯碱、苏打 c.属于碱 d.可与酸反应
(7)传统蒸馒头常采用酵头发面,酵头可使面团在微生物作用下产生CO2气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸,需要额外添加“碱面"将酸去除。等质量的Na2CO3和NaHCO3,因_____ (填“Na2CO3”或*NaHCO3")消耗酸更多,更适合作为中和发酵带来的酸味的“碱面”。
(8)若面团发得不好,面团内的气孔少,不够膨松,需添加______ (填“Na2CO3"或“NaHCO3"),继续揉面,上锅蒸后也能蒸出松软的馒头,用化学方程式表示其产气原理_____________ 。
Ⅰ.钠与水的反应
(1)写出钠与水反应的化学方程式
(2)若反应中生成H2的体积为1.12L(标准状况下),则参与反应的金属Na的质量是
(3)同物质类别的金属Mg也能与水发生反应,试着调用反应规律分析Na和Mg分别与水反应的剧烈程度:Na
Ⅱ.钠与氧气的反应
(4)钠与氧气反应的产物有多种可能,造成产物多样的原因是
(5)其中产物
Ⅲ.碳酸钠、碳酸氢钠在食品加工方面有着广泛的用途。
(6)下列关于Na2CO3的认识正确的是
a.受热易分解 b.俗称纯碱、苏打 c.属于碱 d.可与酸反应
(7)传统蒸馒头常采用酵头发面,酵头可使面团在微生物作用下产生CO2气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸,需要额外添加“碱面"将酸去除。等质量的Na2CO3和NaHCO3,因
(8)若面团发得不好,面团内的气孔少,不够膨松,需添加
您最近一年使用:0次
名校
解题方法
2 . 下列关于碳酸钠和碳酸氢钠的叙述正确的是
| A.相同条件下,在水中的溶解性:碳酸钠<碳酸氢钠 |
| B.相同条件下,溶液的碱性:碳酸钠>碳酸氢钠 |
| C.相同条件下,与酸反应产生二氧化碳气体的速率:碳酸钠>碳酸氢钠 |
| D.碳酸钠溶液和碳酸氢钠溶液可以用澄清石灰水来区别 |
您最近一年使用:0次
解题方法
3 . I.某校化学课外小组为了鉴别Na2CO3和NaHCO3两种白色固体,用不同的方法做了以下实验,如图所示:
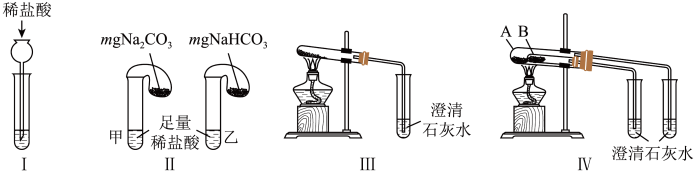
(1)方法Ⅰ,为鉴别Na2CO3和NaHCO3两种白色固体,分别取样配成溶液,再逐滴加入稀盐酸。若将稀盐酸改为Ba(OH)2溶液_______ (填“能”或“不能”)鉴别。
(2)方法Ⅱ,若固体质量相同且稀盐酸足量时,气球鼓起较小的是_______ (填“甲”或“乙”)试管。
(3)方法Ⅲ、Ⅳ均能鉴别这两种物质,加热试管发生反应的化学方程式为________ 。方法Ⅳ中NaHCO3应放在________ (填“A”或“B”)试管中。
Ⅱ.某同学欲配制450mL0.2mol/LNaOH溶液,试回答下列问题:
(4)需要称取NaOH固体的质量为_______ 。
(5)配制过程中若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)?没有洗涤烧杯和玻璃棒_______ ;加蒸馏水时不慎超过了刻度线然后用胶头滴管吸掉多余的溶液至刻度线_______ ;定容时俯视刻度线_______ 。

(1)方法Ⅰ,为鉴别Na2CO3和NaHCO3两种白色固体,分别取样配成溶液,再逐滴加入稀盐酸。若将稀盐酸改为Ba(OH)2溶液
(2)方法Ⅱ,若固体质量相同且稀盐酸足量时,气球鼓起较小的是
(3)方法Ⅲ、Ⅳ均能鉴别这两种物质,加热试管发生反应的化学方程式为
Ⅱ.某同学欲配制450mL0.2mol/LNaOH溶液,试回答下列问题:
(4)需要称取NaOH固体的质量为
(5)配制过程中若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)?没有洗涤烧杯和玻璃棒
您最近一年使用:0次
解题方法
4 . 侯氏制碱法又称联合制碱法,是我国化学工程专家侯德榜于1943年创立的。实验室模拟侯氏制碱法的工艺流程如图所示。下列说法错误的是


A.由 固体制备纯碱的操作在坩埚中进行 固体制备纯碱的操作在坩埚中进行 |
B.该反应利用了 溶解度小的特点 溶解度小的特点 |
C.向饱和食盐水中先通入 后通入氨气 后通入氨气 |
D.检验 固体中是否混有 固体中是否混有 可用稀硝酸、 可用稀硝酸、 溶液 溶液 |
您最近一年使用:0次
解题方法
5 . 小苏打和苏打分别和等浓度的盐酸反应,下列说法正确的是
| A.苏打与盐酸的反应比较剧烈 |
| B.等物质的量的小苏打和苏打分别与盐酸完全反应,产生的CO2质量相等 |
| C.实验室制取CO2通常用苏打和盐酸反应 |
| D.等物质的量的小苏打和苏打分别与盐酸完全反应,消耗的盐酸一样多 |
您最近一年使用:0次
6 . 我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献。
I.如图为联合制碱法的主要过程(部分物质已略去):
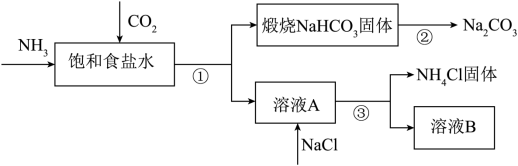
(1)①~③的涉及的操作方法中,包含过滤的是___________ (填序号)。
(2)煅烧NaHCO3固体的化学方程式是___________ 。
(3)上述联合制碱法流程可以循环使用的中一种物质是___________ (填化学式)。
II.某小组利用下列装置对Na2CO3和NaHCO3的性质进行探究,(夹持装置已略去,气密性已检查)。
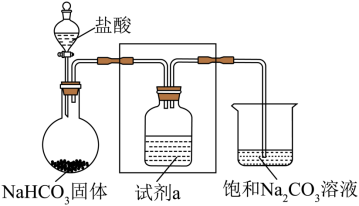
(4)方框中为洗气装置,请将该装置图补充完整___________ 。
(5)试剂a为饱和NaHCO3溶液,其作用是___________ 。
(6)实验持续-段时间后,观察到饱和Na2CO3溶液中有细小晶体析出,用化学方程式表示产生细小晶体的原因___________ 。
(7)下列选项中哪种物质可以鉴别浓度相同的 和
和 ___________。
___________。
I.如图为联合制碱法的主要过程(部分物质已略去):

(1)①~③的涉及的操作方法中,包含过滤的是
(2)煅烧NaHCO3固体的化学方程式是
(3)上述联合制碱法流程可以循环使用的中一种物质是
II.某小组利用下列装置对Na2CO3和NaHCO3的性质进行探究,(夹持装置已略去,气密性已检查)。

(4)方框中为洗气装置,请将该装置图补充完整
(5)试剂a为饱和NaHCO3溶液,其作用是
(6)实验持续-段时间后,观察到饱和Na2CO3溶液中有细小晶体析出,用化学方程式表示产生细小晶体的原因
(7)下列选项中哪种物质可以鉴别浓度相同的
 和
和 ___________。
___________。| A.澄清石灰水 | B.氢氧化钠溶液 | C.稀盐酸 | D. 溶液 溶液 |
您最近一年使用:0次
解题方法
7 . 下列有关说法正确的是
| A.为了除去Na2CO3溶液中的NaHCO3,可滴加适量的稀盐酸 |
| B.为了除去NaHCO3固体中的Na2CO3,可通过加热除去 |
C.热稳定性: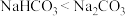 |
D.将某溶液与稀盐酸反应产生的气体通入澄清石灰水中,石灰水变浑浊,说明该溶液中含有CO |
您最近一年使用:0次
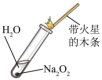
8 . 下列实验装置与操作能达到实验目的的是
| ①验证Na和水反应是否为放热反应 | ②检验Na2O2与 H2O反应有O2生成 | ③用pH试纸测氯水的酸碱度 | ④比较Na2CO3、NaHCO3的稳定性 |
 |  | 用玻璃棒蘸取氯水滴到pH试纸上,再与标准比色卡对比 | 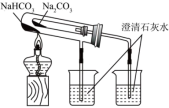 |
| A.①② | B.①③ | C.②③ | D.③④ |
您最近一年使用:0次
解题方法
9 . 为除去括号内的杂质,所选用的试剂或方法正确的是
| A.CO2(HCl):将混合气体通过足量的饱和碳酸钠溶液 |
| B.Na2CO3固体粉末(NaHCO3):加热到固体质量不再减轻为止 |
| C.NaHCO3溶液(Na2CO3):向溶液中加入过量Ca(OH)2溶液,过滤 |
| D.Cl2(HCl):将混合气体通过浓硫酸 |
您最近一年使用:0次
2024-04-07更新
|
69次组卷
|
2卷引用:四川省雅安天立学校腾飞高中2023-2024学年高一上学期11月月考化学试题
10 . 刘丽同学在实验室看到一瓶没有标签的白色粉末,经询问老师得知可能是食盐、碳酸钠或碳酸氢钠。于是她和自己小组的同学们一起对白色粉末的成分进探究。
【作出猜想】
(1)猜想1:可能是食盐 猜想2:可能是_____ 猜想3:可能是_____
【查阅资料】碳酸氢钠的性质:①水溶液呈碱性;②受热易分解;③能和氢氧化钠溶液发生化学反应:NaHCO3+NaOH=Na2CO3+H2O。
【实验探究】
(2)方案如下:
【反思评价】
(3)张伟同学认为通过上述实验还不能确定这种白色粉末就是碳酸钠,他的理由是_____ 。
【继续探究】
(4)小组同学们于是另取了少量白色粉末于试管中,管口塞上带导管的橡胶塞,再将导管通入澄清石灰水中,给试管加热,观察到澄清石灰水未变浑浊,得出该白色粉末是_____ 。
【交流总结】
(5)通过本组同学的探究,作为组长的刘丽同学根据已有的知识及实验情况,总结出了鉴别碳酸钠和碳酸氢钠的如下方法:
①用无色酚酞试液进行鉴别;②用加热的方法进行鉴别;③加入稀盐酸进行鉴别;④加入澄清石灰水进行鉴别。你认为其中可行的是_____ (填序号)。
【拓展延伸】
(6)碳酸氢钠俗称_____ ,在日常生活中用于生产食品,主要起发泡作用,通过上述研究性学习过程,你认为碳酸氢钠除用于食品工业外,在日常生活及实验室中还有哪些应用,试举一例:_____ 。
【作出猜想】
(1)猜想1:可能是食盐 猜想2:可能是
【查阅资料】碳酸氢钠的性质:①水溶液呈碱性;②受热易分解;③能和氢氧化钠溶液发生化学反应:NaHCO3+NaOH=Na2CO3+H2O。
【实验探究】
(2)方案如下:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量白色粉末于试管中,加入足量水溶解,滴加1~2滴无色酚酞试液 | 溶液变红色 | 该白色粉末不是 |
| 取少量该溶液,向其中滴加稀盐酸 | ||
| 再取少量该溶液,向其中滴加澄清石灰水 | 产生白色沉淀 | 该白色粉末是碳酸钠 |
【反思评价】
(3)张伟同学认为通过上述实验还不能确定这种白色粉末就是碳酸钠,他的理由是
【继续探究】
(4)小组同学们于是另取了少量白色粉末于试管中,管口塞上带导管的橡胶塞,再将导管通入澄清石灰水中,给试管加热,观察到澄清石灰水未变浑浊,得出该白色粉末是
【交流总结】
(5)通过本组同学的探究,作为组长的刘丽同学根据已有的知识及实验情况,总结出了鉴别碳酸钠和碳酸氢钠的如下方法:
①用无色酚酞试液进行鉴别;②用加热的方法进行鉴别;③加入稀盐酸进行鉴别;④加入澄清石灰水进行鉴别。你认为其中可行的是
【拓展延伸】
(6)碳酸氢钠俗称
您最近一年使用:0次



