解题方法
1 . A.将一定质量的Mg和Al混合物投入400 mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。
计算:
(1)Mg和Al的总质量为________ g;
(2)硫酸的物质的量浓度为________ ;
(3)生成H2的物质的量为________ 。

B.将一定量的铝粉、氧化铝、氧化镁的混合物加入到300mL ,4mol/L的稀硫酸中,生成标准状况下6.72L气体。向反应后的溶液中滴加一定物质的量浓度的KOH溶液时,所得沉淀的物质的量(mol)与滴加KOH溶液的体积(mL)之间的关系如图所示:
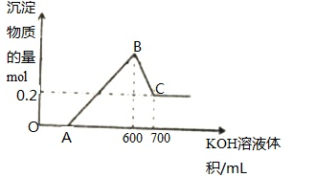
(1)OA对应反应的离子方程式为_________ ,BC对应反应的离子方程式为____________ ;
(2)c(KOH)=_________ mol/L,混合物中氧化铝的物质的量为_____ mol;
(3)A点对应的数值为_______ ;
(4)在中学阶段,实验室里检验B点对应的溶液中的阳离子时,所观察到的现象是___________ 。
(5)向C点对应的溶液中通入足量的CO2所发生反应的离子方程式为_____________ 。
计算:
(1)Mg和Al的总质量为
(2)硫酸的物质的量浓度为
(3)生成H2的物质的量为

B.将一定量的铝粉、氧化铝、氧化镁的混合物加入到300mL ,4mol/L的稀硫酸中,生成标准状况下6.72L气体。向反应后的溶液中滴加一定物质的量浓度的KOH溶液时,所得沉淀的物质的量(mol)与滴加KOH溶液的体积(mL)之间的关系如图所示:

(1)OA对应反应的离子方程式为
(2)c(KOH)=
(3)A点对应的数值为
(4)在中学阶段,实验室里检验B点对应的溶液中的阳离子时,所观察到的现象是
(5)向C点对应的溶液中通入足量的CO2所发生反应的离子方程式为
您最近一年使用:0次
2 . 一定量的Mg、Al的混合物中加入足量盐酸,产生标准状况下的气体5.6L,再在此溶液中加入过量NaOH溶液,产生沉淀5.8克,求:
(1)Mg、Al的物质的量各为多少_________ ?
(2)若将此混合物投入足量的NaOH溶液中,求标准状况下产生气体的体积_________ 。
(1)Mg、Al的物质的量各为多少
(2)若将此混合物投入足量的NaOH溶液中,求标准状况下产生气体的体积
您最近一年使用:0次
3 . 在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如下图所示。
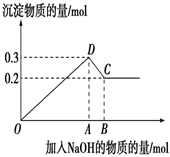
(1)写出代表下列线段发生的反应的离子方程式:
DC段________________________________________________ 。
(2)原溶液中Mg2+、Al3+的物质的量之比为_____________ 。
(3)图中B点时所加入溶液中含NaOH为________ mol
(4)若向50 mL 2 mol·L-1的AlCl3溶液中加入100 mL KOH溶液,充分反应后得到3.12g沉淀。则KOH的物质的量浓度可能为________________________________ 。

(1)写出代表下列线段发生的反应的离子方程式:
DC段
(2)原溶液中Mg2+、Al3+的物质的量之比为
(3)图中B点时所加入溶液中含NaOH为
(4)若向50 mL 2 mol·L-1的AlCl3溶液中加入100 mL KOH溶液,充分反应后得到3.12g沉淀。则KOH的物质的量浓度可能为
您最近一年使用:0次
2018-02-23更新
|
1025次组卷
|
2卷引用:江西省赣州市赣县中学北校区2019-2020学年高一上学期12月月考化学试题
4 . 将0.1 mol的镁、铝混合物溶于100 mL 2 mol·L-1的H2SO4溶液中,然后再滴加1 mol·-1的NaOH溶液。请回答:
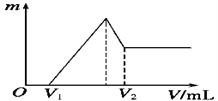
(1)若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化的关系如图所示,当V1=160 mL时,则金属粉末中n(Mg)=______________ mol,V2=_____________ mL。
(2)若混合物仍为0.1 mol,其中Mg粉物质的量分数为a ,用100 mL2mol·L-1的H2SO4溶解此混合物后,再加入450mL1mol/LNaOH溶液,所得沉淀中无Al(OH)3。满足此条件的a的取值范围是______________ 。

(1)若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化的关系如图所示,当V1=160 mL时,则金属粉末中n(Mg)=
(2)若混合物仍为0.1 mol,其中Mg粉物质的量分数为a ,用100 mL2mol·L-1的H2SO4溶解此混合物后,再加入450mL1mol/LNaOH溶液,所得沉淀中无Al(OH)3。满足此条件的a的取值范围是
您最近一年使用:0次
2017-03-04更新
|
616次组卷
|
2卷引用:2016-2017学年江西省南昌市第十中学高一下学期分班考试化学试卷
解题方法
5 . 将一定量的Mg、Al投入100mL一定的物质的量浓度的盐酸中,合金全部溶解。向所得溶液中滴加5mol/L的NaOH至过量,生成的沉淀的质量与加入NaOH的体积的关系如图所示。_____ mol;nAl(OH)3= _______ mol。
②原HCl的物质的量浓度c=_______________ mol/L
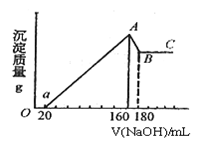
②原HCl的物质的量浓度c=
您最近一年使用:0次
6 . 把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入1mol/LNaOH溶液,生成沉淀的质量和加入NaOH溶液的体积如图所示。
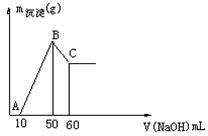
求:(1)合金中镁、铝各自的质量_______ 、_________ 。
(2)盐酸的物质的量浓度______________ 。

求:(1)合金中镁、铝各自的质量
(2)盐酸的物质的量浓度
您最近一年使用:0次
7 . 把由NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量的水中,有1.16 g白色沉淀析出,向所得的浊液里,逐渐加入0.5 mol/L的盐酸,加入盐酸的体积和生成沉淀的质量如图所示:
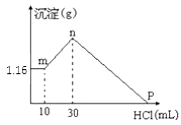
(1)写出m-n段反应的离子方程式___________________ 。
(2)混合物中NaOH的物质的量是____________ ,AlCl3的物质的量是__________ ,MgCl2的物质的量是___________ 。
(3)P点所表示的加入盐酸的体积是_________ mL。

(1)写出m-n段反应的离子方程式
(2)混合物中NaOH的物质的量是
(3)P点所表示的加入盐酸的体积是
您最近一年使用:0次
8 . (1)实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为:MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O,取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。
MnCl2+Cl2↑+2H2O,取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。
请回答下列问题:
①写出该反应的离子反应方程式_________________________,②反应中被氧化的HCl的物质的量为 ________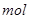 。③实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸的物质的量浓度_________
。③实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸的物质的量浓度_________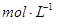 。
。
(2)把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入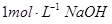 溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。
溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。
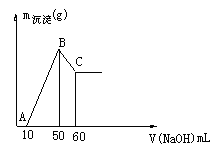
①合金中镁的质量 g。
②盐酸的物质的量浓度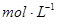 。
。
 MnCl2+Cl2↑+2H2O,取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。
MnCl2+Cl2↑+2H2O,取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。请回答下列问题:
①写出该反应的离子反应方程式_________________________,②反应中被氧化的HCl的物质的量为 ________
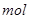 。③实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸的物质的量浓度_________
。③实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸的物质的量浓度_________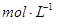 。
。(2)把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入
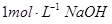 溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。
溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。
①合金中镁的质量 g。
②盐酸的物质的量浓度
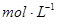 。
。
您最近一年使用:0次
2015-06-03更新
|
466次组卷
|
2卷引用:2014-2015学年湖南省益阳市箴言中学高一12月月考化学试卷
10-11高二上·甘肃天水·阶段练习
9 . 若含有1 mol Mg2+和1 mol Al3+的混合溶液,现按下图横坐标依次加入7 mol NaOH溶液、1 mol盐酸,通入1 mol CO2气体,纵坐标为混合沉淀的物质的量。请画出沉淀的量随反应的变化曲线,并写出各步反应的离子方程式。
_____________
___________ _____________ ________________ ___________ _______________

您最近一年使用:0次



