名校
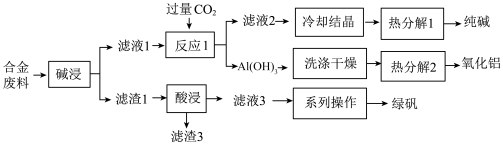
1 . 为探索工业废料的再利用,某化学兴趣小组用含有铝、铁和铜等合金废料制取纯碱、氧化铝和绿矾( ),其工艺流程如下图。
),其工艺流程如下图。
请回答下列问题:
(1)写出“碱浸”中发生反应的化学方程式 ___________ 。
(2)写出“热分解1”的化学方程式为___________ ,纯碱在生产生活中的一种用途是___________ 。
(3)根据流程中的信息,判断“反应1”中生成 的
的离子方程式 为___________ 。
(4)滤渣3的主要成分是___________ (填化学式)。
(5)该工艺流程中,可循环的物质是___________ (填化学式)。
(6)工业废水中含有重铬酸根离子( )有毒,必须处理达标后才能排放。工业上常用绿矾(
)有毒,必须处理达标后才能排放。工业上常用绿矾( )做处理剂,反应的离子方程式如下:
)做处理剂,反应的离子方程式如下: (未配平),在该反应方程式中氧化产物与还原产物的物质的量之比是
(未配平),在该反应方程式中氧化产物与还原产物的物质的量之比是___________ ,当转移a mol电子,则处理 的粒子数为
的粒子数为___________ 。
 ),其工艺流程如下图。
),其工艺流程如下图。
请回答下列问题:
(1)写出“碱浸”中发生反应的
(2)写出“热分解1”的化学方程式为
(3)根据流程中的信息,判断“反应1”中生成
 的
的(4)滤渣3的主要成分是
(5)该工艺流程中,可循环的物质是
(6)工业废水中含有重铬酸根离子(
 )有毒,必须处理达标后才能排放。工业上常用绿矾(
)有毒,必须处理达标后才能排放。工业上常用绿矾( )做处理剂,反应的离子方程式如下:
)做处理剂,反应的离子方程式如下: (未配平),在该反应方程式中氧化产物与还原产物的物质的量之比是
(未配平),在该反应方程式中氧化产物与还原产物的物质的量之比是 的粒子数为
的粒子数为
您最近一年使用:0次
解题方法
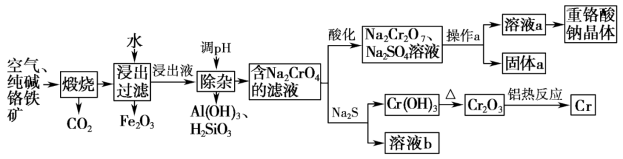
2 . 重铬酸钠是一种用途极广的氧化剂,以铬铁矿[主要成分Fe(CrO2)2,含有Al2O3、Fe2O3、SiO2等杂质]为主要原料生产重铬酸钠晶体,同时回收Cr的主要工艺流程如图:
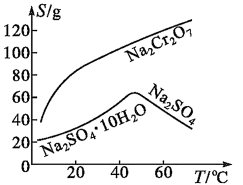
已知部分物质的溶解度曲线如图所示。
请回答下列问题:
(1)煅烧生成Na2CrO4的化学方程式为___________ 。
(2)将Fe2O3溶于稀硫酸后得到对应盐溶液,检验该溶液中金属阳离子的方法是___________ 。
(3)若通过加入稀硫酸调节溶液pH使铝元素转化为Al(OH)3,所发生反应的离子方程式为___________ 。
(4)Na2CrO4经酸化转化为Na2Cr2O7的原理为___________ (结合离子方程式用平衡移动原理解释)。
(5)操作a的实验步骤为___________ 。
(6)加入Na2S溶液反应后,硫元素全部以S2O 的形式存在,该反应中氧化剂和还原剂的物质的量之比为
的形式存在,该反应中氧化剂和还原剂的物质的量之比为___________ 。
(7)含铬废水会对环境造成污染,要经过化学处理才能排放。现将含CrO 的废水加入可溶性钡盐生成BaCrO4沉淀,加入可溶性钡盐后,废水中Ba2+的浓度应不小于
的废水加入可溶性钡盐生成BaCrO4沉淀,加入可溶性钡盐后,废水中Ba2+的浓度应不小于___________ mol•L−1,CrO 才能沉淀完全[当溶液中c(CrO
才能沉淀完全[当溶液中c(CrO )≤1×10-5 mol•L−1时,可视作该离子沉淀完全,已知Ksp(BaCrO4)=1.2×10−10]
)≤1×10-5 mol•L−1时,可视作该离子沉淀完全,已知Ksp(BaCrO4)=1.2×10−10]

已知部分物质的溶解度曲线如图所示。

请回答下列问题:
(1)煅烧生成Na2CrO4的化学方程式为
(2)将Fe2O3溶于稀硫酸后得到对应盐溶液,检验该溶液中金属阳离子的方法是
(3)若通过加入稀硫酸调节溶液pH使铝元素转化为Al(OH)3,所发生反应的离子方程式为
(4)Na2CrO4经酸化转化为Na2Cr2O7的原理为
(5)操作a的实验步骤为
(6)加入Na2S溶液反应后,硫元素全部以S2O
 的形式存在,该反应中氧化剂和还原剂的物质的量之比为
的形式存在,该反应中氧化剂和还原剂的物质的量之比为(7)含铬废水会对环境造成污染,要经过化学处理才能排放。现将含CrO
 的废水加入可溶性钡盐生成BaCrO4沉淀,加入可溶性钡盐后,废水中Ba2+的浓度应不小于
的废水加入可溶性钡盐生成BaCrO4沉淀,加入可溶性钡盐后,废水中Ba2+的浓度应不小于 才能沉淀完全[当溶液中c(CrO
才能沉淀完全[当溶液中c(CrO )≤1×10-5 mol•L−1时,可视作该离子沉淀完全,已知Ksp(BaCrO4)=1.2×10−10]
)≤1×10-5 mol•L−1时,可视作该离子沉淀完全,已知Ksp(BaCrO4)=1.2×10−10]
您最近一年使用:0次
名校
3 . 某课外小组研究铝土矿中Al2O3的含量。查阅资料得知,铝土矿的主要成分是Al2O3,杂质是Fe2O3、SiO2等。从铝土矿中提取Al2O3的过程如下:
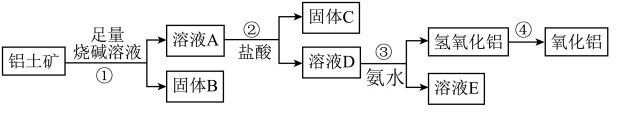
(1)固体B的主要用途为(只写一种即可)______________ ;
(2)第①步,向铝土矿中加入足量烧碱溶液,充分反应,发生反应的离子方程式是:___________ 、_______________ ;
(3)第③步中,生成氢氧化铝的离子方程式是___________________ 。若往A溶液中通入足量CO2,产生的沉淀为____________________ (填化学式);
(4)工业上制取AlCl3常用Al2O3与C、Cl2在高温条件下反应,已知每消耗0.5mol碳单质,转移1mol电子,则该反应的氧化产物为_____________ (填化学式)。

(1)固体B的主要用途为(只写一种即可)
(2)第①步,向铝土矿中加入足量烧碱溶液,充分反应,发生反应的离子方程式是:
(3)第③步中,生成氢氧化铝的离子方程式是
(4)工业上制取AlCl3常用Al2O3与C、Cl2在高温条件下反应,已知每消耗0.5mol碳单质,转移1mol电子,则该反应的氧化产物为
您最近一年使用:0次
4 . 已知A为淡黄色固体,T、R 为两种常见的用途广泛的金属单质,D具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体。
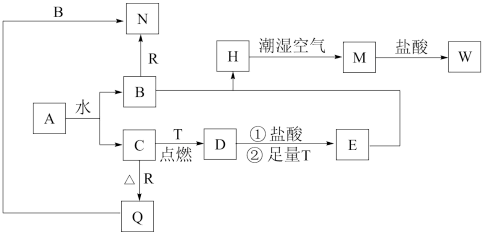
(1)写出下列物质的化学式:D:_______ R: _______
(2)按要求写出下列反应方程式
A与水反应的化学方程式_______
B与R反应的离子方程式_______
H转化为M的化学方程式_______
(3)向R的盐溶液中滴加弱碱,可制得一种具有吸附性的白色胶装物质,该反应的离子方程为_______

(1)写出下列物质的化学式:D:
(2)按要求写出下列反应方程式
A与水反应的化学方程式
B与R反应的离子方程式
H转化为M的化学方程式
(3)向R的盐溶液中滴加弱碱,可制得一种具有吸附性的白色胶装物质,该反应的离子方程为
您最近一年使用:0次
5 . 已知B、C为用途广泛的金属,H具有磁性氧化物,I是一种白色胶状沉淀,它们有如图所示的转化关系(部分产物未列出):

回答下列问题:
(1).E和G的化学式分别为_______ 。
(2).写出反应的化学方程式:①_______ 、③_______ 。
(3)写出反应的离子方程式②_______ 、④_______ 。

回答下列问题:
(1).E和G的化学式分别为
(2).写出反应的化学方程式:①
(3)写出反应的离子方程式②
您最近一年使用:0次



