1 . 有四种常见药物:①阿司匹林( )②青霉素③胃舒平[Al(OH)3]④麻黄碱。
)②青霉素③胃舒平[Al(OH)3]④麻黄碱。
请回答:
(1)某同学胃酸过多,应选用的药物是_______ (填序号),抗酸药的成分Al(OH)3中和胃酸过多的离子方程式为________ 。
(2)由于具有兴奋作用,国际奥委会严禁运动员服用的药物是___________ (填序号,下同)。
(3)从用药安全角度考虑,使用前要进行皮肤敏感性测试的药物是___________ 。
(4)阿司匹林药品标签上贴有OTC,它表示___________ 。
(5)滥用药物会导致不良后果,如过量服用___________ (填序号)会出现水杨酸中毒,应立即停药,并静脉注射NaHCO3溶液,试写出该药物和NaHCO3反应的离子方程式:____________ 。
 )②青霉素③胃舒平[Al(OH)3]④麻黄碱。
)②青霉素③胃舒平[Al(OH)3]④麻黄碱。请回答:
(1)某同学胃酸过多,应选用的药物是
(2)由于具有兴奋作用,国际奥委会严禁运动员服用的药物是
(3)从用药安全角度考虑,使用前要进行皮肤敏感性测试的药物是
(4)阿司匹林药品标签上贴有OTC,它表示
(5)滥用药物会导致不良后果,如过量服用
您最近一年使用:0次
名校
解题方法
2 . 有关铝及其化合物的说法正确的是
| A.铝片可与冷水剧烈反应 | B.铝热反应放出的热量使生成的铁熔化 |
| C.氧化铝是碱性氧化物 | D.氢氧化铝能溶于稀氨水 |
您最近一年使用:0次
2022-12-24更新
|
214次组卷
|
2卷引用:上海市金山区2022-2023学年高三第一次质量调研(一模)化学试题
3 . 表述Ⅰ与表述Ⅱ中,两者之间因果关系错误 的是
| 选项 | 表述Ⅰ | 表述Ⅱ |
| A | 金属钠保存在煤油中,以隔绝空气 | 常温下,金属钠在空气中会发生反应 |
| B | 用 溶液腐蚀印刷电路板 溶液腐蚀印刷电路板 |  溶液能与 溶液能与 反应 反应 |
| C | 将干燥的氯气通入盛有红色鲜花的集气瓶中,鲜花褪色 | 干燥的氯气具有漂白性 |
| D | 氢氧化铝可用于治疗胃酸过多 | 氢氧化铝可与盐酸反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-23更新
|
233次组卷
|
2卷引用:安徽省安庆市2021-2022学年高一上学期期末考试化学试题
解题方法
4 . 下列离子方程式书写正确的是
A.金属钠投入水中: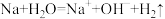 |
B.氯气通入澄清石灰水中: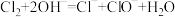 |
C.氢氧化铝溶于盐酸: |
D.将铜粉加入氯化铁溶液中: |
您最近一年使用:0次
2022-01-19更新
|
242次组卷
|
2卷引用:广东省佛山市2021-2022学年高一上学期期末考试化学试题
名校
解题方法
5 . 下列性质和用途一致的是
| A.钠单质熔点较低,可用于冶炼金属钛 |
| B.K2FeO4(高铁酸钾)具有强氧化性,可用作杀菌消毒 |
| C.FeCl3溶液具有酸性,可以腐蚀铜箔制造印刷电路板 |
| D.氢氧化铝受热分解,可用于中和过多的胃酸 |
您最近一年使用:0次
解题方法
6 . 钠、铝、铁是三种重要的金属,三种金属及其化合物在生活生产中有重要作用。请回答下列问题:
(1)将一小块钠投入到CuCl2溶液中,观察到的现象是____ 。
(2)工业上通过以下反应生产高铁酸钠(Na2FeO4):3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4+3NaCl+6NaNO3+5H2O,此反应中氧化剂和还原剂的物质的量之比为____ 。
(3)胃舒平是日常生活中常用的抗酸药,其成分含有Al(OH)3,其抗酸原理是(用离子方程式表示)____ 。
(4)Fe在Cl2燃烧,所得产物的化学式是____ 。将该产物溶于水配成溶液,分装在两支试管中。请回答:
a.若向其中一支试管中滴加KSCN溶液,则溶液变成____ 色。
b.向另一支试管中滴加NaOH溶液,其反应的化学方程式为____ 。
(5)向一定量的Fe、FeO、Fe2O3、Fe3O4的混合物中加入100 mL2 mol·L-1的盐酸,恰好完全反应,放出11.2 mL(标准状况)气体,所得溶液加入KSCN溶液不变红色。用足量的CO在高温下还原相同质量的此混合物,所得铁的质量为____ g。
(1)将一小块钠投入到CuCl2溶液中,观察到的现象是
| A.钠溶解,有铜析出并有气体产生 | B.只有气体产生 |
| C.只有沉淀产生 | D.既有气体产生,又有蓝色沉淀产生 |
(3)胃舒平是日常生活中常用的抗酸药,其成分含有Al(OH)3,其抗酸原理是(用离子方程式表示)
(4)Fe在Cl2燃烧,所得产物的化学式是
a.若向其中一支试管中滴加KSCN溶液,则溶液变成
b.向另一支试管中滴加NaOH溶液,其反应的化学方程式为
(5)向一定量的Fe、FeO、Fe2O3、Fe3O4的混合物中加入100 mL2 mol·L-1的盐酸,恰好完全反应,放出11.2 mL(标准状况)气体,所得溶液加入KSCN溶液不变红色。用足量的CO在高温下还原相同质量的此混合物,所得铁的质量为
您最近一年使用:0次
名校
解题方法
7 . 下列离子方程式的书写正确的是
| A.将1molCl2通入到含1molFeI2溶液中:2Fe2++2I﹣+2Cl2=2Fe3++4Cl﹣+I2 |
B.1mol·L﹣1的NaAlO2溶液和2.5mol·L﹣1的HCl溶液等体积互相均匀混合:2AlO +5H+=Al3++Al(OH)3↓+H2O +5H+=Al3++Al(OH)3↓+H2O |
C.过量SO2通入到NaClO溶液中:SO2+H2O+ClO﹣=HClO+HSO |
D.Ca(HCO3)2溶液与足量NaOH溶液反应:Ca2++HCO +OH﹣=CaCO3↓+H2O +OH﹣=CaCO3↓+H2O |
您最近一年使用:0次
8 . (I)俄美科学家联合小组宣布合成出114号元素(Fl)的一种同位素,该原子的质量数是289,试回答下列问题:
(1)该元素在周期表中的位置为:___________ ,属于___________ 元素(填“金属”或“非金属”)。
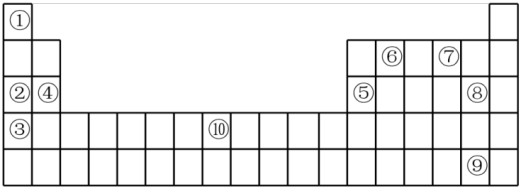
(II)下表为元素周期表的部分,列出了10种元素在元素周期表中的位置,回答下列问题:
(2)②③④三种元素最高价氧化物的水化物碱性由强到弱的顺序是___________ (填化学式)。
(3)元素⑦的简单氢化物与③的单质反应的离子方程式为___________ ;
(4)元素②和⑤的最高价氧化物的水化物反应的离子方程式为___________ ;
(5)元素⑩为铁,其单质与⑧的单质反应的化学方程式为___________ ;
(6)部分短周期元素的原子半径及主要化合价如下表,判断以下叙述不正确的是___________
(1)该元素在周期表中的位置为:
(II)下表为元素周期表的部分,列出了10种元素在元素周期表中的位置,回答下列问题:

(2)②③④三种元素最高价氧化物的水化物碱性由强到弱的顺序是
(3)元素⑦的简单氢化物与③的单质反应的离子方程式为
(4)元素②和⑤的最高价氧化物的水化物反应的离子方程式为
(5)元素⑩为铁,其单质与⑧的单质反应的化学方程式为
(6)部分短周期元素的原子半径及主要化合价如下表,判断以下叙述不正确的是___________
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A.L2+、R2-的核外电子数相等 |
| B.单质与稀盐酸反应的速率L<Q |
| C.M与T形成的化合物具有两性 |
| D.T与R可形成的化合物TR2、TR3 |
您最近一年使用:0次
解题方法
9 . 下列关于药物的说法正确的是
| A.药物的服用剂量越大,治疗效果越明显 |
| B.包装上印有“OTC”标志的药品属于处方药 |
| C.氢氧化铝可作为抑酸剂,用于治疗胃酸过多 |
| D.长期大量服用阿司匹林可预防某些疾病,没有副作用 |
您最近一年使用:0次
解题方法
10 . 化学与生活密切相关。下列说法错误的是
| A.碳酸钠可用于去除餐具的油污 |
| B.氢氧化铝可用于中和过多胃酸 |
| C.碳酸钡可用于胃肠X射线造影检查 |
| D.红葡萄酒中添加少量SO2具有抗氧化的作用 |
您最近一年使用:0次



