解题方法
1 . 下表为元素周期表的一部分,请回答有关问题(用元素符号表示对应元素):
(1)⑤和⑧的元素符号是___________ 和___________ 。
(2)表中最活泼的金属是___________ ,非金属性最强的元素是___________ (填写元素符号,下同)。
(3)表中能形成两性氢氧化物的元素是___________ ,分别写出该元素的氢氧化物与⑥、⑨的最高价氧化物对应水化物反应的化学方程式:___________ ,___________ 。
(4)比较⑦、⑩单质氧化性的强弱,请用化学方程式表示___________ 。
| 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ | ⑩ |
(2)表中最活泼的金属是
(3)表中能形成两性氢氧化物的元素是
(4)比较⑦、⑩单质氧化性的强弱,请用化学方程式表示
您最近一年使用:0次
名校
解题方法
2 . 下列有关物质的性质与用途不具有对应关系的是
| A.Fe2O3能与酸反应,可用作外墙涂料 |
| B.钠具有强还原性,可用于冶炼金属Ti |
| C.铁粉能与O2反应,可用作食品保存的吸氧剂 |
| D.Al(OH)3能与酸反应,可用于治疗胃酸过多 |
您最近一年使用:0次
名校
解题方法
3 . 化学在生活中无处不在,下列有关物质及成分、性质和用途有误的是
| 选项 | 物质及成分 | 性质 | 用途 |
| A | 纯碱( ) ) | 与酸反应产生二氧化碳 | 作发酵粉 |
| B | 磁性氧化铁( ) ) | 难溶于水,黑色 | 制造磁性材料 |
| C |  | 与 、 、 均能反应放出氧气 均能反应放出氧气 |  可以为航天员供氧 可以为航天员供氧 |
| D | 胃舒平[ ] ] | 与酸发生中和 | 作胃酸中和剂 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
4 . 重铬酸钾( ),室温下为橘红色结晶性粉末,溶于水,不溶于乙醇。实验室以铬铁矿(主要成分为
),室温下为橘红色结晶性粉末,溶于水,不溶于乙醇。实验室以铬铁矿(主要成分为 ,还含有硅、铝等杂质)为原料,利用固体碱熔氧化法制备
,还含有硅、铝等杂质)为原料,利用固体碱熔氧化法制备 的步骤如下:
的步骤如下:
步骤I.熔融氧化
将6g铬铁矿与4g氯酸钾在研钵中混合均匀,取碳酸钠和氢氧化钠各4.5g于仪器A中混匀后,小火熔融,再将矿粉分批加入坩埚中并不断搅拌。用煤气灯强热,灼烧30~35min,稍冷几分钟,加水,过滤,得滤液i,滤渣中含红棕色固体。
步骤Ⅱ.中和除杂
将滤液i用稀硫酸调pH为7~8,加热煮沸3min后,趁热过滤,用少量蒸馏水洗涤残渣,得滤液ii。
步骤Ⅲ.结晶
将滤液ii转移至蒸发皿中,用6 硫酸调pH后加入1g氯化钾,在水浴上浓缩至表面有晶膜为止,冷却结晶,过滤得重铬酸钾晶体,烘干,称量。
硫酸调pH后加入1g氯化钾,在水浴上浓缩至表面有晶膜为止,冷却结晶,过滤得重铬酸钾晶体,烘干,称量。
步骤Ⅳ.纯度测定
利用库仑滴定法测定 固体样品的纯度:取mg样品,配成250mL溶液,取2mL溶液进行库仑法滴定,重复三次实验,测定平均电量(Q)为1.158C,已知计算
固体样品的纯度:取mg样品,配成250mL溶液,取2mL溶液进行库仑法滴定,重复三次实验,测定平均电量(Q)为1.158C,已知计算 的浓度公式为
的浓度公式为 (F为96500
(F为96500 ,N为1个
,N为1个 转化为
转化为 时转移的电子数,V为滴定样品溶液的体积)。已知:常见微粒在不同pH条件下的存在形式如下图所示。当离子浓度
时转移的电子数,V为滴定样品溶液的体积)。已知:常见微粒在不同pH条件下的存在形式如下图所示。当离子浓度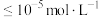 ,则认为该微粒已除尽。
,则认为该微粒已除尽。

回答下列问题:
(1)仪器A为_______(填标号)。
(2)若用 代替
代替 ,则理论上转化1mol
,则理论上转化1mol  所需
所需 的体积(标准状况,单位为L)是所消耗
的体积(标准状况,单位为L)是所消耗 物质的量的
物质的量的_______ 倍。
(3)步骤I中“分批加入”的目的是_______ 。
(4)若步骤Ⅱ中“调pH至3~4”的不良后果是_______ 。
(5)进一步提纯步骤Ⅲ所得晶体的方法是_______ 。
(6)探究pH对 溶液的氧化性强弱的影响。
溶液的氧化性强弱的影响。
(7) 与浓盐酸反应可制得
与浓盐酸反应可制得 ,已知部分卤素单质的键能如下表:
,已知部分卤素单质的键能如下表:
试解释键能 的原因
的原因_______ 。
(8) 固体样品的纯度为
固体样品的纯度为_______ (用含m的式子表示)。
 ),室温下为橘红色结晶性粉末,溶于水,不溶于乙醇。实验室以铬铁矿(主要成分为
),室温下为橘红色结晶性粉末,溶于水,不溶于乙醇。实验室以铬铁矿(主要成分为 ,还含有硅、铝等杂质)为原料,利用固体碱熔氧化法制备
,还含有硅、铝等杂质)为原料,利用固体碱熔氧化法制备 的步骤如下:
的步骤如下:步骤I.熔融氧化
将6g铬铁矿与4g氯酸钾在研钵中混合均匀,取碳酸钠和氢氧化钠各4.5g于仪器A中混匀后,小火熔融,再将矿粉分批加入坩埚中并不断搅拌。用煤气灯强热,灼烧30~35min,稍冷几分钟,加水,过滤,得滤液i,滤渣中含红棕色固体。
步骤Ⅱ.中和除杂
将滤液i用稀硫酸调pH为7~8,加热煮沸3min后,趁热过滤,用少量蒸馏水洗涤残渣,得滤液ii。
步骤Ⅲ.结晶
将滤液ii转移至蒸发皿中,用6
 硫酸调pH后加入1g氯化钾,在水浴上浓缩至表面有晶膜为止,冷却结晶,过滤得重铬酸钾晶体,烘干,称量。
硫酸调pH后加入1g氯化钾,在水浴上浓缩至表面有晶膜为止,冷却结晶,过滤得重铬酸钾晶体,烘干,称量。步骤Ⅳ.纯度测定
利用库仑滴定法测定
 固体样品的纯度:取mg样品,配成250mL溶液,取2mL溶液进行库仑法滴定,重复三次实验,测定平均电量(Q)为1.158C,已知计算
固体样品的纯度:取mg样品,配成250mL溶液,取2mL溶液进行库仑法滴定,重复三次实验,测定平均电量(Q)为1.158C,已知计算 的浓度公式为
的浓度公式为 (F为96500
(F为96500 ,N为1个
,N为1个 转化为
转化为 时转移的电子数,V为滴定样品溶液的体积)。已知:常见微粒在不同pH条件下的存在形式如下图所示。当离子浓度
时转移的电子数,V为滴定样品溶液的体积)。已知:常见微粒在不同pH条件下的存在形式如下图所示。当离子浓度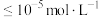 ,则认为该微粒已除尽。
,则认为该微粒已除尽。
回答下列问题:
(1)仪器A为_______(填标号)。
| A.普通坩埚 | B. 坩埚 坩埚 | C.氮化硅坩埚 | D.石英坩埚 |
 代替
代替 ,则理论上转化1mol
,则理论上转化1mol  所需
所需 的体积(标准状况,单位为L)是所消耗
的体积(标准状况,单位为L)是所消耗 物质的量的
物质的量的(3)步骤I中“分批加入”的目的是
(4)若步骤Ⅱ中“调pH至3~4”的不良后果是
(5)进一步提纯步骤Ⅲ所得晶体的方法是
(6)探究pH对
 溶液的氧化性强弱的影响。
溶液的氧化性强弱的影响。| 实验操作 | 实验现象 | 实验结论 |
向酸化的 溶液中加入一定量甲醇 溶液中加入一定量甲醇 | 溶液形成蓝紫色溶液,并产生无色无味的气体 | |
向碱化的 溶液中加入相同量甲醇 溶液中加入相同量甲醇 | 酸性条件下 溶液的氧化性更强 溶液的氧化性更强 |
 与浓盐酸反应可制得
与浓盐酸反应可制得 ,已知部分卤素单质的键能如下表:
,已知部分卤素单质的键能如下表:| 化学键 | F-F | C1-Cl | Br-Br |
键能/( ) ) | 157 | 242.7 | 193.7 |
 的原因
的原因(8)
 固体样品的纯度为
固体样品的纯度为
您最近一年使用:0次
名校
5 . 明矾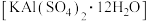 可用作净水剂。某同学设计利用废铝箔(主要成分为
可用作净水剂。某同学设计利用废铝箔(主要成分为 ,含少量
,含少量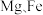 等)制备明矾的流程如下图所示。
等)制备明矾的流程如下图所示。

下列说法不正确 的是
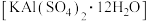 可用作净水剂。某同学设计利用废铝箔(主要成分为
可用作净水剂。某同学设计利用废铝箔(主要成分为 ,含少量
,含少量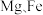 等)制备明矾的流程如下图所示。
等)制备明矾的流程如下图所示。
下列说法
A.①中反应的离子方程式是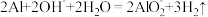 |
B.③中反应的离子方程式是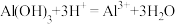 |
| C.操作a是蒸发结晶,用到的仪器有蒸发皿、酒精灯、玻璃棒等 |
D.明矾净水的原理: 水解生成的 水解生成的 胶体能吸附水中的悬浮颗粒物 胶体能吸附水中的悬浮颗粒物 |
您最近一年使用:0次
2023-05-07更新
|
583次组卷
|
3卷引用:北京市东城区2022-2023学年高三第二次模拟考试化学试题
北京市东城区2022-2023学年高三第二次模拟考试化学试题(已下线)考点15 铝及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)黑龙江省哈尔滨师范大学附属中学2024届高三上学期开学考试化学试题
解题方法
6 . 下列治疗胃酸过多的最佳药品是
| A.纯碱 | B.烧碱 | C.氢氧化铝片 | D.小苏打 |
您最近一年使用:0次
解题方法
7 . 化学与生产、生活密切相关。下列关于物质用途的说法错误的是
| A.14C:测定文物年代 | B.Al(OH)3:制抗酸药 |
| C.SO2:作食品添加剂 | D.CuSO4:制红色颜料 |
您最近一年使用:0次
8 . (I)俄美科学家联合小组宣布合成出114号元素(Fl)的一种同位素,该原子的质量数是289,试回答下列问题:
(1)该元素在周期表中的位置为:___________ ,属于___________ 元素(填“金属”或“非金属”)。
(II)下表为元素周期表的部分,列出了10种元素在元素周期表中的位置,回答下列问题:
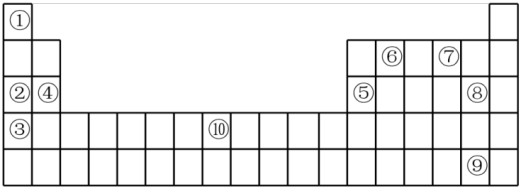
(2)②③④三种元素最高价氧化物的水化物碱性由强到弱的顺序是___________ (填化学式)。
(3)元素⑦的简单氢化物与③的单质反应的离子方程式为___________ ;
(4)元素②和⑤的最高价氧化物的水化物反应的离子方程式为___________ ;
(5)元素⑩为铁,其单质与⑧的单质反应的化学方程式为___________ ;
(6)部分短周期元素的原子半径及主要化合价如下表,判断以下叙述不正确的是___________
(1)该元素在周期表中的位置为:
(II)下表为元素周期表的部分,列出了10种元素在元素周期表中的位置,回答下列问题:

(2)②③④三种元素最高价氧化物的水化物碱性由强到弱的顺序是
(3)元素⑦的简单氢化物与③的单质反应的离子方程式为
(4)元素②和⑤的最高价氧化物的水化物反应的离子方程式为
(5)元素⑩为铁,其单质与⑧的单质反应的化学方程式为
(6)部分短周期元素的原子半径及主要化合价如下表,判断以下叙述不正确的是___________
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A.L2+、R2-的核外电子数相等 |
| B.单质与稀盐酸反应的速率L<Q |
| C.M与T形成的化合物具有两性 |
| D.T与R可形成的化合物TR2、TR3 |
您最近一年使用:0次
名校
解题方法
9 . 某溶液既能溶解Al(OH)3,又能溶解H2SiO3,在该溶液中可能大量共存的离子组是
A.K+、NH 、HCO 、HCO 、NO 、NO | B.Na+、SO 、Cl-、ClO- 、Cl-、ClO- |
C.Na+、Fe2+、SO 、NO 、NO | D.K+、Na+、SO 、S2- 、S2- |
您最近一年使用:0次
解题方法
10 . 下列离子方程式书写错误的是
A.工业上制漂白液: |
B.复方氢氧化铝片做抗酸药(胃酸为强酸): |
C.二氧化氮溶于水: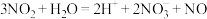 |
D.氨气溶于水: |
您最近一年使用:0次



