解题方法
1 . 将铁屑溶于过量的稀硫酸中,再加入适量硝酸,反应完全后加入过量的氨水,有红褐色沉淀生成。过滤,灼烧沉淀物至质量不再发生变化,得到红棕色的残渣。上述沉淀是_________ ,残渣是_________ 。
您最近一年使用:0次
2022-11-24更新
|
228次组卷
|
2卷引用:苏教2020版化学必修第二册专题7第三单元 含氮化合物的合理使用课后习题
2 . 铁的氢氧化物
(1)Fe(OH)2、Fe(OH)3的比较
(2)Fe(OH)2的制备
Fe(OH)2具有很强的还原性,易被氧化为Fe(OH)3.在实验室中制备Fe(OH)2,并使Fe(OH)2长时间保持白色沉淀状态,成功的关键有以下两点:
①溶液中不含Fe3+和O2等氧化性物质;
②制备过程中,保证生成的Fe(OH)2在密闭的隔绝空气的体系中。
(1)Fe(OH)2、Fe(OH)3的比较
| 名称 | Fe(OH)2 | Fe(OH)3 |
| 颜色 | ① | ② |
| 热稳定性 | —— | ③ |
| 水溶解性 | 难溶 | 难溶 |
| 制备(离子方程式) | ④ | ⑤ |
| 与盐酸反应(离子方程式) | ⑥ | ⑦ |
| 转化 | ⑧ | |
Fe(OH)2具有很强的还原性,易被氧化为Fe(OH)3.在实验室中制备Fe(OH)2,并使Fe(OH)2长时间保持白色沉淀状态,成功的关键有以下两点:
①溶液中不含Fe3+和O2等氧化性物质;
②制备过程中,保证生成的Fe(OH)2在密闭的隔绝空气的体系中。
您最近一年使用:0次
21-22高一上·全国·课时练习
解题方法
3 .
化学式 | Fe(OH)2 | Fe(OH)3 |
颜色状态 | 白色固体 | 红褐色固体 |
与盐酸反应 | Fe(OH)2+2H+=Fe2++2H2O | Fe(OH)3+3H+=Fe3++3H2O |
受热分解 | - | |
制备 | 可溶性亚铁盐与碱溶液反应: | 可溶性铁盐与碱溶液反应: |
二者的关系 | 在空气中,Fe(OH)2能够非常迅速地被氧气氧化成Fe(OH)3,现象是白色絮状沉淀迅速变成 | |
您最近一年使用:0次
4 . 氯化铁的用途之一是五金蚀刻,蚀刻产品有眼镜架、钟表、电子元件和标牌等。例如,日常生活中不锈钢广告牌上的图形或文字就是用氯化铁溶液蚀刻而成的。
(1)请写出用氯化铁溶液蚀刻不锈钢时发生的主要反应的离子方程式______ 。
(2)铁红是一种常见的红色颜料。请你设计在实验室中由氯化铁制备铁红的实验方案________ ,并写出有关反应的化学方程式____________ 。
(1)请写出用氯化铁溶液蚀刻不锈钢时发生的主要反应的离子方程式
(2)铁红是一种常见的红色颜料。请你设计在实验室中由氯化铁制备铁红的实验方案
您最近一年使用:0次
5 . 把少量废铁屑溶于过量稀硫酸中,过滤,除去杂质。向滤液中加入适量氯水,再加入过量的氨水,有红褐色沉淀生成。过滤,加热沉淀物至质量不再发生变化,得到红棕色的残渣。上述沉淀和残渣分别为___________ 和___________ (填化学式)。
您最近一年使用:0次
2021-12-01更新
|
645次组卷
|
3卷引用:人教2019版必修第一册第三章 铁 金属材料复习与提高
20-21高二上·全国·课时练习
解题方法
6 . 在Fe(OH)3中,逐滴加入HI稀溶液,会发生一系列变化,请简述原因。
(1)固体溶解,溶液显黄色,原因是___ ;有关离子方程式为___ 。
(2)最后溶液颜色加深,原因是___ ;有关离子方程式为___ 。
(1)固体溶解,溶液显黄色,原因是
(2)最后溶液颜色加深,原因是
您最近一年使用:0次
7 . 以含Fe2O3、FeO、SiO2、A12O3的混合物为原料,设计两种制备铁红(Fe2O3)的一种方案,部分产物已略去。

其中第③步试剂X体积(ml)与产生沉淀质量(g)的关系如图所示。
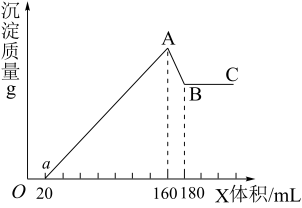
回答下列问题:
(1)溶液B中的溶质是_______ (填化学式)
(2)第②步的化学方程式为_______ 。
(3)试剂X的溶质可能是_______ (选填编号)
A.HNO3 B.NaHCO3 C. NH3.H2O D.NaOH
加入足量试剂X后,应进行的操作名称是_______ 。
(4)若试剂X的浓度为5mol/L,则固体中Al2O3的质量是_______ g。最终得到铁红的质量是_______ g(保留一位小数)

其中第③步试剂X体积(ml)与产生沉淀质量(g)的关系如图所示。

回答下列问题:
(1)溶液B中的溶质是
(2)第②步的化学方程式为
(3)试剂X的溶质可能是
A.HNO3 B.NaHCO3 C. NH3.H2O D.NaOH
加入足量试剂X后,应进行的操作名称是
(4)若试剂X的浓度为5mol/L,则固体中Al2O3的质量是
您最近一年使用:0次
2021-03-08更新
|
156次组卷
|
3卷引用:9.2.2反应条件影响的探究(课后)-2019苏教版必修2课前课中课后
9.2.2反应条件影响的探究(课后)-2019苏教版必修2课前课中课后上海市黄浦区格致中学2020-2021学年高二上学期期末化学试题(已下线)第13讲 铁的氧化物和铁的氢氧化物-【暑假自学课】2023年新高一化学暑假精品课(鲁科版2019必修第一册)
19-20高一下·湖北·期中
解题方法
8 . 《我在故宫修文物》展示了专家精湛的技艺和对传统文化的热爱与坚守,也令人体会到化学方法在文物保护中的巨大作用,某博物馆修复出土铁器的过程如下:
(1)检测锈蚀产物
铁器在具有 、
、_____ 等环境中容易被腐蚀。
(2)分析腐蚀原理:一般认为,铁经过了如下腐蚀循环。
Ⅰ. 转化为
转化为 。
。
Ⅱ. 在自然环境中形成
在自然环境中形成 ,该物质中铁元素的化合价为
,该物质中铁元素的化合价为_______ 。
Ⅲ. 和
和 反应形成致密的
反应形成致密的 保护层,
保护层, 的作用是
的作用是_______ 。
a.氧化剂 b.还原剂 c.既不是氧化剂也不是还原剂
Ⅳ. 保护层被氧化为
保护层被氧化为 ,如此往复腐蚀,
,如此往复腐蚀,___  +
+___  +
+___ 

____  (将反应补充完整)
(将反应补充完整)
(3)研究发现,Cl-对铁的腐蚀会造成严重影响。化学修复:脱氯、还原,形成 保护层,方法如下: 将铁器浸没在盛有
保护层,方法如下: 将铁器浸没在盛有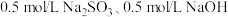 溶液的容器中,缓慢加热至 60~90℃。一段时间, 取出器物,用
溶液的容器中,缓慢加热至 60~90℃。一段时间, 取出器物,用 溶液洗涤至无Cl-。
溶液洗涤至无Cl-。
①检测洗涤液中 Cl-的方法是_____ 。
②脱氯反应: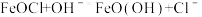 。离子反应的本质是离子浓度的减小,比较
。离子反应的本质是离子浓度的减小,比较 与
与 溶解度的大小:
溶解度的大小:__________ 较大。[填 与
与 ]
]
(1)检测锈蚀产物
| 主要成分的化学式 | |||
 |  |  |  |
铁器在具有
 、
、(2)分析腐蚀原理:一般认为,铁经过了如下腐蚀循环。
Ⅰ.
 转化为
转化为 。
。Ⅱ.
 在自然环境中形成
在自然环境中形成 ,该物质中铁元素的化合价为
,该物质中铁元素的化合价为Ⅲ.
 和
和 反应形成致密的
反应形成致密的 保护层,
保护层, 的作用是
的作用是a.氧化剂 b.还原剂 c.既不是氧化剂也不是还原剂
Ⅳ.
 保护层被氧化为
保护层被氧化为 ,如此往复腐蚀,
,如此往复腐蚀, +
+ +
+

 (将反应补充完整)
(将反应补充完整)(3)研究发现,Cl-对铁的腐蚀会造成严重影响。化学修复:脱氯、还原,形成
 保护层,方法如下: 将铁器浸没在盛有
保护层,方法如下: 将铁器浸没在盛有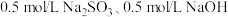 溶液的容器中,缓慢加热至 60~90℃。一段时间, 取出器物,用
溶液的容器中,缓慢加热至 60~90℃。一段时间, 取出器物,用 溶液洗涤至无Cl-。
溶液洗涤至无Cl-。①检测洗涤液中 Cl-的方法是
②脱氯反应:
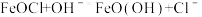 。离子反应的本质是离子浓度的减小,比较
。离子反应的本质是离子浓度的减小,比较 与
与 溶解度的大小:
溶解度的大小: 与
与 ]
]
您最近一年使用:0次
9 . 钠和铁是两种重要的金属。请回答:
(1)切开的金属钠暴露在空气中,最先发生的化学方程式是____ ,将钠投入水中后,钠熔化成一个小球,根据这一现象得出金属钠的物理性质是_______ ,钠与水反应的离子方程式为____ 。
(2)Fe与Cl2在一定条件下反应,所得产物的化学式是____ 。将该产物溶于水配成溶液,分装在两支试管中。请回答:若向其中一支试管中滴加KSCN溶液,则溶液变成____ 色。向另一支试管中滴加NaOH溶液,反应的离子方程式是____ 。
(1)切开的金属钠暴露在空气中,最先发生的化学方程式是
(2)Fe与Cl2在一定条件下反应,所得产物的化学式是
您最近一年使用:0次



