1 . 三草酸合铁酸钾晶体K3[Fe(C2O4)3]·3H2O(M=491g/mol)是一种感光剂和高效的污水处理剂。
I.某研究小组同学查阅资料发现K3[Fe(C2O4)3]·3H2O加热后会分解产生CO和CO2,于是设计了如下实验进行验证。请回答:
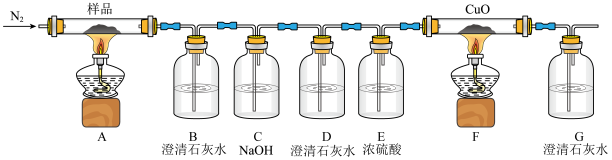
(1)C中NaOH溶液的作用为___________ ;D中澄清石灰水作用为___________ 。
(2)证明有CO产生的现象为___________ 。
(3)该装置还存在的缺陷是___________ 。
II.制备K3[Fe(C2O4)3]·3H2O的途径如下,请回答下列问题:
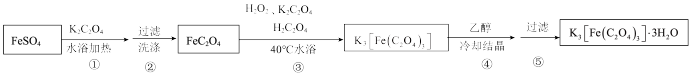
研究小组通过查阅资料得知:
a.K3[Fe(C2O4)3]·3H2O对光敏感,易溶于水,难溶于乙醇;
b.很多草酸盐(例如CaC2O4、BaC2O4)难溶于水,但能溶解于稀硝酸。
(4)步骤③中,控制水浴温度不能超过40℃的原因为___________ 。
(5)研究小组的同学对K3[Fe(C2O4)3]组成有两种看法,分别为:
甲同学:K3[Fe(C2O4)3]由K+、Fe3+、 构成;
构成;
乙同学:K3[Fe(C2O4)3]由K+、[Fe(C2O4)3]3-构成。
请设计实验,验证哪位同学的说法是正确的:___________ 。
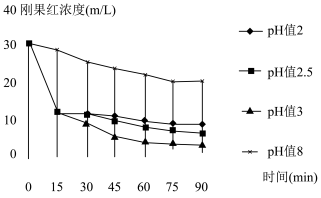
(6)K3[Fe(C2O4)3]联合H2O2体系可用于降解染料,一定浓度的该混合溶液,在不同pH条件下降解刚果红的效率如图所示,在实际应用过程中,应选择pH=___________ 。
(7)关于制备流程,下列说法正确的是___________。
(8)制得的K3[Fe(C2O4)3]·3H2O含少量FeC2O4·2H2O,为测定其纯度,进行如下实验:
步骤I:称取5.000g三草酸合铁酸钾晶体,配制成1.000L溶液,固体完全溶解。
步骤II:取20.00mL溶液,与0.1000molL-酸性KMnO4溶液反应,消耗2.46mL。
步骤III:另取20.00mL溶液,加入过量铜粉,过滤,洗涤,将滤液和洗涤液合并。
步骤IV:将合并液与0.1000mol/L酸性KMnO4溶液反应,消耗2.86mL。
已知 与
与 的反应为(未配平):
的反应为(未配平): +
+ +H+→CO2↑+Mn2++H2O
+H+→CO2↑+Mn2++H2O
①写出Fe2+与酸性KMnO4溶液反应的离子方程式:___________ 。
②研究小组制得的K3[Fe(C2O4)3]·3H2O纯度为___________ 。
I.某研究小组同学查阅资料发现K3[Fe(C2O4)3]·3H2O加热后会分解产生CO和CO2,于是设计了如下实验进行验证。请回答:

(1)C中NaOH溶液的作用为
(2)证明有CO产生的现象为
(3)该装置还存在的缺陷是
II.制备K3[Fe(C2O4)3]·3H2O的途径如下,请回答下列问题:

研究小组通过查阅资料得知:
a.K3[Fe(C2O4)3]·3H2O对光敏感,易溶于水,难溶于乙醇;
b.很多草酸盐(例如CaC2O4、BaC2O4)难溶于水,但能溶解于稀硝酸。
(4)步骤③中,控制水浴温度不能超过40℃的原因为
(5)研究小组的同学对K3[Fe(C2O4)3]组成有两种看法,分别为:
甲同学:K3[Fe(C2O4)3]由K+、Fe3+、
 构成;
构成;乙同学:K3[Fe(C2O4)3]由K+、[Fe(C2O4)3]3-构成。
请设计实验,验证哪位同学的说法是正确的:
(6)K3[Fe(C2O4)3]联合H2O2体系可用于降解染料,一定浓度的该混合溶液,在不同pH条件下降解刚果红的效率如图所示,在实际应用过程中,应选择pH=

(7)关于制备流程,下列说法正确的是___________。
| A.步骤①为复分解反应,步骤③为氧化还原反应 |
| B.步骤②判断沉淀是否洗涤干净,可以取少量最后一次洗涤液,加入氯化钡溶液,观察是否有白色沉淀产生 |
| C.步骤④,加入乙醇目的在于降低K3[Fe(C2O4)3]的溶解度,使其结晶析出 |
| D.步骤④⑤可以在日光下进行 |
(8)制得的K3[Fe(C2O4)3]·3H2O含少量FeC2O4·2H2O,为测定其纯度,进行如下实验:
步骤I:称取5.000g三草酸合铁酸钾晶体,配制成1.000L溶液,固体完全溶解。
步骤II:取20.00mL溶液,与0.1000molL-酸性KMnO4溶液反应,消耗2.46mL。
步骤III:另取20.00mL溶液,加入过量铜粉,过滤,洗涤,将滤液和洗涤液合并。
步骤IV:将合并液与0.1000mol/L酸性KMnO4溶液反应,消耗2.86mL。
已知
 与
与 的反应为(未配平):
的反应为(未配平): +
+ +H+→CO2↑+Mn2++H2O
+H+→CO2↑+Mn2++H2O①写出Fe2+与酸性KMnO4溶液反应的离子方程式:
②研究小组制得的K3[Fe(C2O4)3]·3H2O纯度为
您最近一年使用:0次
20-21高一上·山东·单元测试
解题方法
2 . 下列说法正确的是( )
| A.向NaClO溶液中滴入少量FeSO4溶液,反应的离子方程式为3H2O+3ClO-+6Fe2+=2Fe(OH)3↓+4Fe3++3Cl- |
| B.向FeSO4溶液中先滴入KSCN溶液,再滴加H2O2溶液,溶液变红色,说明Fe2+既有氧化性又有还原性 |
| C.向某溶液中滴加氯水后再加入KSCN溶液,若溶液呈红色,则溶液中一定含有Fe2+ |
| D.在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+ |
您最近一年使用:0次
3 . 某校化学小组学生利用如图所列装置进行“铁与水反应”的实验,并利用产物进一步制取FeCl3•6H2O晶体.(图中夹持及尾气处理装置均已略去)
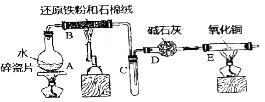
(1)装置B中发生反应的化学方程式是________ ;
(2)装置E中的现象是________ ;
(3)该小组把B中反应后的产物加入足量的盐酸,用该溶液制取FeCl3•6H2O晶体.
①欲检验溶液里含有Fe3+,选用的试剂为________ ,现象是________ ;
②该实验小组同学用上述试剂没有检验到Fe3+,用离子方程式解释滤液中不存在Fe3+可能的原因________ ;
③将此溶液中FeCl2完全氧化为FeCl3,最好选择下列物质中的________
④在③所得溶液浓缩结晶前需要用实验证明FeCl2已完全氧化,实验方法是________ 。

(1)装置B中发生反应的化学方程式是
(2)装置E中的现象是
(3)该小组把B中反应后的产物加入足量的盐酸,用该溶液制取FeCl3•6H2O晶体.
①欲检验溶液里含有Fe3+,选用的试剂为
②该实验小组同学用上述试剂没有检验到Fe3+,用离子方程式解释滤液中不存在Fe3+可能的原因
③将此溶液中FeCl2完全氧化为FeCl3,最好选择下列物质中的
| A.酸性KMnO4溶液 | B.Cl2 | C.Na2O2 | D.FeCl3 |
您最近一年使用:0次
2016-12-09更新
|
425次组卷
|
3卷引用:2015-2016学年山西省怀仁一中高一下第一次月考化学试卷
2015-2016学年山西省怀仁一中高一下第一次月考化学试卷(已下线)第三章 章末检测(1)——《高中新教材同步备课》(人教版 必修第一册)安徽省池州市第一中学2020-2021学年高一12月月考化学试题
名校
4 . 为确定 和
和 混合物的组成(假设混合均匀),某兴趣小组称取五份不同质量的样品,分别投入
混合物的组成(假设混合均匀),某兴趣小组称取五份不同质量的样品,分别投入 某浓度的稀硫酸中。充分反应后,每组样品剩余固体的质量与原样品质量的关系如图所示。下列说法不正确的是
某浓度的稀硫酸中。充分反应后,每组样品剩余固体的质量与原样品质量的关系如图所示。下列说法不正确的是

 和
和 混合物的组成(假设混合均匀),某兴趣小组称取五份不同质量的样品,分别投入
混合物的组成(假设混合均匀),某兴趣小组称取五份不同质量的样品,分别投入 某浓度的稀硫酸中。充分反应后,每组样品剩余固体的质量与原样品质量的关系如图所示。下列说法不正确的是
某浓度的稀硫酸中。充分反应后,每组样品剩余固体的质量与原样品质量的关系如图所示。下列说法不正确的是
A.各组样品均发生反应: 、 、 |
B.a、e两组样品分别充分反应后,溶液中一定存在 和 和 ,一定不存在 ,一定不存在 |
C.该混合物中,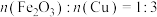 |
D.稀硫酸的浓度为 |
您最近一年使用:0次
2024-02-20更新
|
192次组卷
|
2卷引用:吉林省长春市东北师大附中2023-2024学年高一上学期期末考试化学试题
名校
5 . 已知A、B、C、D为原子序数依次增大的短周期主族元素,A与D同主族,B与C同周期,且C与D的原子序数之和为20。E为地壳中含量最高的过渡元素。甲、乙分别为元素E、A的单质,丙、丁为A、E分别与B形成的二元化合物,它们之间的转化关系如图(反应条件已略去)。下列说法错误的是
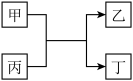

| A.A、B形成的一种化合物具有漂白性 |
| B.D的离子半径小于C的离子半径 |
| C.C的单质能与丙反应置换出B的单质 |
| D.将反应后的固体混合物溶于稀盐酸中,再滴加KSCN溶液,溶液一定呈红色 |
您最近一年使用:0次
2023-05-15更新
|
912次组卷
|
4卷引用: 重庆市第一中学校2022-2023学年高一下学期期中考试化学试题
名校
6 . 同一还原剂与多种氧化剂在一起时,先与氧化性强的粒子反应,待强的反应完后,再与氧化性弱的反应,称为反应先后规律。已知 ,且氧化性:
,且氧化性: ,在溶有
,在溶有 和
和 的溶液中加入铁粉,下列说法中正确的是
的溶液中加入铁粉,下列说法中正确的是
 ,且氧化性:
,且氧化性: ,在溶有
,在溶有 和
和 的溶液中加入铁粉,下列说法中正确的是
的溶液中加入铁粉,下列说法中正确的是A.若铁粉无剩余,且溶液中有 ,则溶液中一定无 ,则溶液中一定无 |
B.若铁粉无剩余,且溶液中无 ,则溶液中一定有 ,则溶液中一定有 ,也可能有 ,也可能有 |
| C.若铁粉有剩余,则不溶物中一定有铜 |
D.若铁粉有剩余,则溶液中的金属阳离子有 和 和 |
您最近一年使用:0次
2022-01-16更新
|
1670次组卷
|
6卷引用:河南省南阳市2021-2022学年高一上学期期末考试化学试题
名校
解题方法
7 . 已知:还原性 ,某溶液中含有等物质的量的
,某溶液中含有等物质的量的 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的几种离子,为了确定其组成,某同学进行了如下实验:
中的几种离子,为了确定其组成,某同学进行了如下实验:
①取少量溶液,滴入酸性高锰酸钾溶液,发现高锰酸钾溶液褪色
②取①中溶液,加入KSCN溶液,溶液呈红色;加入氢氧化钠固体并加热,产生能使湿润的红色石蕊试纸变蓝的气体
③取少量溶液,加入足量盐酸酸化的氯化钡溶液,产生白色沉淀
下列说法不正确的是
 ,某溶液中含有等物质的量的
,某溶液中含有等物质的量的 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的几种离子,为了确定其组成,某同学进行了如下实验:
中的几种离子,为了确定其组成,某同学进行了如下实验:①取少量溶液,滴入酸性高锰酸钾溶液,发现高锰酸钾溶液褪色
②取①中溶液,加入KSCN溶液,溶液呈红色;加入氢氧化钠固体并加热,产生能使湿润的红色石蕊试纸变蓝的气体
③取少量溶液,加入足量盐酸酸化的氯化钡溶液,产生白色沉淀
下列说法不正确的是
A.溶液中肯定存在 、 、 、 、 |
B.溶液中不可能同时存在 、 、 |
C.溶液中可能同时存在 、 、 |
D.溶液中可能存在 、 、 |
您最近一年使用:0次
2022-06-26更新
|
1324次组卷
|
5卷引用:浙江省宁波市九校2021-2022学年高一下学期6月联考化学试题
名校
解题方法
8 . 常温时,将0.1 mol Fe(NO3)3和2 mol HCl溶于水得2 L混合溶液,然后向该溶液投入m g铁粉使其充分反应后,滴加KSCN溶液不变红色。下列有关说法正确的是( )
| A.由于氧化性Fe3+>H+,首先发生的反应是:Fe+2Fe3+=3Fe2+ |
| B.当加入16.8 g铁粉时,可生成标准状况下6.72 L气体 |
| C.在铁粉充分反应后的溶液中,铁元素以Fe2+和Fe3+的形式存在 |
| D.m≥28,反应过程中溶液的质量一直在减小 |
您最近一年使用:0次
2020-08-15更新
|
415次组卷
|
8卷引用:2015届山东省青岛市高三下学期第二次模拟考试理综化学试卷
2015届山东省青岛市高三下学期第二次模拟考试理综化学试卷(已下线)2019年8月5日《每日一题》2020年高考一轮复习—— Fe2+、Fe3+的检验(已下线)专题3.3 铁及其重要化合物(练)——2020年高考化学一轮复习讲练测(已下线)第11讲 铁及其重要化合物(精练)——2021年高考化学一轮复习讲练测(已下线)考点15 铁及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点15 铁及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第07讲 铁及其化合物(练)-2023年高考化学一轮复习讲练测(新教材新高考)江西省丰城中学2023-2024学年高一上学期12月月考化学试题
名校
解题方法
9 . 向一定量的Fe、Fe2O3和CuO混合物投入100mL 0.9mol/L的硫酸溶液中,充分反应后生成448mL标准状况下的气体,得不溶物0.03mol。向滤液中加入2mol/L的NaOH溶液,加至10mL时开始出现沉淀。忽略溶液的体积变化,下列说法不正确的
| A.0.03mol不溶物全为Cu | B.混合物中氧原子的物质的量为0.05mol |
| C.滤液中的阳离子只有两种 | D.滤液中的Fe2+的物质的量浓度为0.8mol/L |
您最近一年使用:0次
2021-02-02更新
|
1403次组卷
|
8卷引用:湖北省沙市中学2020-2021学年高一上学期期末考试化学试题
湖北省沙市中学2020-2021学年高一上学期期末考试化学试题(已下线)专题讲座(一) 化学计算的常用方法(精练)-2022年高考化学一轮复习讲练测(已下线)3.1.2 不同价态铁元素之间的转化-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)江西省景德镇一中2022-2023学年高一上学期期中考试(19班)化学试题湖北省武汉市第六中学2021-2022学年高一上学期12月月考化学试题重庆市南开中学2022-2023学年高一上学期12月定时练习化学试题湖南省邵阳市第二中学2023-2024学年高一下学期第一次月考化学试题福建师范大学附属中学2021-2022学年高一下学期期末考试化学试题
名校
10 . 某试样含有的阳离子为NH4+、Ag+、Ba2+、Cu2+、Fe2+中的若干种,为确定其组成,某同学进行了如下实验,下列说法不正确的是
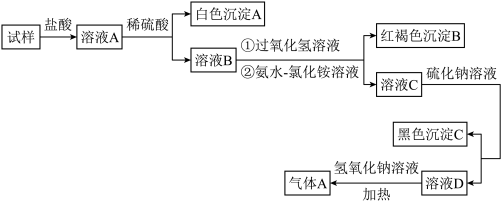
注:①CuS为难溶于水的黑色固体;②气体A能使湿润的红色石蕊试纸变蓝。

注:①CuS为难溶于水的黑色固体;②气体A能使湿润的红色石蕊试纸变蓝。
| A.沉淀A为BaSO4 |
| B.加入过氧化氢溶液时发生的反应:2Fe2++H2O2+2H+=2Fe3++2H2O |
| C.加入氨水-氯化铵溶液可使Fe3+沉淀完全,而Cu2+不形成沉淀 |
| D.试样中一定含NH4+、Ba2+、Cu2+、Fe2+,一定不含Ag+ |
您最近一年使用:0次



