名校
1 . 物质的性质决定用途。下列两者对应关系不正确的是
A. 能吸收 能吸收 产生 产生 ,可用作呼吸面具供氧剂 ,可用作呼吸面具供氧剂 |
B. 溶液呈酸性,可用于腐蚀电路板上的 溶液呈酸性,可用于腐蚀电路板上的 |
C. 具有还原性,可用作抗氧化剂 具有还原性,可用作抗氧化剂 |
| D.液氨汽化需要吸收大量的热,可用作制冷剂 |
您最近一年使用:0次
名校
2 . 下列物质的性质与用途不具有对应关系是
| A.CO具有还原性,可用于冶炼铁 | B.KNO3具有氧化性,可用于制黑火药 |
| C.Na2CO3溶液显碱性,可用于除油污 | D.FeCl3溶液显酸性,可用于刻蚀电路板上的铜 |
您最近一年使用:0次
名校
3 . 下列有关物质的性质与用途具有对应关系的是( )
| A.Mg(OH)2具有碱性,可用于制胃酸中和剂 |
| B.H2O2是无色液体,可用作消毒剂 |
| C.FeCl3具有氧化性,可用作净水剂 |
| D.液NH3具有碱性,可用作制冷剂 |
您最近一年使用:0次
2020-01-13更新
|
261次组卷
|
4卷引用:重庆市2023届高三上学期11月质量检测化学试题
名校
解题方法
4 . SO2是硫元素中一种重要物质。在生产生活中有着重要用途。
(1)某研究小组用如图装置进行SO2与FeCl3溶液反应的相关实验(夹持装置已略去)。_____ 。根据以上现象,该小组同学认为SO2与FeCl3溶液发生氧化还原反应。
a.请设计实验方案检验溶液中是否还有Fe3+:_____ 。
b.该小组同学向C试管反应后的溶液中先加入稀硝酸,后加入BaCl2溶液,发现出现白色沉淀,即可证明反应生成了SO 。该做法
。该做法_____ (填“合理”或“不合理”),理由是_____ 。
②为了验证SO2具有还原性,实验中可以代替FeCl3溶液的试剂有_____ (填字母)。
A.浓硫酸 B.酸性KMnO4溶液 C.碘水 D.NaCl溶液
(2)某同学利用如图所示的装置研究SO2的性质:(已知熔点:SO2:-76.1℃,SO3:16.8℃,沸点:SO2:-10℃,SO3:45℃)_____ 。
②乙同学按Ⅰ、Ⅱ、III顺序连接装置,发现装置III溶液褪色,出现该现象的原因是_____ (用离子方程式表示)。
③乙同学按Ⅰ、Ⅱ、Ⅳ顺序连接装置,若装置Ⅳ中有50mL2.5mol·L-1NaOH溶液,反应后增重4.8g,则装置Ⅳ中发生反应的化学方程式是_____ 。
(1)某研究小组用如图装置进行SO2与FeCl3溶液反应的相关实验(夹持装置已略去)。
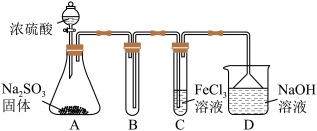
a.请设计实验方案检验溶液中是否还有Fe3+:
b.该小组同学向C试管反应后的溶液中先加入稀硝酸,后加入BaCl2溶液,发现出现白色沉淀,即可证明反应生成了SO
 。该做法
。该做法②为了验证SO2具有还原性,实验中可以代替FeCl3溶液的试剂有
A.浓硫酸 B.酸性KMnO4溶液 C.碘水 D.NaCl溶液
(2)某同学利用如图所示的装置研究SO2的性质:(已知熔点:SO2:-76.1℃,SO3:16.8℃,沸点:SO2:-10℃,SO3:45℃)
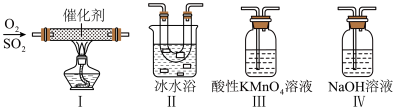
②乙同学按Ⅰ、Ⅱ、III顺序连接装置,发现装置III溶液褪色,出现该现象的原因是
③乙同学按Ⅰ、Ⅱ、Ⅳ顺序连接装置,若装置Ⅳ中有50mL2.5mol·L-1NaOH溶液,反应后增重4.8g,则装置Ⅳ中发生反应的化学方程式是
您最近一年使用:0次
2024-04-03更新
|
271次组卷
|
2卷引用:重庆市万州第二高级中学2023-2024学年高一下学期3月月考试题 化学试题
5 . 金属及其化合物在生产中用途广泛。
I.利用生产硼砂的废渣一一确镁泥(主要成分为MgCO3.SiO2,还含有少量Fe2O3、MnO、CaO等)为主要原料制取轻质碳酸镁[MgCO3:Mg(OH)2:2H2O]的工业流程如下:
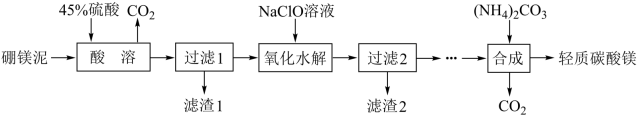
(1)写出“酸溶"一步中,MgCO3和硫酸反应的离子方程式_____________ 。
(2)滤渣2的主要成分有MnO2和____ ,写出生成MnO2的离子方程式__________ 。
(3)“合成”时需通蒸汽至80℃,边加热边搅拌,温度不能超80℃的原因是______________ 。
II.从含铜丰富的自然资源黄铜矿(CuFeS2)冶炼铜的工艺流程如下:
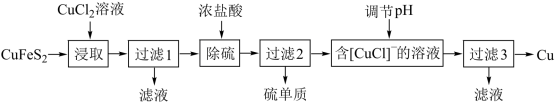
已知:①CuFeS2+3CuCl2=4CuCl↓+FeCl2+2S↓ ②+1价的Cu在酸性条件下易歧化
(4)浸取时,若改用FeCl3溶液,也能生成CuCl和S,该反应化学方程式为________ 。
(5)若过滤1所得滤液中只含FeCl2,则将其在空气中加热蒸干、灼烧后,所得固体的化学式为______ 。
(6)调节溶液的pH后,除生成Cu外,还能产生一种金属离子,此金属离子是______ 。(填离子符号)
(7)过滤3所得滤液中的CuCl2可循环使用,为保持流程持续循环,每生成1molCu,理论上需补充CuCl2的物质的量为_________ 。
I.利用生产硼砂的废渣一一确镁泥(主要成分为MgCO3.SiO2,还含有少量Fe2O3、MnO、CaO等)为主要原料制取轻质碳酸镁[MgCO3:Mg(OH)2:2H2O]的工业流程如下:

(1)写出“酸溶"一步中,MgCO3和硫酸反应的离子方程式
(2)滤渣2的主要成分有MnO2和
(3)“合成”时需通蒸汽至80℃,边加热边搅拌,温度不能超80℃的原因是
II.从含铜丰富的自然资源黄铜矿(CuFeS2)冶炼铜的工艺流程如下:

已知:①CuFeS2+3CuCl2=4CuCl↓+FeCl2+2S↓ ②+1价的Cu在酸性条件下易歧化
(4)浸取时,若改用FeCl3溶液,也能生成CuCl和S,该反应化学方程式为
(5)若过滤1所得滤液中只含FeCl2,则将其在空气中加热蒸干、灼烧后,所得固体的化学式为
(6)调节溶液的pH后,除生成Cu外,还能产生一种金属离子,此金属离子是
(7)过滤3所得滤液中的CuCl2可循环使用,为保持流程持续循环,每生成1molCu,理论上需补充CuCl2的物质的量为
您最近一年使用:0次
2017-10-12更新
|
406次组卷
|
2卷引用:重庆市第一中学2018届高三上学期第一次月考(9月)化学试题



