名校
解题方法
1 . 由硫铁矿烧渣(主要含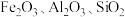 )制取绿矾
)制取绿矾 的流程如下:
的流程如下:
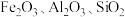 )制取绿矾
)制取绿矾 的流程如下:
的流程如下: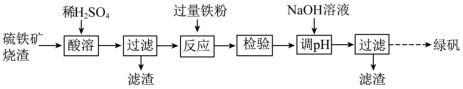
A.“检验”时可用 溶液检验上一步“反应”是否进行完全 溶液检验上一步“反应”是否进行完全 |
| B.将第二次“过滤”所得滤液加热,经蒸发结晶可以制得绿矾 |
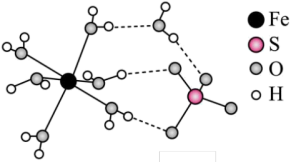
C.绿矶中 为配体,中心离子的配位数为7 为配体,中心离子的配位数为7 |
| D.绿矾中存在共价键、配位键、氢键、离子键 |
您最近一年使用:0次
名校
2 .  的配位化合物较稳定且用运广泛。
的配位化合物较稳定且用运广泛。 可与
可与 、
、 、
、 等配体形成溶液呈浅紫色的
等配体形成溶液呈浅紫色的 、红色的
、红色的 、无色的
、无色的 配离子。某同学按如下步骤完成实验:
配离子。某同学按如下步骤完成实验: 的溶液中加入KSCN溶液生成蓝色的
的溶液中加入KSCN溶液生成蓝色的 的配离子,
的配离子, 不能与
不能与 形成配位离子。下列说法错误的是
形成配位离子。下列说法错误的是
 的配位化合物较稳定且用运广泛。
的配位化合物较稳定且用运广泛。 可与
可与 、
、 、
、 等配体形成溶液呈浅紫色的
等配体形成溶液呈浅紫色的 、红色的
、红色的 、无色的
、无色的 配离子。某同学按如下步骤完成实验:
配离子。某同学按如下步骤完成实验: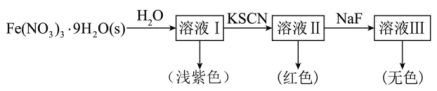
 的溶液中加入KSCN溶液生成蓝色的
的溶液中加入KSCN溶液生成蓝色的 的配离子,
的配离子, 不能与
不能与 形成配位离子。下列说法错误的是
形成配位离子。下列说法错误的是| A.Fe晶体中原子通过金属阳离子和自由电子间的静电作用相结合 |
B.可用NaF和KSCN溶液检验 溶液中是否含有 溶液中是否含有 |
C.溶液Ⅰ中 仅参与形成范德华力和氢键 仅参与形成范德华力和氢键 |
D.上述实验可得出,与 形成配合物的能力: 形成配合物的能力: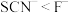 |
您最近一年使用:0次
2024-04-22更新
|
228次组卷
|
3卷引用:福建省宁德市福安市第一中学2023-2024学年高二下学期3月月考化学试题
名校
解题方法
3 . 下列实验方案能达到探究目的的是
| 选项 | 探究目的 | 实验方案 |
| A | CO还原Fe2O3实验中,Fe2O3是否全部被还原 | 向CO还原Fe2O3所得到的产物中加入稀盐酸,再滴加KSCN溶液,观察颜色变化 |
| B | 比较CH3COO-和ClO-结合H+的能力大小 | 室温下,用pH计分别测定等物质的量浓度的CH3COONa溶液和NaClO溶液的pH |
| C | 比较Ksp(BaSO4)和Ksp(BaCO3)的相对大小 | 将BaSO4粉末和Na2CO3饱和溶液混合,充分振荡,静置,取少量上层清液,滴加盐酸和BaCl2溶液,观察是否有沉淀产生 |
| D | 蔗糖水解产物是否具有还原性 | 向蔗糖溶液中加入少量稀硫酸,加热煮沸,冷却后加入银氨溶液,水浴加热,观察现象 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-17更新
|
1478次组卷
|
4卷引用:江西省宜春市宜丰中学2023-2024学年高二下学期3月月考化学试题
江西省宜春市宜丰中学2023-2024学年高二下学期3月月考化学试题江苏省南京市盐城市2024届高三一模考试化学试题(已下线)通关练03 常考化学实验基础知识-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)(已下线)题型6 元素及其化合物 化学实验基础(25题)-2024年高考化学常考点必杀300题(新高考通用)
名校
解题方法
4 . 某实验小组同学用KSCN探究久置FeSO4固体变质的情况。将0.3gFeSO4固体用10mL蒸馏水溶解,配成待测液,进行实验。
【初步实验】
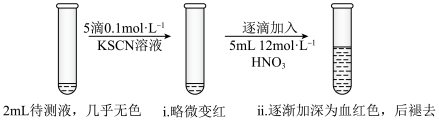
(1)用KSCN检验Fe3+的原理是___________ (用离子方程式表示)。
(2)甲同学认为FeSO4固体几乎未变质,ⅱ中变血红色是由于Fe2+被___________ (填化学式)氧化。结合平衡移动原理解释ⅱ中血红色褪去的可能原因___________ 。
(3)乙同学不认同甲对现象的解释,他推测加入浓硝酸后ⅱ中变血红色还可能与其它因素有关,可能的影响因素是___________ 。
为验证该猜测,乙同学继续进行了以下实验。【继续探究】
(4)请补全步骤Ⅱ中的操作:___________ 。
(5)由Ⅰ~Ⅲ推测FeSO4固体变质的情况是___________ (填字母序号)。
a.几乎未变质 b.部分变质 c.完全变质
【反思与迁移】
(6)从上述探究中获得启发,在用KSCN检验Fe3+及进行Fe2+还原性验证实验时,需要注意的事项有___________ (至少2条)。
【初步实验】

(1)用KSCN检验Fe3+的原理是
(2)甲同学认为FeSO4固体几乎未变质,ⅱ中变血红色是由于Fe2+被
(3)乙同学不认同甲对现象的解释,他推测加入浓硝酸后ⅱ中变血红色还可能与其它因素有关,可能的影响因素是
为验证该猜测,乙同学继续进行了以下实验。【继续探究】
| 步骤 | 操作 | 现象 |
| Ⅰ | 取2mL待测液,加入5滴0.1mol·L-1KSCN溶液,再加入5mL浓KNO3溶液 | 溶液无明显变化 |
| Ⅱ | 取2mL待测液,加入5滴0.1mol·L-1KSCN溶液,___________ | 溶液变为红色 |
| Ⅲ | 向Ⅱ中所得溶液中逐滴加入浓硝酸,边加边振荡 | 溶液逐渐加深为血红色,继续滴加浓硝酸,溶液褪色,pH变化始终不明显 |
(4)请补全步骤Ⅱ中的操作:
(5)由Ⅰ~Ⅲ推测FeSO4固体变质的情况是
a.几乎未变质 b.部分变质 c.完全变质
【反思与迁移】
(6)从上述探究中获得启发,在用KSCN检验Fe3+及进行Fe2+还原性验证实验时,需要注意的事项有
您最近一年使用:0次
名校
解题方法
5 . 某实验小组为探究 和
和 的氧化能力设计如下实验.
的氧化能力设计如下实验.
Ⅰ.探究 和
和 氧化
氧化 的速率向体积均为
的速率向体积均为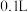 、浓度均为
、浓度均为 的
的 溶液和
溶液和 溶液中加入表面积相同、质量相等的铜片,反应一段时间后,经检验,
溶液中加入表面积相同、质量相等的铜片,反应一段时间后,经检验, 已完全消耗,
已完全消耗, 还有剩余.该小组同学猜测
还有剩余.该小组同学猜测 和
和 的氧化能力:
的氧化能力: .
.
(1)检验溶液中还有 剩余的试剂为
剩余的试剂为___________ 。
(2)相较于 溶液,
溶液, 溶液和铜反应速率较快的原因为
溶液和铜反应速率较快的原因为______________________________ 。
Ⅱ.探究反应 为可逆反应 将浓度均为
为可逆反应 将浓度均为 的
的 溶液和
溶液和 溶液等体积混合,一段时间后,溶液变为黄色,且有灰黑色沉淀生成.
溶液等体积混合,一段时间后,溶液变为黄色,且有灰黑色沉淀生成.
(3)若要证明该反应为可逆反应,只需用 溶液检测出有
溶液检测出有 的存在即可,写出该检测反应的离子方程式
的存在即可,写出该检测反应的离子方程式_________________________ 。
Ⅲ.测定反应 的平衡常数
的平衡常数
取 中上层清液,用
中上层清液,用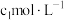 酸性
酸性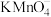 溶液滴定上层清液中剩余的
溶液滴定上层清液中剩余的 ,并记录滴定终点所消耗的酸性
,并记录滴定终点所消耗的酸性 溶液的体积;重复滴定3次,平均消耗酸性
溶液的体积;重复滴定3次,平均消耗酸性 溶液的体积为
溶液的体积为 .
.
(4)滴定至接近终点时,控制标准溶液半滴滴入,其操作是用锥形瓶口内壁轻靠滴定管尖嘴悬挂的液滴.要使这半滴液体流入锥形瓶内的操作是___________ ;滴定终点时的现象为___________ 。
(5)平衡时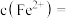
___________ (用含V、 、
、 的代数式表示),由此可计算出反应的平衡常数K.若盛装酸性
的代数式表示),由此可计算出反应的平衡常数K.若盛装酸性 溶液的滴定管未润洗,则计算得到的K值
溶液的滴定管未润洗,则计算得到的K值___________ (填“偏大”“偏小”或“不影响”)。
 和
和 的氧化能力设计如下实验.
的氧化能力设计如下实验.Ⅰ.探究
 和
和 氧化
氧化 的速率向体积均为
的速率向体积均为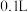 、浓度均为
、浓度均为 的
的 溶液和
溶液和 溶液中加入表面积相同、质量相等的铜片,反应一段时间后,经检验,
溶液中加入表面积相同、质量相等的铜片,反应一段时间后,经检验, 已完全消耗,
已完全消耗, 还有剩余.该小组同学猜测
还有剩余.该小组同学猜测 和
和 的氧化能力:
的氧化能力: .
.(1)检验溶液中还有
 剩余的试剂为
剩余的试剂为(2)相较于
 溶液,
溶液, 溶液和铜反应速率较快的原因为
溶液和铜反应速率较快的原因为Ⅱ.探究反应
 为可逆反应 将浓度均为
为可逆反应 将浓度均为 的
的 溶液和
溶液和 溶液等体积混合,一段时间后,溶液变为黄色,且有灰黑色沉淀生成.
溶液等体积混合,一段时间后,溶液变为黄色,且有灰黑色沉淀生成.(3)若要证明该反应为可逆反应,只需用
 溶液检测出有
溶液检测出有 的存在即可,写出该检测反应的离子方程式
的存在即可,写出该检测反应的离子方程式Ⅲ.测定反应
 的平衡常数
的平衡常数 取
 中上层清液,用
中上层清液,用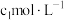 酸性
酸性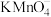 溶液滴定上层清液中剩余的
溶液滴定上层清液中剩余的 ,并记录滴定终点所消耗的酸性
,并记录滴定终点所消耗的酸性 溶液的体积;重复滴定3次,平均消耗酸性
溶液的体积;重复滴定3次,平均消耗酸性 溶液的体积为
溶液的体积为 .
.(4)滴定至接近终点时,控制标准溶液半滴滴入,其操作是用锥形瓶口内壁轻靠滴定管尖嘴悬挂的液滴.要使这半滴液体流入锥形瓶内的操作是
(5)平衡时
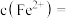
 、
、 的代数式表示),由此可计算出反应的平衡常数K.若盛装酸性
的代数式表示),由此可计算出反应的平衡常数K.若盛装酸性 溶液的滴定管未润洗,则计算得到的K值
溶液的滴定管未润洗,则计算得到的K值
您最近一年使用:0次
名校
解题方法
6 . 常温下,下列各组离子在指定溶液中能大量存在的是
A. 的溶液中: 的溶液中: 、 、 、 、 、 、 |
B.滴入 溶液显红色的溶液中: 溶液显红色的溶液中: 、 、 、 、 、 、 |
C. 的溶液中: 的溶液中: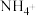 、 、 、 、 、 、 |
D. 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
2024-03-07更新
|
182次组卷
|
2卷引用:云南省昆明市第三中学2023-2024学年高二下学期4月第二次综合测试化学试题
7 . 下列实验操作过程中不会形成配位键的是
A. 溶于 溶于 中形成紫红色的溶液 中形成紫红色的溶液 |
B. 粉末溶于水形成蓝色的溶液 粉末溶于水形成蓝色的溶液 |
C.将硫氰化铵溶液滴加到含 的溶液中检验 的溶液中检验 |
D.向 溶液中加入过量的氨水 溶液中加入过量的氨水 |
您最近一年使用:0次
2024-03-07更新
|
341次组卷
|
4卷引用:辽宁省沈阳市东北育才学校高中部2023-2024学年高二下学期第1次月考化学试题
名校
8 . 常温下,下列各组离子一定能大量共存的是
A.由水电离出的c(H+)=1×10-11 mol/L的溶液中:Mg2+、 、 、 、 、 |
B.在含大量Fe3+的溶液中: 、Na+、Cl-、SCN-、 、Na+、Cl-、SCN-、 |
C.与Al反应能放出H2溶液中: 、Ba2+、Cl-、 、Ba2+、Cl-、 |
D.在Kw/c(H+)=1×10-12 mol/L的溶液中:Na+、K+、Br-、 |
您最近一年使用:0次
名校
解题方法
9 . 室温下,下列各组离子在指定溶液中能大量共存的是
A.pH=2的溶液:Na+、Fe2+、I-、 |
B.c[NaAl(OH)4]=0.1mol·L-1的溶液:K+、H+、Cl-、 |
C.Kw/(H+) =0.1mol·L-1的溶液:Na+、K+、 、ClO- 、ClO- |
D.c(Fe3+)=0.1mol·L-1的溶液:Al3+、 、 、 、SCN- 、SCN- |
您最近一年使用:0次
名校
解题方法
10 . 下列反应对应的离子方程式正确的是
| A.Fe2(SO4)3的酸性溶液中通入足量硫化氢:Fe3++H2S=Fe2++S↓+2H+ |
B.碳酸氢钙溶液中加入过量氢氧化钠溶液:Ca2++2 +2OH-=CaCO3↓+2H2O+ +2OH-=CaCO3↓+2H2O+ |
| C.氯化铝溶液中加入过量氨水:Al3++3OH-=Al(OH)3↓ |
D.用Na2SO3溶液吸收少量Cl2:3 +Cl2+H2O=2 +Cl2+H2O=2 +2Cl-+ +2Cl-+ |
您最近一年使用:0次



