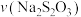解题方法
1 . 高铁酸钠( )是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为
)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为 。下列说法错误的是
。下列说法错误的是
 )是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为
)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为 。下列说法错误的是
。下列说法错误的是A. 中 中 原子的杂化轨道类型为 原子的杂化轨道类型为 |
B.该反应中氧化产物与还原产物的物质的量之比为 |
| C.依据该反应原理,可设计原电池 |
D.完全反应后,可用 溶液检验反应后的溶液中是否存在 溶液检验反应后的溶液中是否存在 |
您最近一年使用:0次
名校
解题方法
2 . 由硫铁矿烧渣(主要含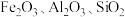 )制取绿矾
)制取绿矾 的流程如下:
的流程如下:
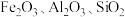 )制取绿矾
)制取绿矾 的流程如下:
的流程如下: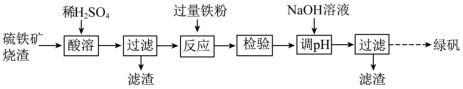
A.“检验”时可用 溶液检验上一步“反应”是否进行完全 溶液检验上一步“反应”是否进行完全 |
| B.将第二次“过滤”所得滤液加热,经蒸发结晶可以制得绿矾 |
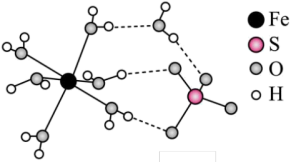
C.绿矶中 为配体,中心离子的配位数为7 为配体,中心离子的配位数为7 |
| D.绿矾中存在共价键、配位键、氢键、离子键 |
您最近一年使用:0次
名校
解题方法
3 . 某研究性学习小组进行某补血剂中铁元素( 价)含量测定的实验,其流程如下:
价)含量测定的实验,其流程如下:不 正确的是
 价)含量测定的实验,其流程如下:
价)含量测定的实验,其流程如下: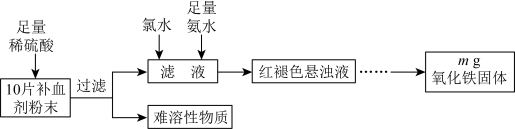
A.向过滤后的滤液中滴加 溶液,溶液可能呈红色 溶液,溶液可能呈红色 |
B.可以用 替代上述流程中的氯水 替代上述流程中的氯水 |
| C.红褐色悬浊液经过滤、洗涤、干燥,得到氧化铁固体 |
D.每片补血剂中铁元素的质量为 |
您最近一年使用:0次
2024-05-06更新
|
210次组卷
|
3卷引用:河南省焦作市博爱县第一中2023-2024学年高二下学期4月期中考试化学试题
解题方法
4 . 实验室用绿矾 制备
制备 的流程如图所示,下列说法错误的是
的流程如图所示,下列说法错误的是
 制备
制备 的流程如图所示,下列说法错误的是
的流程如图所示,下列说法错误的是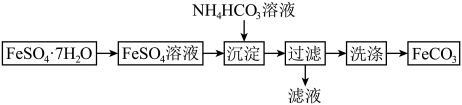
| A.绿矾应隔绝空气密封保存 |
B. 中既含有离子键也含有共价键 中既含有离子键也含有共价键 |
C.可利用 溶液检验 溶液检验 溶液是否含有 溶液是否含有 |
D.产品 在空气中高温分解可得到纯净的 在空气中高温分解可得到纯净的 |
您最近一年使用:0次
名校
5 .  的配位化合物较稳定且用运广泛。
的配位化合物较稳定且用运广泛。 可与
可与 、
、 、
、 等配体形成溶液呈浅紫色的
等配体形成溶液呈浅紫色的 、红色的
、红色的 、无色的
、无色的 配离子。某同学按如下步骤完成实验:
配离子。某同学按如下步骤完成实验: 的溶液中加入KSCN溶液生成蓝色的
的溶液中加入KSCN溶液生成蓝色的 的配离子,
的配离子, 不能与
不能与 形成配位离子。下列说法错误的是
形成配位离子。下列说法错误的是
 的配位化合物较稳定且用运广泛。
的配位化合物较稳定且用运广泛。 可与
可与 、
、 、
、 等配体形成溶液呈浅紫色的
等配体形成溶液呈浅紫色的 、红色的
、红色的 、无色的
、无色的 配离子。某同学按如下步骤完成实验:
配离子。某同学按如下步骤完成实验: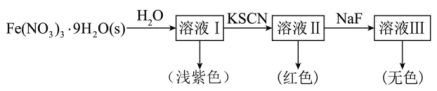
 的溶液中加入KSCN溶液生成蓝色的
的溶液中加入KSCN溶液生成蓝色的 的配离子,
的配离子, 不能与
不能与 形成配位离子。下列说法错误的是
形成配位离子。下列说法错误的是| A.Fe晶体中原子通过金属阳离子和自由电子间的静电作用相结合 |
B.可用NaF和KSCN溶液检验 溶液中是否含有 溶液中是否含有 |
C.溶液Ⅰ中 仅参与形成范德华力和氢键 仅参与形成范德华力和氢键 |
D.上述实验可得出,与 形成配合物的能力: 形成配合物的能力: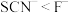 |
您最近一年使用:0次
2024-04-22更新
|
216次组卷
|
3卷引用:福建省宁德市福安市第一中学2023-2024学年高二下学期3月月考化学试题
名校
解题方法
6 . 下列实验方案能达到探究目的的是
| 选项 | 探究目的 | 实验方案 |
| A | CO还原Fe2O3实验中,Fe2O3是否全部被还原 | 向CO还原Fe2O3所得到的产物中加入稀盐酸,再滴加KSCN溶液,观察颜色变化 |
| B | 比较CH3COO-和ClO-结合H+的能力大小 | 室温下,用pH计分别测定等物质的量浓度的CH3COONa溶液和NaClO溶液的pH |
| C | 比较Ksp(BaSO4)和Ksp(BaCO3)的相对大小 | 将BaSO4粉末和Na2CO3饱和溶液混合,充分振荡,静置,取少量上层清液,滴加盐酸和BaCl2溶液,观察是否有沉淀产生 |
| D | 蔗糖水解产物是否具有还原性 | 向蔗糖溶液中加入少量稀硫酸,加热煮沸,冷却后加入银氨溶液,水浴加热,观察现象 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-17更新
|
1272次组卷
|
4卷引用:江西省宜春市宜丰中学2023-2024学年高二下学期3月月考化学试题
江西省宜春市宜丰中学2023-2024学年高二下学期3月月考化学试题江苏省南京市盐城市2024届高三一模考试化学试题(已下线)通关练03 常考化学实验基础知识-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)(已下线)题型6 元素及其化合物 化学实验基础(25题)-2024年高考化学常考点必杀300题(新高考通用)
7 . 下列实验操作过程中不会形成配位键的是
A. 溶于 溶于 中形成紫红色的溶液 中形成紫红色的溶液 |
B. 粉末溶于水形成蓝色的溶液 粉末溶于水形成蓝色的溶液 |
C.将硫氰化铵溶液滴加到含 的溶液中检验 的溶液中检验 |
D.向 溶液中加入过量的氨水 溶液中加入过量的氨水 |
您最近一年使用:0次
2024-03-29更新
|
320次组卷
|
3卷引用:辽宁省沈阳市东北育才学校高中部2023-2024学年高二下学期第1次月考化学试题
名校
解题方法
8 . 某实验小组同学用KSCN探究久置FeSO4固体变质的情况。将0.3gFeSO4固体用10mL蒸馏水溶解,配成待测液,进行实验。
【初步实验】
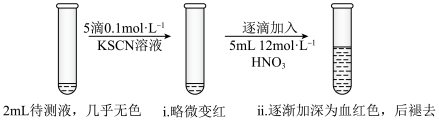
(1)用KSCN检验Fe3+的原理是___________ (用离子方程式表示)。
(2)甲同学认为FeSO4固体几乎未变质,ⅱ中变血红色是由于Fe2+被___________ (填化学式)氧化。结合平衡移动原理解释ⅱ中血红色褪去的可能原因___________ 。
(3)乙同学不认同甲对现象的解释,他推测加入浓硝酸后ⅱ中变血红色还可能与其它因素有关,可能的影响因素是___________ 。
为验证该猜测,乙同学继续进行了以下实验。【继续探究】
(4)请补全步骤Ⅱ中的操作:___________ 。
(5)由Ⅰ~Ⅲ推测FeSO4固体变质的情况是___________ (填字母序号)。
a.几乎未变质 b.部分变质 c.完全变质
【反思与迁移】
(6)从上述探究中获得启发,在用KSCN检验Fe3+及进行Fe2+还原性验证实验时,需要注意的事项有___________ (至少2条)。
【初步实验】

(1)用KSCN检验Fe3+的原理是
(2)甲同学认为FeSO4固体几乎未变质,ⅱ中变血红色是由于Fe2+被
(3)乙同学不认同甲对现象的解释,他推测加入浓硝酸后ⅱ中变血红色还可能与其它因素有关,可能的影响因素是
为验证该猜测,乙同学继续进行了以下实验。【继续探究】
| 步骤 | 操作 | 现象 |
| Ⅰ | 取2mL待测液,加入5滴0.1mol·L-1KSCN溶液,再加入5mL浓KNO3溶液 | 溶液无明显变化 |
| Ⅱ | 取2mL待测液,加入5滴0.1mol·L-1KSCN溶液,___________ | 溶液变为红色 |
| Ⅲ | 向Ⅱ中所得溶液中逐滴加入浓硝酸,边加边振荡 | 溶液逐渐加深为血红色,继续滴加浓硝酸,溶液褪色,pH变化始终不明显 |
(4)请补全步骤Ⅱ中的操作:
(5)由Ⅰ~Ⅲ推测FeSO4固体变质的情况是
a.几乎未变质 b.部分变质 c.完全变质
【反思与迁移】
(6)从上述探究中获得启发,在用KSCN检验Fe3+及进行Fe2+还原性验证实验时,需要注意的事项有
您最近一年使用:0次
名校
解题方法
9 . 下列各组离子在指定溶液中一定能大量共存的是
A.常温下,在 的溶液中:Na+、Fe2+、 的溶液中:Na+、Fe2+、 、Cl- 、Cl- |
B.1mol/L的NaAlO2溶液中:Al3+、Na+、SO2-、 |
C.含有Fe3+的溶液中:K+、Na+、SCN-、 |
D.常温下,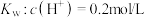 的溶液:K+、Na+、 的溶液:K+、Na+、 、 、 |
您最近一年使用:0次
10 . I.某实验小组采用下列实验探究外界条件对化学反应速率及其化学平衡的影响。
(1)室温下,向盛有 溶液的试管中加入
溶液的试管中加入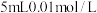 的
的 溶液,溶液变为
溶液,溶液变为_________ 色。发生反应的离子方程式为____________________________________________________ 。
(2)现将上述溶液均分为两份置于甲、乙两支试管中;
①向甲试管中加入4滴饱和 溶液,平衡
溶液,平衡______ (填“正向移动”、“逆向移动”或“不移动”);溶液中的 浓度
浓度
______ (填“增大”、“减小”或“不变”,下同),重新达到平衡时 转化率
转化率______ 。
②向乙试管中加入 固体,平衡
固体,平衡______ (填“正向移动”、“逆向移动”或“不移动”)。
II.该实验小组还利用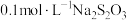 溶液和
溶液和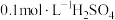 溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如表。请结合表中信息,回答有关问题:
溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如表。请结合表中信息,回答有关问题:
(3)该反应的离子方程式为____________________________________________ 。
(4)在比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰,即需要控制好与实验有关的各项反应条件,其中:
①能说明温度对该反应速率影响的组合是______ (填实验序号,下同);
②实验Ⅱ和Ⅲ探究的是_______ (填外部因素)对化学反应速率的影响,其中实验Ⅲ中 =
=_______ 。
(1)室温下,向盛有
 溶液的试管中加入
溶液的试管中加入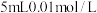 的
的 溶液,溶液变为
溶液,溶液变为(2)现将上述溶液均分为两份置于甲、乙两支试管中;
①向甲试管中加入4滴饱和
 溶液,平衡
溶液,平衡 浓度
浓度
 转化率
转化率②向乙试管中加入
 固体,平衡
固体,平衡II.该实验小组还利用
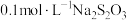 溶液和
溶液和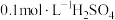 溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如表。请结合表中信息,回答有关问题:
溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如表。请结合表中信息,回答有关问题:实验序号 | 反应温度 |
|
|
| 出现沉淀所需的时间 |
I | 0℃ | 5mL | 5mL | 10mL | 12s |
II | 30℃ | 5mL | 10mL | 5mL | 8s |
III | 30℃ | 5mL | 7mL |
| 10s |
IV | 30℃ | 5mL | 5mL | 10mL | 10s |
(4)在比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰,即需要控制好与实验有关的各项反应条件,其中:
①能说明温度对该反应速率影响的组合是
②实验Ⅱ和Ⅲ探究的是
 =
=
您最近一年使用:0次