名校
解题方法
1 . 铁是人类较早使用的金属之一,FeSO4和FeCl3是重要的化工原料。
(I)硫酸亚铁晶体(FeSO4·7H2O)在医药上可作补血剂。
(1)为防止FeSO4溶液变质,应在溶液中加入少量_______ (填标号,下同);向FeSO4溶液加入_______ 可验证该溶液是否变质。
A.铜片 B.KSCN溶液 C.氯气 D.铁粉
(2)该补血剂与维生素C同时服用,有利于Fe2+的吸收。某同学设计如下实验探究维生素C的作用:取少量Fe2(SO4)3溶液于试管中,加入维生素C片2片,振荡溶解,再滴加铁氰化钾溶液,溶液出现蓝色沉淀,由此得出结论是_______ 。(已知:Fe2+遇铁氰化钾溶液产生蓝色沉淀)
(II)氯化铁溶液可用于腐蚀印刷电路板上的铜,某腐蚀后的废液中含有FeCl3、FeCl2和CuCl2,且c(Fe3+)=c(Fe2+)。
(3)从废液中可回收铜,并获得FeCl3溶液,设计如下方案:
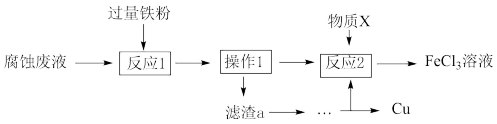
①滤渣a为_______ 。
②物质X为_______ 。
A.HCl B.酸性KMnO4溶液 C.Cl2
(4)取该废液20mL并加入mg铁粉,充分反应。
①对反应后的溶液分析错误的是_______
A.溶液中一定含有Fe2+
B.若有固体剩余,则固体中一定含有铁
C.若溶液中有Cu2+,则可能有固体析出
D.溶液若有Fe3+剩余,则一定没有固体析出
②若m=2.72,则充分反应后得到20mL3.0mol/L氯化亚铁溶液和2.24g固体混合物。则原废液中Fe3+的物质的量浓度为_______ 。
(I)硫酸亚铁晶体(FeSO4·7H2O)在医药上可作补血剂。
(1)为防止FeSO4溶液变质,应在溶液中加入少量
A.铜片 B.KSCN溶液 C.氯气 D.铁粉
(2)该补血剂与维生素C同时服用,有利于Fe2+的吸收。某同学设计如下实验探究维生素C的作用:取少量Fe2(SO4)3溶液于试管中,加入维生素C片2片,振荡溶解,再滴加铁氰化钾溶液,溶液出现蓝色沉淀,由此得出结论是
(II)氯化铁溶液可用于腐蚀印刷电路板上的铜,某腐蚀后的废液中含有FeCl3、FeCl2和CuCl2,且c(Fe3+)=c(Fe2+)。
(3)从废液中可回收铜,并获得FeCl3溶液,设计如下方案:

①滤渣a为
②物质X为
A.HCl B.酸性KMnO4溶液 C.Cl2
(4)取该废液20mL并加入mg铁粉,充分反应。
①对反应后的溶液分析错误的是
A.溶液中一定含有Fe2+
B.若有固体剩余,则固体中一定含有铁
C.若溶液中有Cu2+,则可能有固体析出
D.溶液若有Fe3+剩余,则一定没有固体析出
②若m=2.72,则充分反应后得到20mL3.0mol/L氯化亚铁溶液和2.24g固体混合物。则原废液中Fe3+的物质的量浓度为
您最近一年使用:0次
2023-02-14更新
|
299次组卷
|
3卷引用:山东省聊城市2022-2023学年高一上学期期末教学质量抽测化学试题
名校
2 . 某研究性学习小组利用如图所示的装置制备无水氯化铁。
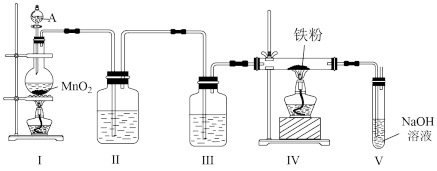
(1)装置Ⅰ中仪器A的名称是_______ ,写出装置Ⅰ中制备氯气的离子方程式_______ 。
(2)装置Ⅱ的作用是_______ 。
(3)写出在装置V中发生的反应的化学方程式_______ 。
(4)实验结束后将装置Ⅳ中的固体加水溶解并过滤,往滤液中滴加KSCN溶液,观察到_______ ,即可证明滤液中含有 。
。
(5)另一组同学发现,在装置Ⅳ和装置Ⅴ之间还需要增加一个装置才能制得无水氯化铁。为了达到这一实验目的,你认为还需在装置Ⅳ和装置Ⅴ之间添加下图中的_______ 装置(填序号)。


(1)装置Ⅰ中仪器A的名称是
(2)装置Ⅱ的作用是
(3)写出在装置V中发生的反应的化学方程式
(4)实验结束后将装置Ⅳ中的固体加水溶解并过滤,往滤液中滴加KSCN溶液,观察到
 。
。(5)另一组同学发现,在装置Ⅳ和装置Ⅴ之间还需要增加一个装置才能制得无水氯化铁。为了达到这一实验目的,你认为还需在装置Ⅳ和装置Ⅴ之间添加下图中的

您最近一年使用:0次
名校
解题方法
3 . 将 铁和氧化铁的混合物加入足量的盐酸中充分反应,固体无剩余。测得参加反应的盐酸的物质的量为
铁和氧化铁的混合物加入足量的盐酸中充分反应,固体无剩余。测得参加反应的盐酸的物质的量为 ,放出的气体
,放出的气体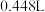 (标准状况)。则下列判断中正确的是
(标准状况)。则下列判断中正确的是
 铁和氧化铁的混合物加入足量的盐酸中充分反应,固体无剩余。测得参加反应的盐酸的物质的量为
铁和氧化铁的混合物加入足量的盐酸中充分反应,固体无剩余。测得参加反应的盐酸的物质的量为 ,放出的气体
,放出的气体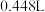 (标准状况)。则下列判断中正确的是
(标准状况)。则下列判断中正确的是A.原混合物中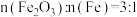 |
B.原混合物中氧化铁的质量为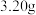 |
C.向所得溶液中滴加 溶液,溶液显红色 溶液,溶液显红色 |
D.向所得溶液中通入 ,可以将 ,可以将 完全转化为 完全转化为 |
您最近一年使用:0次
2023-01-01更新
|
590次组卷
|
6卷引用:山东省枣庄市第八中学南校2022-2023学年高一1月线上测试化学试题
山东省枣庄市第八中学南校2022-2023学年高一1月线上测试化学试题辽宁省大连市2022-2023学年高一上学期期末考试化学试题(已下线)综合突破01 期末压轴80题之选择题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(辽宁专用)河南省信阳市华中师大息县附中2022-2023学年高一下学期开学考试化学试题新疆乌鲁木齐市第八中学2022-2023学年高一下学期第一次质量检测(开学摸底)化学试题江苏省扬州中学2022-2023学年高一下学期4月期中考试化学试题
名校
4 . 下列操作能达到相应实验目的的是
| 实验目的 | 操作 | |
| A | 检验 溶液是否变质 溶液是否变质 | 取少量加入到酸性 溶液中 溶液中 |
| B | 测定家用84消毒液的 | 用洁净的玻璃棒蘸取少许消毒液滴在 试纸上 试纸上 |
| C | 除去 中的少量 中的少量 | 将混合气体通过盛有饱和 溶液的洗气瓶 溶液的洗气瓶 |
| D | 实验室制备 胶体 胶体 | 向沸水中逐滴加入饱和 溶液,边加边搅拌 溶液,边加边搅拌 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-25更新
|
277次组卷
|
2卷引用:山东省威海市2021-2022学年高一上学期期末考试化学试题
名校
5 . 微量元素体检报告单显示,某儿童体内铁元素含量偏低。
(1)服用维生素C可使食物中的 转化为
转化为 。在这个过程中体现维生素C的
。在这个过程中体现维生素C的_______ (填“氧化性”或“还原性”)。缺铁性贫血患者应补充 ,一些补铁剂用硫酸亚铁制成药片时,外表包有一层特殊的糖衣,推测糖衣的作用是
,一些补铁剂用硫酸亚铁制成药片时,外表包有一层特殊的糖衣,推测糖衣的作用是_______ 。
(2)硫酸亚铁晶体 在医药上用作补血剂.某课外小组设计实验测定该补血剂中铁元素的含量,并检验该补血剂是否变质.实验步骤如下:
在医药上用作补血剂.某课外小组设计实验测定该补血剂中铁元素的含量,并检验该补血剂是否变质.实验步骤如下:
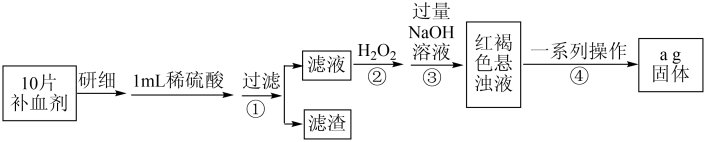
请回答下列问题:
i.取步骤①的滤液滴加 溶液后变为红色,说明滤液中含有
溶液后变为红色,说明滤液中含有_______ (填离子符号),加入 粉后红色褪去,写出加入铁粉时反应的离子方程式:
粉后红色褪去,写出加入铁粉时反应的离子方程式:_______ 。
ii.另取步骤①的滤液,检验其中是否存在 的试剂为
的试剂为_______ 。
iii.步骤②加入过量 的目的是
的目的是_______ 。
iv.一系列操作包括过滤、洗涤、灼烧,最后所得固体为_______ (写化学式)。
v.假设实验中的损耗忽略不计,若1片补血剂的质量为 ,则补血剂中铁元素的质量分数为
,则补血剂中铁元素的质量分数为_______ 。
(1)服用维生素C可使食物中的
 转化为
转化为 。在这个过程中体现维生素C的
。在这个过程中体现维生素C的 ,一些补铁剂用硫酸亚铁制成药片时,外表包有一层特殊的糖衣,推测糖衣的作用是
,一些补铁剂用硫酸亚铁制成药片时,外表包有一层特殊的糖衣,推测糖衣的作用是(2)硫酸亚铁晶体
 在医药上用作补血剂.某课外小组设计实验测定该补血剂中铁元素的含量,并检验该补血剂是否变质.实验步骤如下:
在医药上用作补血剂.某课外小组设计实验测定该补血剂中铁元素的含量,并检验该补血剂是否变质.实验步骤如下:
请回答下列问题:
i.取步骤①的滤液滴加
 溶液后变为红色,说明滤液中含有
溶液后变为红色,说明滤液中含有 粉后红色褪去,写出加入铁粉时反应的离子方程式:
粉后红色褪去,写出加入铁粉时反应的离子方程式:ii.另取步骤①的滤液,检验其中是否存在
 的试剂为
的试剂为iii.步骤②加入过量
 的目的是
的目的是iv.一系列操作包括过滤、洗涤、灼烧,最后所得固体为
v.假设实验中的损耗忽略不计,若1片补血剂的质量为
 ,则补血剂中铁元素的质量分数为
,则补血剂中铁元素的质量分数为
您最近一年使用:0次
2022-01-24更新
|
327次组卷
|
3卷引用:山东省济宁市2021-2022学年高一上学期期末考试化学试题
解题方法
6 . 除去下列物质中含有的少量杂质,所选试剂错误的是
A. 溶液 溶液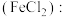 氯水 氯水 |
B. 溶液 溶液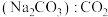 气体 气体 |
C. 溶液 溶液 粉 粉 |
D.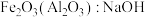 溶液 溶液 |
您最近一年使用:0次
名校
7 . 某工厂的工业废水中含有大量的 和
和 ,为了减少污染并变废为宝,工厂拟定用以下流程从该废水中回收
,为了减少污染并变废为宝,工厂拟定用以下流程从该废水中回收 和金属
和金属 。请回答相关问题:
。请回答相关问题:
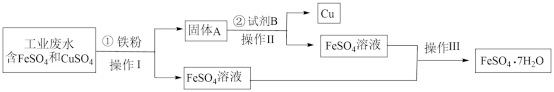
(1)操作I分离方法的名称是___________ 。
(2)实验室模拟操作II使用的主要玻璃仪器有___________ 种。
(3)为得到纯净的铜需要进行洗涤,请简述如何证明洗涤干净___________ 。
(4)从 溶液中得到
溶液中得到 的操作是加热浓缩→冷却结晶→过滤→洗涤,该过程特别需要注意的事项为
的操作是加热浓缩→冷却结晶→过滤→洗涤,该过程特别需要注意的事项为___________ 。
(5)流程图中, 溶液只含有
溶液只含有 而不含
而不含 ,可证明该事实的实验方法是
,可证明该事实的实验方法是______ (填序号)。
①先加氯水,后加 溶液后显红色
溶液后显红色
②先加 溶液,不显红色,再加氯水后显红色
溶液,不显红色,再加氯水后显红色
③只滴加 溶液不显红色
溶液不显红色
 和
和 ,为了减少污染并变废为宝,工厂拟定用以下流程从该废水中回收
,为了减少污染并变废为宝,工厂拟定用以下流程从该废水中回收 和金属
和金属 。请回答相关问题:
。请回答相关问题:
(1)操作I分离方法的名称是
(2)实验室模拟操作II使用的主要玻璃仪器有
(3)为得到纯净的铜需要进行洗涤,请简述如何证明洗涤干净
(4)从
 溶液中得到
溶液中得到 的操作是加热浓缩→冷却结晶→过滤→洗涤,该过程特别需要注意的事项为
的操作是加热浓缩→冷却结晶→过滤→洗涤,该过程特别需要注意的事项为(5)流程图中,
 溶液只含有
溶液只含有 而不含
而不含 ,可证明该事实的实验方法是
,可证明该事实的实验方法是①先加氯水,后加
 溶液后显红色
溶液后显红色②先加
 溶液,不显红色,再加氯水后显红色
溶液,不显红色,再加氯水后显红色③只滴加
 溶液不显红色
溶液不显红色
您最近一年使用:0次
2022-01-24更新
|
138次组卷
|
2卷引用:山东省枣庄滕州市2021-2022学年高一上学期期末考试化学试题
8 . 某化学兴趣小组对硫酸亚铁的性质进行探究并做如下实验,将称量好的硫酸亚铁溶解于一定浓度的稀硫酸中配制成 的溶液:
的溶液:
回答下列问题:
(1)进一步研究证实,黑色沉淀的主要成分是 。
。 溶液呈碱性,
溶液呈碱性, 溶液与其反应不生成
溶液与其反应不生成 而生成
而生成 的可能原因是
的可能原因是_______ 。
(2用离子方程式表示步骤ⅱ中溶液变红的原因:_______ 、_______ 。
(3)甲同学探究步骤ⅲ中溶液褪色的原因,提出如下假设:
a. 被
被 还原 b.
还原 b. 被
被 氧化 c.
氧化 c. 被
被 氧化
氧化
乙同学根据上述实验认为假设b不成立,他依据的现象是_____ 。
(4)甲同学利用上述部分试剂,通过以下实验验证了(3)中假设c成立。请将以下实验操作及现象补充完整。
 的溶液:
的溶液:| 实验序号 | 操作及现象 |
| ⅰ | 取 上述 上述 溶液于试管中,逐滴加入少量 溶液于试管中,逐滴加入少量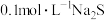 溶液,产生大量黑色沉淀 溶液,产生大量黑色沉淀 |
| ⅱ | 取 上述 上述 溶液于试管中,加入2滴 溶液于试管中,加入2滴 溶液无现象,通入一段时间 溶液无现象,通入一段时间 ,溶液变为浅红色 ,溶液变为浅红色 |
| ⅲ | 重复实验ⅱ,向浅红色溶液中加入5% 溶液至过量,产生无色气体(经检验为 溶液至过量,产生无色气体(经检验为 ),溶液变为深红色中,且红色很快褪去 ),溶液变为深红色中,且红色很快褪去 |
(1)进一步研究证实,黑色沉淀的主要成分是
 。
。 溶液呈碱性,
溶液呈碱性, 溶液与其反应不生成
溶液与其反应不生成 而生成
而生成 的可能原因是
的可能原因是(2用离子方程式表示步骤ⅱ中溶液变红的原因:
(3)甲同学探究步骤ⅲ中溶液褪色的原因,提出如下假设:
a.
 被
被 还原 b.
还原 b. 被
被 氧化 c.
氧化 c. 被
被 氧化
氧化乙同学根据上述实验认为假设b不成立,他依据的现象是
(4)甲同学利用上述部分试剂,通过以下实验验证了(3)中假设c成立。请将以下实验操作及现象补充完整。
| 步骤 | 试剂及操作 | 现象 |
| 1 | 取实验ⅲ中褪色后溶液少量于试管,滴加 溶液 溶液 | ① |
| 2 | ② | 溶液变为红色 |
您最近一年使用:0次
2021-06-25更新
|
266次组卷
|
2卷引用:山东省莱州市2020-2021学年高二下学期期末考试化学试题



