解题方法
1 . 某城市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径≤2.5um的悬浮颗粒物,已知1μm=1×10-6m),其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1)PM2.5分散在空气中形成的分散系___________ (填“属于"或“不属于)胶体。
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断待测试样为___________ (填“酸”或“碱”)性。
(3)洗涤含SO2的烟气,以下物质可作洗涤剂的是___________ (填字母)
a.Ca(OH)2 b.CaCl2 c.Na2CO3 d.NaHSO3
(4)硫酸生产及煤燃烧产生的废气SO2等会对大气造成污染。
①为防止工业煤燃烧产生SO2,常向燃煤中加入CaCO3浆状物进行脱硫,脱硫的产品用于制造石膏。脱硫反应的化学方程式为___________ 。
②某硫酸化工厂,使用一种含杂质为25%的黄铁矿石(FeS2)为原料。若取2吨该矿石,可制得98%的浓硫酸___________ 吨(假设生产过程中96%SO2转化为SO3)。
(1)PM2.5分散在空气中形成的分散系
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ | NH | SO | NO | Cl- |
| 浓度/mol/L | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
(3)洗涤含SO2的烟气,以下物质可作洗涤剂的是
a.Ca(OH)2 b.CaCl2 c.Na2CO3 d.NaHSO3
(4)硫酸生产及煤燃烧产生的废气SO2等会对大气造成污染。
①为防止工业煤燃烧产生SO2,常向燃煤中加入CaCO3浆状物进行脱硫,脱硫的产品用于制造石膏。脱硫反应的化学方程式为
②某硫酸化工厂,使用一种含杂质为25%的黄铁矿石(FeS2)为原料。若取2吨该矿石,可制得98%的浓硫酸
您最近一年使用:0次
解题方法
2 . 按要求回答下列问题:
(1)现有8种物质:A.稀硫酸;B.Fe2(SO4)3溶液;C.CO;D.熔融的NaNO3;E.SO2;F.Fe(OH)3胶体;G.NH4NO3固体;H.Na2CO3溶液。
①能导电的电解质有___________ (填字母,下同),属于酸性氧化物的有___________ 。
②Fe2(SO4)3溶于水的电离方程式为___________ 。
③写出实验室制取Fe(OH)3胶体的离子方程式:___________ 。
④写出H与足量A反应的离子方程式:___________ 。
(2)①甲烷(甲烷中C的化合价为-4)在厌氧氧化菌的作用下,可以和氢氧化铁发生如下反应,配平该离子方程式:___________ 。

②该反应中的还原剂为___________ (填化学式),被还原的物质与被氧化的物质的物质的量之比为___________ 。
(3)无氧条件下加热蓝铁矿(无杂质),发生反应的化学方程式为 ,蓝铁矿的质量由10.04g减小到7.16g,则n=
,蓝铁矿的质量由10.04g减小到7.16g,则n=___________ 。
(1)现有8种物质:A.稀硫酸;B.Fe2(SO4)3溶液;C.CO;D.熔融的NaNO3;E.SO2;F.Fe(OH)3胶体;G.NH4NO3固体;H.Na2CO3溶液。
①能导电的电解质有
②Fe2(SO4)3溶于水的电离方程式为
③写出实验室制取Fe(OH)3胶体的离子方程式:
④写出H与足量A反应的离子方程式:
(2)①甲烷(甲烷中C的化合价为-4)在厌氧氧化菌的作用下,可以和氢氧化铁发生如下反应,配平该离子方程式:

②该反应中的还原剂为
(3)无氧条件下加热蓝铁矿(无杂质),发生反应的化学方程式为
 ,蓝铁矿的质量由10.04g减小到7.16g,则n=
,蓝铁矿的质量由10.04g减小到7.16g,则n=
您最近一年使用:0次
解题方法
3 . 甲烷干重整(DRM)是利用 和
和 在催化剂的作用下制备合成气,作为可持续替代燃料。DRM的主要反应为:
在催化剂的作用下制备合成气,作为可持续替代燃料。DRM的主要反应为:
Ⅰ.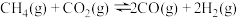
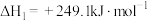
Ⅱ.
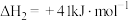
该过程中还伴随积碳反应的发生。
(1)一定压强下,由最稳定单质生成 化合物的焓变为该物质的摩尔生成焓。已知
化合物的焓变为该物质的摩尔生成焓。已知 、
、 的摩尔生成焓分别为
的摩尔生成焓分别为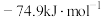 、
、 。则
。则 的摩尔生成焓为
的摩尔生成焓为_______  。
。
(2)甲烷和二氧化碳的起始物质的量均为 ,实验测得在
,实验测得在 下,平衡时各组分的量随温度变化如图所示。
下,平衡时各组分的量随温度变化如图所示。_______ mol,反应Ⅱ的压强平衡常数
_______ 。
②为了消除积碳带来的影响,反应选择在_______ (填“高温”或“低温”)下进行。
(3)在不同压强下,按照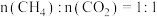 投料,假设只发生反应Ⅰ和Ⅱ。
投料,假设只发生反应Ⅰ和Ⅱ。 的平衡转化率随温度的变化关系如图所示。
的平衡转化率随温度的变化关系如图所示。 、
、 、
、 ,三者由大到小顺序为
,三者由大到小顺序为________ 。
②压强 、
、 、
、 、
、 由小到大的顺序为
由小到大的顺序为________ 。
③ ,四条曲线几乎交于一点的原因是
,四条曲线几乎交于一点的原因是________ 。
 和
和 在催化剂的作用下制备合成气,作为可持续替代燃料。DRM的主要反应为:
在催化剂的作用下制备合成气,作为可持续替代燃料。DRM的主要反应为:Ⅰ.
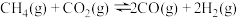
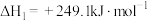
Ⅱ.

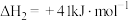
该过程中还伴随积碳反应的发生。
(1)一定压强下,由最稳定单质生成
 化合物的焓变为该物质的摩尔生成焓。已知
化合物的焓变为该物质的摩尔生成焓。已知 、
、 的摩尔生成焓分别为
的摩尔生成焓分别为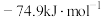 、
、 。则
。则 的摩尔生成焓为
的摩尔生成焓为 。
。(2)甲烷和二氧化碳的起始物质的量均为
 ,实验测得在
,实验测得在 下,平衡时各组分的量随温度变化如图所示。
下,平衡时各组分的量随温度变化如图所示。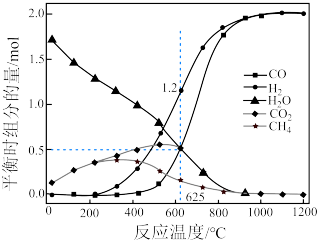

②为了消除积碳带来的影响,反应选择在
(3)在不同压强下,按照
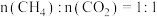 投料,假设只发生反应Ⅰ和Ⅱ。
投料,假设只发生反应Ⅰ和Ⅱ。 的平衡转化率随温度的变化关系如图所示。
的平衡转化率随温度的变化关系如图所示。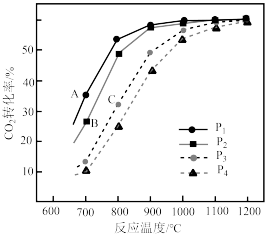
 、
、 、
、 ,三者由大到小顺序为
,三者由大到小顺序为②压强
 、
、 、
、 、
、 由小到大的顺序为
由小到大的顺序为③
 ,四条曲线几乎交于一点的原因是
,四条曲线几乎交于一点的原因是
您最近一年使用:0次
名校
解题方法
4 . 除去粗盐中的Ca2+、Mg2+、 及泥沙,可先将粗盐溶于水,然后进行下列操作:
及泥沙,可先将粗盐溶于水,然后进行下列操作:
①过滤②加过量的NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液。正确的操作顺序是
 及泥沙,可先将粗盐溶于水,然后进行下列操作:
及泥沙,可先将粗盐溶于水,然后进行下列操作:①过滤②加过量的NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液。正确的操作顺序是
| A.①④②⑤③ | B.④①②⑤③ | C.②④⑤①③ | D.⑤②④①③ |
您最近一年使用:0次
2024-03-30更新
|
214次组卷
|
66卷引用:山东省昌邑市第一中学2017-2018学年高一上学期期末模拟化学试题
山东省昌邑市第一中学2017-2018学年高一上学期期末模拟化学试题吉林省长春外国语学校2017-2018学年高一上学期期末考试化学(文)试题山东省日照市莒县2020-2021学年高一11月模块考试化学试题(已下线)专题01 硫及其化合物【专项训练】-2020-2021学年高一化学下学期期末专项复习(人教版2019必修第二册)北京市大兴区2020-2021学年高一下学期期末考试化学试题吉林省长春市2020-2021学年高一下学期期末联考化学试题黑龙江省哈尔滨市第一六二中学2021-2022学年高一上学期期末考试化学试题安徽省蚌埠市2021-2022学年高一上学期期末学业水平测试化学试题山东省临沂市2021-2022学年高一下学期期中考试化学试题云南红河县第一中学2021-2022学年高一下学期期末考试化学试题云南省红河县第一中学2020-2021学年高一下学期期末考试化学试题山西省阳泉市2022-2023学年高一下学期期末考试化学试题安徽省蚌埠市固镇县汉兴学校、怀远县禹泽学校2023-2024学年高一上学期12月期末联考化学试题2015-2016学年陕西省城固一中高一上学期期中测试化学试卷北京市首师附2019-2020学年第一学期期中考试高一化学试卷四川省自贡市田家炳中学2019-2020学年高一上学期期中考试化学试题天津市静海县第一中学2019-2020学年高一3月学生学业能力调研考试化学试题四川省江油中学2018-2019学年高一10月月考化学试题内蒙古北京八中乌兰察布分校2020-2021学年高一上学期第一次月考化学试题北京交通大学附属中学2020-2021学年高一上学期期中考试化学试题宁夏吴忠市吴忠中学2020-2021学年高一上学期期中考试化学试题四川省成都市实验外国语学校(西区)2020-2021学年高一上学期期中考试化学试题辽宁省抚顺县高级中学2019-2020学年高一下学期期中网课学习质量检测化学试题黑龙江省大庆实验中学2020-2021学年高一上学期第一次线上教学质量检测(1月)化学试题合肥市第十一中学2020-2021学年高一下学期第一次教学质量评估化学试题贵州省毕节市民族中学2020-2021学年高一上学期12月月考化学试题广东省中山市第二中学2020-2021学年高一下学期第一次段考化学试题黑龙江省牡丹江市海林市朝鲜族中学2020-2021学年高一4月月考化学试题湖北省黄冈市麻城市麻城二中2020-2021学年高一下学期期中考试化学试题山西省大同市天镇县实验中学2020-2021学年高一下学期期中考试化学试题河北省师范大学附属中学2020-2021学年高一第二学期期中考试化学试题吉林省白城市第一中学2020-2021学年高一下学期期中考试化学试题内蒙古集宁新世纪中学2020-2021学年高一上学期期中考试化学试题重庆铁路中学2020-2021学年高一下学期4月月考化学试题广东省2012年全国高中学生化学素质和实验能力竞赛初赛试题(B组)(已下线)3.3.1 粗盐提纯 从海水中提取溴(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)宁夏中卫市第一中学2021-2022学年高一上学期第一次月考化学试题安徽省合肥市第六中学2021-2022学年高一上学期第一次月考化学试题浙江省绍兴市诸暨中学2021-2022学年高一上学期期中考试(实验班)化学试题甘肃省永昌县第一高级中学2020-2021学年高一上学期期中考试化学试题云南省宣威市第三中学2021-2022学年高一下学期4月考试化学试题云南省昆明市云南师范大学附属中学2021-2022学年高一下学期期中考试化学试题广东省深圳市福田区外国语高级中学2021-2022学年高一下学期期中考试(选择考)化学试题江苏省天一中学2021-2022学年高一下学期期中考试(文)化学试题北京市东直门中学2021—2022学年高一下学期6月月考化学试题四川省什邡中学2021-2022学年高一上学期第一次月考化学试题云南省昆明北大博雅实验中学2020-2021学年高一下学期期中考试化学试题吉林省洮南市第一中学2021-2022学年高一下学期第一次月考化学试题黑龙江省双鸭山市第一中学2022-2023学年高一下学期4月月考(普通班)化学试题湖南省岳阳市2022-2023学年高一上学期第一次月考化学试题辽宁省鞍山市普通高中2022-2023学年高一下学期期中考试化学(A卷)试题广东省广州大同中学2022-2023学年高一下学期期中考试化学试题广东省江门市新会陈经纶中学2022-2023学年高一下学期期中考试(合格考)化学试题安徽省六安第二中学2022-2023学年高一下学期期中考试化学试题陕西省武功县普集高级中学2022-2023学年高一下学期3月月考化学试题广东省佛山市三水中学2022-2023学年高一下学期3月第一次统测化学试题黑龙江省哈尔滨市第四中学校2023-2024学年高一上学期11月月考化学试题 新疆生产建设兵团第三师图木舒克市第一中学2023-2024学年高一上学期10月第一次月考化学试卷河北省邯郸市永年区第二中学2023-2024学年高一上学期12月月考化学试题广东省深圳市光明中学2023-2024学年高一下学期3月第一次统测化学试题广东省江门市某校2023-2024学年高一下学期第一次质量检测化学试题云南省昆明市禄劝彝族苗族自治县第一中学2023-2024学年高一下学期3月月考化学试题四川省华蓥中学2023-2024学年高一下学期4月月考化学试题广东省深圳市龙岗区平湖外国语学校2023-2024学年高一下学期期中考试化学试卷广东省潮州市松昌中学2023-2024学年高一下学期期中考试化学试题重庆市辅仁中学校2023-2024学年高一下学期期中考试化学试题
5 . 氢气是一种清洁燃料和重要的工业原料,广泛应用于航空航天、石油化工、有机合成等领域。回答下列问题:
(1)一定条件下,氢气与二氧化碳气体反应生成 和水蒸气。已知相关化学键键能如表所示:
和水蒸气。已知相关化学键键能如表所示:
则该反应的热化学方程式为___________ 。
(2)“萨巴蒂尔反应”[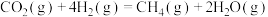
 ]可将航天员呼出的
]可将航天员呼出的 转化为供空间站在轨运行的火箭燃料。有关物质的摩尔燃烧焓如表所示:
转化为供空间站在轨运行的火箭燃料。有关物质的摩尔燃烧焓如表所示:
①石墨不完全燃烧生成 的热化学方程式为
的热化学方程式为___________ 。
②已知每18g水蒸气转化为液态水释放44kJ的热量,则“萨巴蒂尔反应”的
___________ 。
(3)一种用于制氢气的膜基海水电解装置如图所示,其中隔膜只允许水分子通过。
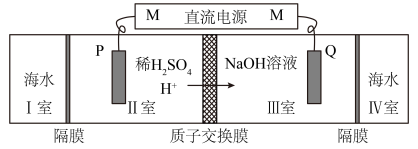
①N电极为直流电源的电子___________ (填“流入”或“流出”)极,P电极发生的电极反应式为___________ 。
②理论上,该装置每产生13.44L(STP)气体时,转移电子的数目为___________ ,I室海水减少的质量为___________ 。
(1)一定条件下,氢气与二氧化碳气体反应生成
 和水蒸气。已知相关化学键键能如表所示:
和水蒸气。已知相关化学键键能如表所示:| 化学键 | H―H | C―O | C=O | O―H | C―H |
E/( ) ) | 436 | 326 | 803 | 464 | 414 |
(2)“萨巴蒂尔反应”[
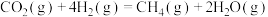
 ]可将航天员呼出的
]可将航天员呼出的 转化为供空间站在轨运行的火箭燃料。有关物质的摩尔燃烧焓如表所示:
转化为供空间站在轨运行的火箭燃料。有关物质的摩尔燃烧焓如表所示:| 物质 |  |  |  |  |
摩尔燃烧焓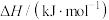 | ―393.5 | ―285.8 | ―283 | ―890.3 |
 的热化学方程式为
的热化学方程式为②已知每18g水蒸气转化为液态水释放44kJ的热量,则“萨巴蒂尔反应”的

(3)一种用于制氢气的膜基海水电解装置如图所示,其中隔膜只允许水分子通过。

①N电极为直流电源的电子
②理论上,该装置每产生13.44L(STP)气体时,转移电子的数目为
您最近一年使用:0次
6 . 乙烯被广泛用于合成聚乙烯等聚合产品。工业生产的乙烯中含有的少量乙炔会导致聚合催化剂中毒失活,含有的乙烷会使聚合过程终止。因此乙炔的选择加氢制乙烯在生产中有重大经济意义。反应原理如下:
反应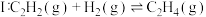 (主反应)
(主反应)
反应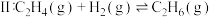 (副反应)
(副反应)
回答下列问题:
(1)分别以 乙炔和
乙炔和  氢气或
氢气或  乙烯为初始原料,在
乙烯为初始原料,在 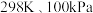 下,使用对反应
下,使用对反应  选择性好的催化剂,分别在恒压容器中反应,达平衡时,以乙炔和氢气为原料,体系向环境放热
选择性好的催化剂,分别在恒压容器中反应,达平衡时,以乙炔和氢气为原料,体系向环境放热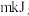 以乙烯为原料,体系从环境吸热
以乙烯为原料,体系从环境吸热 ,忽略副反应热效应,反应焓变
,忽略副反应热效应,反应焓变
___________  。
。
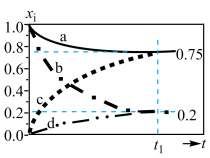
(2)初始条件同上,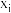 表示某物种
表示某物种  的物质的量与除
的物质的量与除  外其它各物种总物质的量之比,
外其它各物种总物质的量之比,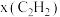 和
和  随时间
随时间 变化关系如图所示,实验测得
变化关系如图所示,实验测得 ,则图中表示
,则图中表示 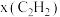 变化的曲线是
变化的曲线是___________ ;反应I平衡常数Kp=___________  ;以乙炔和氢气为原料时,
;以乙炔和氢气为原料时, 时刻
时刻 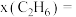
___________ 。
(3) 在催化剂表面逐步加氢,当变成
在催化剂表面逐步加氢,当变成  时,
时, 可从催化剂表面脱附生成
可从催化剂表面脱附生成 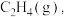 也可以继续加氢。清华大学李亚林团队找到一种催化剂,可使
也可以继续加氢。清华大学李亚林团队找到一种催化剂,可使  脱附生成
脱附生成  而不继续加氢,使催化产物停留在乙烯而不继续加氢生成乙烷。下面是两种催化剂(①
而不继续加氢,使催化产物停留在乙烯而不继续加氢生成乙烷。下面是两种催化剂(① 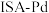 和②
和②  )分别催化乙炔加氢的反应机理:
)分别催化乙炔加氢的反应机理:
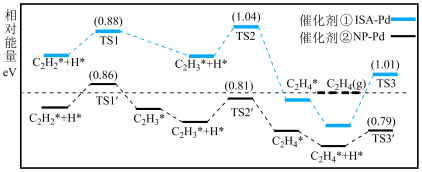
在催化剂② 作用下,
作用下, 倾向于
倾向于___________ (填“脱附”或“加氢”),结合图中数据,推测清华大学团队找到的理想催化剂是___________ (填“①”或“②”),原因是在该催化剂上 的脱附能
的脱附能___________ (填“高于”或“低于”)  进一步加氢需要突破的能垒,该催化剂具有好的选择性。
进一步加氢需要突破的能垒,该催化剂具有好的选择性。
反应
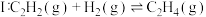 (主反应)
(主反应)反应
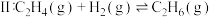 (副反应)
(副反应)回答下列问题:
(1)分别以
 乙炔和
乙炔和  氢气或
氢气或  乙烯为初始原料,在
乙烯为初始原料,在 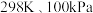 下,使用对反应
下,使用对反应  选择性好的催化剂,分别在恒压容器中反应,达平衡时,以乙炔和氢气为原料,体系向环境放热
选择性好的催化剂,分别在恒压容器中反应,达平衡时,以乙炔和氢气为原料,体系向环境放热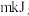 以乙烯为原料,体系从环境吸热
以乙烯为原料,体系从环境吸热 ,忽略副反应热效应,反应焓变
,忽略副反应热效应,反应焓变
 。
。(2)初始条件同上,
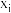 表示某物种
表示某物种  的物质的量与除
的物质的量与除  外其它各物种总物质的量之比,
外其它各物种总物质的量之比,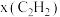 和
和  随时间
随时间 变化关系如图所示,实验测得
变化关系如图所示,实验测得 ,则图中表示
,则图中表示 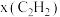 变化的曲线是
变化的曲线是 ;以乙炔和氢气为原料时,
;以乙炔和氢气为原料时, 时刻
时刻 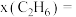

(3)
 在催化剂表面逐步加氢,当变成
在催化剂表面逐步加氢,当变成  时,
时, 可从催化剂表面脱附生成
可从催化剂表面脱附生成 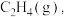 也可以继续加氢。清华大学李亚林团队找到一种催化剂,可使
也可以继续加氢。清华大学李亚林团队找到一种催化剂,可使  脱附生成
脱附生成  而不继续加氢,使催化产物停留在乙烯而不继续加氢生成乙烷。下面是两种催化剂(①
而不继续加氢,使催化产物停留在乙烯而不继续加氢生成乙烷。下面是两种催化剂(① 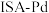 和②
和②  )分别催化乙炔加氢的反应机理:
)分别催化乙炔加氢的反应机理:
在催化剂②
 作用下,
作用下, 倾向于
倾向于 的脱附能
的脱附能 进一步加氢需要突破的能垒,该催化剂具有好的选择性。
进一步加氢需要突破的能垒,该催化剂具有好的选择性。
您最近一年使用:0次
解题方法
7 . W、X、Y、Z、R为原子序数依次增大的短周期主族元素,W的核外电子只有一种自旋方向;Y、Z、R在元素周期表中相邻,X的核外电子数与Y的价层电子数相等,R2是氧化性最强的单质,回答下列问题:
(1)由X原子核形成的三种微粒,电子排布式分别为:①1s22s2、②1s22s22p1、③1s22s12p2,有关这些微粒的叙述正确的是___________ (填标号)。
a.得电子能力:②>① b.表示基态原子(或离子)的是:①②
c.微粒半径:①>② d.电离一个电子所需最低能量:①>②>③
(2)YR3是一种重要的电子工业材料。分子的极性:YR3___________ XR3(填“>”或“<”或“=”);YR3与YW3结构相似,YW3易与过渡金属阳离子形成配离子而YR3不能,原因是___________ 。
(3)同周期元素中,第一电离能比Z大的元素有_________ 种;Z与Y形成的固态Y2Z5由YZ 和YZ
和YZ 两种离子组成,固态Y2Z5中Y原子的杂化方式为
两种离子组成,固态Y2Z5中Y原子的杂化方式为_________ ,YZ 的电子式为
的电子式为_________ 。
(4)X与Z可形成多种结构形式的阴离子,已知阴离子X3Z 结构中只有一个正六元环,则n=
结构中只有一个正六元环,则n=___________ ,该阴离子的结构式为___________ 。
(1)由X原子核形成的三种微粒,电子排布式分别为:①1s22s2、②1s22s22p1、③1s22s12p2,有关这些微粒的叙述正确的是
a.得电子能力:②>① b.表示基态原子(或离子)的是:①②
c.微粒半径:①>② d.电离一个电子所需最低能量:①>②>③
(2)YR3是一种重要的电子工业材料。分子的极性:YR3
(3)同周期元素中,第一电离能比Z大的元素有
 和YZ
和YZ 两种离子组成,固态Y2Z5中Y原子的杂化方式为
两种离子组成,固态Y2Z5中Y原子的杂化方式为 的电子式为
的电子式为(4)X与Z可形成多种结构形式的阴离子,已知阴离子X3Z
 结构中只有一个正六元环,则n=
结构中只有一个正六元环,则n=
您最近一年使用:0次
名校
8 . 咪唑(a)和N-甲基咪唑(b)都是合成医药中间体的重要原料,分子中均存在大π键,结构如图.下列说法正确的是
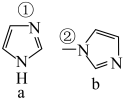
A.大π键均表示为 | B.C―N键的键长:①<② |
C.C、N原子均为 杂化 杂化 | D.a、b所有原子均在同一平面上 |
您最近一年使用:0次
2024-02-22更新
|
664次组卷
|
2卷引用:山东省青岛市2023-2024学年高二上学期1月期末化学试题
9 . 氨是化肥工业的主要原料,其在国防、涂料等领域应用广泛。回答下列问题:
(1)合成氨反应 的活化能
的活化能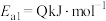 ,则氨分解反应
,则氨分解反应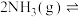
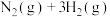 的活化能
的活化能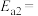
___________  (用含Q、a、b、c的关系式表示)。(已知相关化学键的键能数据如表所示)
(用含Q、a、b、c的关系式表示)。(已知相关化学键的键能数据如表所示)
(2)在体积为2L的密闭容器中充入1mol 和3mol
和3mol ,发生反应
,发生反应 。
。 、
、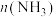 在
在 和
和 温度下的变化曲线如图所示。
温度下的变化曲线如图所示。
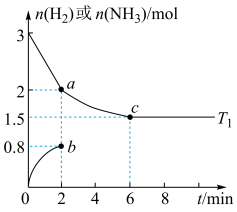
①在___________ (填“ ”“
”“ ”)温度下先达到平衡状态,判断的依据是
”)温度下先达到平衡状态,判断的依据是___________ 。
②a、b、c三点, 的转化率由大到小的顺序为
的转化率由大到小的顺序为___________ ,已知c点之后容器内的压强为P,且保持不变。合成氨反应在 温度下的
温度下的
___________ 。
(3)清华大学科研团队在电催化氮还原合成氨方面取得重大进展。两种条件下的反应历程如图甲所示。

①图乙对应的是图甲中的电催化___________ (填“Ⅰ”“Ⅱ”)。
②由图甲可见,不同历程中 的活化均为决速步骤,理由是
的活化均为决速步骤,理由是___________ 。
③碱性水溶液中,该电催化氮还原合成氨的电极反应式为___________ 。
(1)合成氨反应
 的活化能
的活化能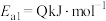 ,则氨分解反应
,则氨分解反应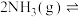
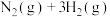 的活化能
的活化能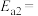
 (用含Q、a、b、c的关系式表示)。(已知相关化学键的键能数据如表所示)
(用含Q、a、b、c的关系式表示)。(已知相关化学键的键能数据如表所示)| 化学键 |  |  |  |
 | a | b | c |
(2)在体积为2L的密闭容器中充入1mol
 和3mol
和3mol ,发生反应
,发生反应 。
。 、
、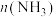 在
在 和
和 温度下的变化曲线如图所示。
温度下的变化曲线如图所示。
①在
 ”“
”“ ”)温度下先达到平衡状态,判断的依据是
”)温度下先达到平衡状态,判断的依据是②a、b、c三点,
 的转化率由大到小的顺序为
的转化率由大到小的顺序为 温度下的
温度下的
(3)清华大学科研团队在电催化氮还原合成氨方面取得重大进展。两种条件下的反应历程如图甲所示。

①图乙对应的是图甲中的电催化
②由图甲可见,不同历程中
 的活化均为决速步骤,理由是
的活化均为决速步骤,理由是③碱性水溶液中,该电催化氮还原合成氨的电极反应式为
您最近一年使用:0次
10 . 在铜氨溶液中存在如下平衡关系: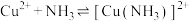 ;
;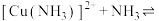
 ;
; ;
; ,平衡常数依次为
,平衡常数依次为 、
、 、
、 、
、 。
。 、
、 、
、 、
、 、
、 的分布系数
的分布系数 随
随 的变化如图。下列说法错误的是
的变化如图。下列说法错误的是
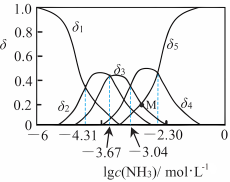
[已知: ]
]
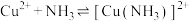 ;
;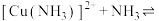
 ;
; ;
; ,平衡常数依次为
,平衡常数依次为 、
、 、
、 、
、 。
。 、
、 、
、 、
、 、
、 的分布系数
的分布系数 随
随 的变化如图。下列说法错误的是
的变化如图。下列说法错误的是
[已知:
 ]
]A.随 的增大, 的增大, 的浓度先增大后减小 的浓度先增大后减小 |
B.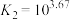 |
C.反应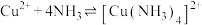 的平衡常数为K, 的平衡常数为K,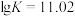 |
D.M点,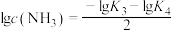 |
您最近一年使用:0次



