名校
解题方法
1 . 如图为铁及其化合物的“价—类”二维图。_______ 和化学式②_______ 。
(2)参考“价—类”二维图,对 的性质进行预测:
的性质进行预测: 可能与下列试剂中的
可能与下列试剂中的_______ (填字母)发生反应。
① ②
② 溶液 ③
溶液 ③ 溶液 ④
溶液 ④ 溶液 ⑤
溶液 ⑤ 溶液
溶液
(3)某工厂用 溶液腐蚀镀有铜的绝缘板生产印刷电路,写出该过程的化学反应方程式并用双线桥标出电子转移的方向和数目
溶液腐蚀镀有铜的绝缘板生产印刷电路,写出该过程的化学反应方程式并用双线桥标出电子转移的方向和数目____ 。当转移电子数为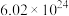 时,被氧化的物质的质量为
时,被氧化的物质的质量为___ g。

(2)参考“价—类”二维图,对
 的性质进行预测:
的性质进行预测: 可能与下列试剂中的
可能与下列试剂中的①
 ②
② 溶液 ③
溶液 ③ 溶液 ④
溶液 ④ 溶液 ⑤
溶液 ⑤ 溶液
溶液(3)某工厂用
 溶液腐蚀镀有铜的绝缘板生产印刷电路,写出该过程的化学反应方程式并用双线桥标出电子转移的方向和数目
溶液腐蚀镀有铜的绝缘板生产印刷电路,写出该过程的化学反应方程式并用双线桥标出电子转移的方向和数目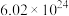 时,被氧化的物质的质量为
时,被氧化的物质的质量为
您最近一年使用:0次
2023-02-21更新
|
224次组卷
|
3卷引用:安徽省六安市裕安区新安中学2022-2023学年高一下学期期中考试化学试题
19-20高一·浙江·阶段练习
名校
解题方法
2 . 某同学用如下实验探究Fe2+、Fe3+的性质。请回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol·L-1的溶液,在FeCl3溶液中需加入少量铁屑,发生反应的化学方程式为_______ 。
(2)甲同学取2 mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化,FeCl2溶液与氯水反应的化学方程式为_______ 。
(3)乙同学认为甲同学的实验不够严谨,该同学在2 mL FeCl2溶液中先加入0.5 mL煤油,再于液面下依次加入1滴KSCN溶液和几滴氯水,溶液变红,煤油的作用是_______ 。
(4)丁同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为_______ 。
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol·L-1的溶液,在FeCl3溶液中需加入少量铁屑,发生反应的化学方程式为
(2)甲同学取2 mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化,FeCl2溶液与氯水反应的化学方程式为
(3)乙同学认为甲同学的实验不够严谨,该同学在2 mL FeCl2溶液中先加入0.5 mL煤油,再于液面下依次加入1滴KSCN溶液和几滴氯水,溶液变红,煤油的作用是
(4)丁同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为
您最近一年使用:0次
2023-02-03更新
|
234次组卷
|
5卷引用:黑龙江省鸡西市第一中学2021-2022学年高一上学期期中考试化学试题
黑龙江省鸡西市第一中学2021-2022学年高一上学期期中考试化学试题(已下线)【浙江新东方】双师 (44).新疆巴音郭楞蒙古自治州第一中学等两校2022-2023学年高一上学期期末联考化学试题第2课时 铁盐和亚铁盐(已下线)【定心卷】3.1.2 铁的重要化合物随堂练习-人教版2023-2024学年必修第一册
名校
3 . 有四种常见药物①维生素C;②青霉素;③胃舒平;④麻黄碱。回答下列问题:
(1)某同学胃酸过多,应选用的药物是_______ (填序号)。抗酸药是治疗胃酸过多的一类药物,写出一种抗酸药与胃酸反应的化学方程式_______ 。
(2)由于具有兴奋作用,国际奥委会严禁运动员服用的药物是_______ (填序号)。
(3)从用药安全角度考虑,使用前要进行皮肤敏感性测试的药物是_______ (填序号)。
(4)_______ (填序号)又称为抗坏血酸,它的分子式为_______ 。
(5)为预防缺铁性贫血,一些食品中加入了铁元素(含Fe2+物质)。若向铁强化牛奶中滴加KSCN溶液,发现牛奶变为红色,说明_______ ,此时若向其中加入一片维生素C,则发现红色消失,该实验说明维生素C具有_______ 性。
(1)某同学胃酸过多,应选用的药物是
(2)由于具有兴奋作用,国际奥委会严禁运动员服用的药物是
(3)从用药安全角度考虑,使用前要进行皮肤敏感性测试的药物是
(4)
(5)为预防缺铁性贫血,一些食品中加入了铁元素(含Fe2+物质)。若向铁强化牛奶中滴加KSCN溶液,发现牛奶变为红色,说明
您最近一年使用:0次
4 . 分类法在化学学习中应用广泛。
(1)为了保护环境,应减少SO2在大气中的排放。SO2属于酸性氧化物,可与NaOH、___ (填与NaOH不同类别的一种具体物质)等反应。写出SO2与NaOH反应的化学方程式___ 。
(2)氯化铁(FeCl3)可用于金属蚀刻、污水处理等,是重要的化工原料。写出两个生成FeCl3的化学方程式(以含铁元素的不同类别物质 为原料)。
①___ 。
②___ 。
(1)为了保护环境,应减少SO2在大气中的排放。SO2属于酸性氧化物,可与NaOH、
(2)氯化铁(FeCl3)可用于金属蚀刻、污水处理等,是重要的化工原料。写出两个生成FeCl3的化学方程式(以含铁元素的
①
②
您最近一年使用:0次
名校
5 . 铁及其化合物在生产、生活中有及其重要的用途,请回答下列问题:
(1)FeCl3溶液呈黄色,FeCl3溶液的分散质是_______ ,分散剂是_______ 。
(2)Fe(OH)3是难溶于水的固体,那么分离Fe(OH)3与水的悬浊液常用的方法是________
(3)Fe(OH)3胶体呈红褐色,具有良好的净水效果。由饱和FeCl3溶液制备 Fe(OH)3胶体的化学方程式是________ 。
(4)鉴别FeCl3溶液和Fe(OH)3胶体,除了可通过观察颜色以外,还有的方法是_______ 。
(5)下列关于Fe(OH)3胶体和Fe(OH)3悬浊液的描述,正确的是_______
A.两者颜色相同 B.两者稳定性相同
C.两者的分子直径均大于100nm D.滴加稀盐酸后,两者现象完全相同
(6)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理,工业制备高铁酸钠 有多种方法,其中一种方法的原理可用离子方程式表示为 3ClO-+2Fe3++10OH-=2FeO +3Cl-+5H2O,则Na2FeO4中铁元素的化合价为
+3Cl-+5H2O,则Na2FeO4中铁元素的化合价为_______ ,该离子反应中氧化剂与还原剂的个数比为_______ ,生成1个高铁酸钠转移 _______ 个电子。
(1)FeCl3溶液呈黄色,FeCl3溶液的分散质是
(2)Fe(OH)3是难溶于水的固体,那么分离Fe(OH)3与水的悬浊液常用的方法是
(3)Fe(OH)3胶体呈红褐色,具有良好的净水效果。由饱和FeCl3溶液制备 Fe(OH)3胶体的化学方程式是
(4)鉴别FeCl3溶液和Fe(OH)3胶体,除了可通过观察颜色以外,还有的方法是
(5)下列关于Fe(OH)3胶体和Fe(OH)3悬浊液的描述,正确的是
A.两者颜色相同 B.两者稳定性相同
C.两者的分子直径均大于100nm D.滴加稀盐酸后,两者现象完全相同
(6)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理,工业制备高铁酸钠 有多种方法,其中一种方法的原理可用离子方程式表示为 3ClO-+2Fe3++10OH-=2FeO
 +3Cl-+5H2O,则Na2FeO4中铁元素的化合价为
+3Cl-+5H2O,则Na2FeO4中铁元素的化合价为
您最近一年使用:0次
名校
解题方法
6 . 某“铁基脱氧剂”的主要成分是还原 粉,使用一段时间后部分
粉,使用一段时间后部分 粉会变质为
粉会变质为 。将一包使用过一段时间后的脱氧剂用稀盐酸浸泡,浸泡过程中粉末表面有大量细小无色气泡产生。
。将一包使用过一段时间后的脱氧剂用稀盐酸浸泡,浸泡过程中粉末表面有大量细小无色气泡产生。
(1)溶液中的反应有: 、
、 、
、________________ 。
(2)甲同学用如下方法验证了溶液中 的存在:取少量上层清液,加入某试剂X,出现白色沉淀,并很快变为灰绿色,将沉淀倾倒在滤纸上,沉淀逐渐变为红褐色。试剂X为
的存在:取少量上层清液,加入某试剂X,出现白色沉淀,并很快变为灰绿色,将沉淀倾倒在滤纸上,沉淀逐渐变为红褐色。试剂X为____________ 。滤纸上沉淀变化反应的化学方程式为____________________________ 。
(3)乙同学另取少量上层溶液,滴加氯水后溶液呈棕黄色,再滴加 溶液,溶液变红。滴加氯水后溶液变棕黄的离子方程式为
溶液,溶液变红。滴加氯水后溶液变棕黄的离子方程式为____________________________ 。丙同学认为 不一定是由氯水反应得到的,理由是
不一定是由氯水反应得到的,理由是____________________________ ,改进方案是____________________________ 。
 粉,使用一段时间后部分
粉,使用一段时间后部分 粉会变质为
粉会变质为 。将一包使用过一段时间后的脱氧剂用稀盐酸浸泡,浸泡过程中粉末表面有大量细小无色气泡产生。
。将一包使用过一段时间后的脱氧剂用稀盐酸浸泡,浸泡过程中粉末表面有大量细小无色气泡产生。(1)溶液中的反应有:
 、
、 、
、(2)甲同学用如下方法验证了溶液中
 的存在:取少量上层清液,加入某试剂X,出现白色沉淀,并很快变为灰绿色,将沉淀倾倒在滤纸上,沉淀逐渐变为红褐色。试剂X为
的存在:取少量上层清液,加入某试剂X,出现白色沉淀,并很快变为灰绿色,将沉淀倾倒在滤纸上,沉淀逐渐变为红褐色。试剂X为(3)乙同学另取少量上层溶液,滴加氯水后溶液呈棕黄色,再滴加
 溶液,溶液变红。滴加氯水后溶液变棕黄的离子方程式为
溶液,溶液变红。滴加氯水后溶液变棕黄的离子方程式为 不一定是由氯水反应得到的,理由是
不一定是由氯水反应得到的,理由是
您最近一年使用:0次
2020-09-10更新
|
454次组卷
|
7卷引用:陕西省商洛市山阳中学2019-2020学年高一上学期期中考试化学试题
名校
解题方法
7 . 某班同学用如下实验探究 、
、 的性质。回答下列问题:
的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成 的溶液。在
的溶液。在 溶液中需加入少量铁屑,其目的是
溶液中需加入少量铁屑,其目的是______________ 。
(2)甲组同学取
 溶液,加入几滴氯水,再加入1滴
溶液,加入几滴氯水,再加入1滴 溶液,溶液变红,说明
溶液,溶液变红,说明 可将
可将 氧化。
氧化。 溶液与氯水反应的离子方程式为
溶液与氯水反应的离子方程式为___________ 。
(3)乙组同学认为甲组的实验不够严谨,该组同学在
 溶液中先加入
溶液中先加入 煤油,再于液面下依次加入几滴氯水和1滴
煤油,再于液面下依次加入几滴氯水和1滴 溶液,溶液变红,煤油的作用是
溶液,溶液变红,煤油的作用是__________ 。
 、
、 的性质。回答下列问题:
的性质。回答下列问题:(1)分别取一定量氯化铁、氯化亚铁固体,均配制成
 的溶液。在
的溶液。在 溶液中需加入少量铁屑,其目的是
溶液中需加入少量铁屑,其目的是(2)甲组同学取

 溶液,加入几滴氯水,再加入1滴
溶液,加入几滴氯水,再加入1滴 溶液,溶液变红,说明
溶液,溶液变红,说明 可将
可将 氧化。
氧化。 溶液与氯水反应的离子方程式为
溶液与氯水反应的离子方程式为(3)乙组同学认为甲组的实验不够严谨,该组同学在

 溶液中先加入
溶液中先加入 煤油,再于液面下依次加入几滴氯水和1滴
煤油,再于液面下依次加入几滴氯水和1滴 溶液,溶液变红,煤油的作用是
溶液,溶液变红,煤油的作用是
您最近一年使用:0次
2020-09-06更新
|
796次组卷
|
9卷引用:云南省育能高级中学2018-2019学年高一上学期期中考试化学试题
云南省育能高级中学2018-2019学年高一上学期期中考试化学试题河南省封丘县第一中学2018-2019学年高一下学期开学考试化学试题河北省武邑中学2019-2020学年高一12月月考化学试题人教版(2019)高一必修第一册第三章 铁 金属材料 高考挑战区吉林省(长春市)榆树市第一高级中学2021届高三10月月考化学试题(已下线)3.1.2 铁的氢氧化物 铁盐和亚铁盐(精练)-2020-2021学年上学期高一化学同步精品课堂(人教版必修第一册)湖南省常德市外国语学校2020-2021学年高一上学期第二次月考化学试题(已下线)周末培优4 金属及其化合物的实验题和工艺流程题-2021-2022学年高一化学课后培优练(人教版2019必修第一册)(已下线)【知识图鉴】单元讲练测必修第一册第三单元01讲核心
8 . 将一定量的铁粉投入FeCl3溶液中,两者恰好完全反应,完成下列问题。
(1)写出该反应的离子方程式并标出电子转移的方向和数目__________________ 。
(2)该反应中氧化产物和还原产物的物质的量之比为____________ 。
(3)若反应过程中转移了0.2mol电子,则溶解消耗的铁的质量为___________ 。
(4)如何检验某未知溶液中是否含有Fe3+________________________
(1)写出该反应的离子方程式并标出电子转移的方向和数目
(2)该反应中氧化产物和还原产物的物质的量之比为
(3)若反应过程中转移了0.2mol电子,则溶解消耗的铁的质量为
(4)如何检验某未知溶液中是否含有Fe3+
您最近一年使用:0次
2020-07-22更新
|
92次组卷
|
3卷引用:内蒙古呼和浩特市开来中学2019-2020学年高二下学期期中考试化学试题
9 . 分析下列反应并按要求填空。
(1) 铁与氯气在一定条件反应,写出化学反应方程式_________________ 其中氧化剂是____________ ;发生氧化反应的是____________ ,当1molFe反应时转移_____ mol电子
(2)取少量铁与氯气反应得到的固体溶于水,分装在两支试管中,若向其中一支试管滴加KSCN溶液,则溶液变成_____ 色。向另一支试管滴加NaOH溶液,现象为_________________ 离子反应的方程式为______________________ 。
(1) 铁与氯气在一定条件反应,写出化学反应方程式
(2)取少量铁与氯气反应得到的固体溶于水,分装在两支试管中,若向其中一支试管滴加KSCN溶液,则溶液变成
您最近一年使用:0次
解题方法
10 . 如图为铁及其化合物的“价-类”二维图。
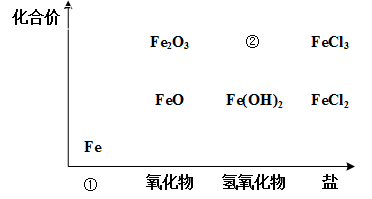
(1)填写二维图缺失的类别①___ 和化学式②___ 。
(2)某同学利用以下试剂研究FeCl3性质,进行了如下预测:
①Cl2②Fe ③NaOH ④H2SO4⑤AgNO3
从物质类别上看,FeCl3属于___ ,可能与___ 发生反应(填序号);
从化合价角度看,Fe3+具有___ 性,可能与___ 发生反应(填序号)。
(3)某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路,其化学原理为如下反应:Cu+2FeCl3=CuCl2+2FeCl2
①用单线桥表示电子转移。___ 。
②反应中FeCl3作___ 剂,理由是___ 。
③写出该反应的离子方程式___ 。

(1)填写二维图缺失的类别①
(2)某同学利用以下试剂研究FeCl3性质,进行了如下预测:
①Cl2②Fe ③NaOH ④H2SO4⑤AgNO3
从物质类别上看,FeCl3属于
从化合价角度看,Fe3+具有
(3)某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路,其化学原理为如下反应:Cu+2FeCl3=CuCl2+2FeCl2
①用单线桥表示电子转移。
②反应中FeCl3作
③写出该反应的离子方程式
您最近一年使用:0次
2019-11-15更新
|
322次组卷
|
3卷引用:北京市丰台区2019-2020学年高一上学期期中考试化学(A卷)试题



